Clear Sky Science · ja
ATPアーゼ N-エチルマレイミド感受性因子によるカルシウム依存的な融合ポア閉鎖とエンドサイトーシス
細胞はどうやって分泌小包を再利用するか
脳細胞、ホルモン分泌細胞、免疫細胞は毎秒のように小さな化学伝達物質のパケットを放出し、空になったパケットを素早く取り込み再利用しています。この迅速な出荷とリサイクルの仕組みが思考、血糖制御、免疫の円滑な働きを支えています。本稿の元になった研究は、そのリサイクルの謎の一片、つまり内容物を出す小さな開口部――「融合ポア」――がいつどのように閉じて、空の小胞が細胞内に引き戻されるのか、という点を明らかにします。
分泌小包のライフサイクル
多くの細胞はニューロトランスミッター、ホルモン、炎症性分子などの信号を小胞と呼ばれる泡状の小包に詰めて伝達します。これらの小胞は細胞表面へ移動し、外膜と一時的に結合して水で満たされた微小なトンネル――融合ポア――を形成し、その中を内容物が抜け出します。しばしば小胞は完全に融合するのではなく「キス・アンド・ラン」を行います:表面に触れて貨物を放出するのに十分な短時間だけポアを開き、そこでポアが閉じると小胞は回収されて再利用されます。この速く経済的なサイクルはタイミングに強く依存します。ポアを開く時間が短すぎれば信号が十分に出ず、閉じるのに失敗すればリサイクルが滞ります。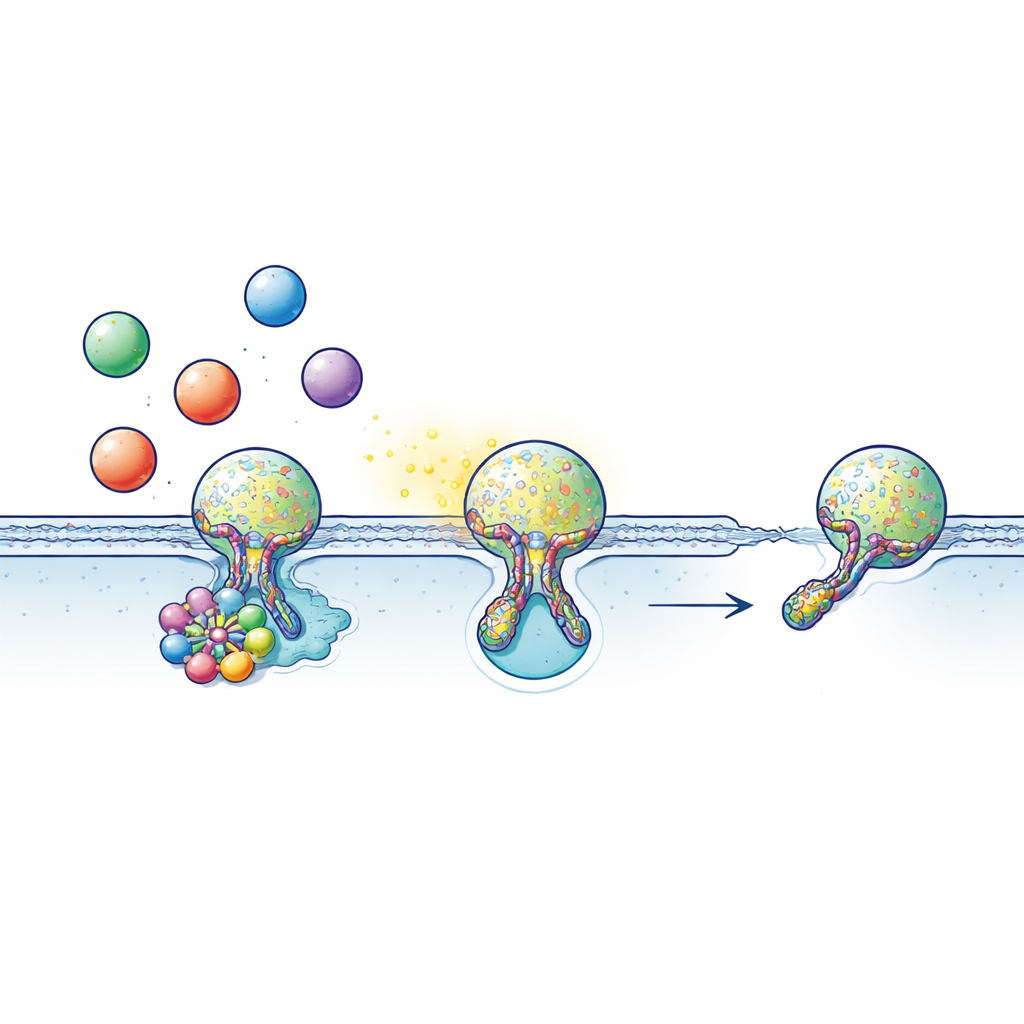
ポアに働く分子モーター
小胞の融合と回収は、小胞と細胞膜をつかんで引き寄せるタンパク質によって駆動されます。これらの「SNARE」タンパク質は両膜を接近させて融合ポアを開く緊密な束を形成します。本研究は別のタンパク質であるNSFに注目しています。NSFはATP(細胞のエネルギー)を用いてSNAREの束を仕事の後に分解する酵素です。細胞表面積の変化に敏感な電気記録と生きたままの共焦点イメージングを組み合わせ、著者らはラットの副腎ホルモン分泌細胞、感覚ニューロン、インスリン産生細胞で単一小胞の融合と回収を観察しました。化学的にNSFを阻害したり遺伝的に除去したりすることで、その活性が融合の前だけでなく後のポア閉鎖にも必要かどうかを検証できました。
NSFが止まるとポアは閉じられない
正常条件下では、これらの細胞の多くの小胞はキス・アンド・ランを行います:融合ポアは開き、短く明確な時間開いた後に閉じ、小胞は再び内部へ引き戻されます。研究者たちが薬でNSFのATP駆動活性を阻害したり機能を欠損させると、挙動に顕著な変化が現れました。小胞は膜に到達してポアは開き続けるものの、ポア閉鎖を完了するイベントの割合が大幅に減少しました。代わりに、小胞は表面に付着したままでポアが通常より遥かに長く開いた状態が続く傾向が出ました。この変化は非常に速いものから遅いもの、「オーバーシュート」として余分な膜が取り戻されるものを含む複数の様式のエンドサイトーシスの強い遅延または停止と合致しました。急速放出に備えた小胞プールの再補充も遅くなり、ポア閉鎖と小胞リサイクルが密接に結びついた過程であることが示されました。
カルシウムが導くリサイクルの選択
細胞はカルシウム依存的な経路と非依存的な経路の両方で小胞をリサイクルできます。著者らは脊髄神経節の感覚ニューロンでこれら二つの経路を比較しました。カルシウムが存在する条件では、NSFを阻害すると再取り込みが遅くなり、NSFがカルシウム刺激によるリサイクルに不可欠であることが示されました。しかし、電位駆動でカルシウムを伴わないリサイクルモードを誘発する刺激パターンを用いると、NSF阻害剤はほとんど影響を与えませんでした。この対比は、細胞が激しいシグナル伝達時に起こるカルシウムの急上昇のような状況に対処するためにNSFを専門的な道具として温存し、静かな基礎的リサイクルのためにはカルシウム非依存的な別経路を残していることを示唆します。
NSFはどうやって紐を引くのか
融合ポアでNSFが何をしているかを詳しく見るため、研究者らはSNAREタンパク質が束を作ると光る蛍光センサーを作り、その束が解体されると光が消えるようにしました。刺激中、これらのシグナルは小胞が融合した場所に現れ、ポアが閉じ小胞が回収される数秒以内に消えていきました。NSFを阻害すると、発光シグナルはずっと長く残り、SNARE束が解体されずに維持されていることを示しました。NSFのATPアーゼ活性の測定結果と合わせて、これらの結果はNSFが融合の後期段階でSNARE束を能動的に分解するという像を支持します。その分解がポアを締め、最終的にピンチオフしてキス・アンド・ランのサイクルを完了させるのに役立っているようです。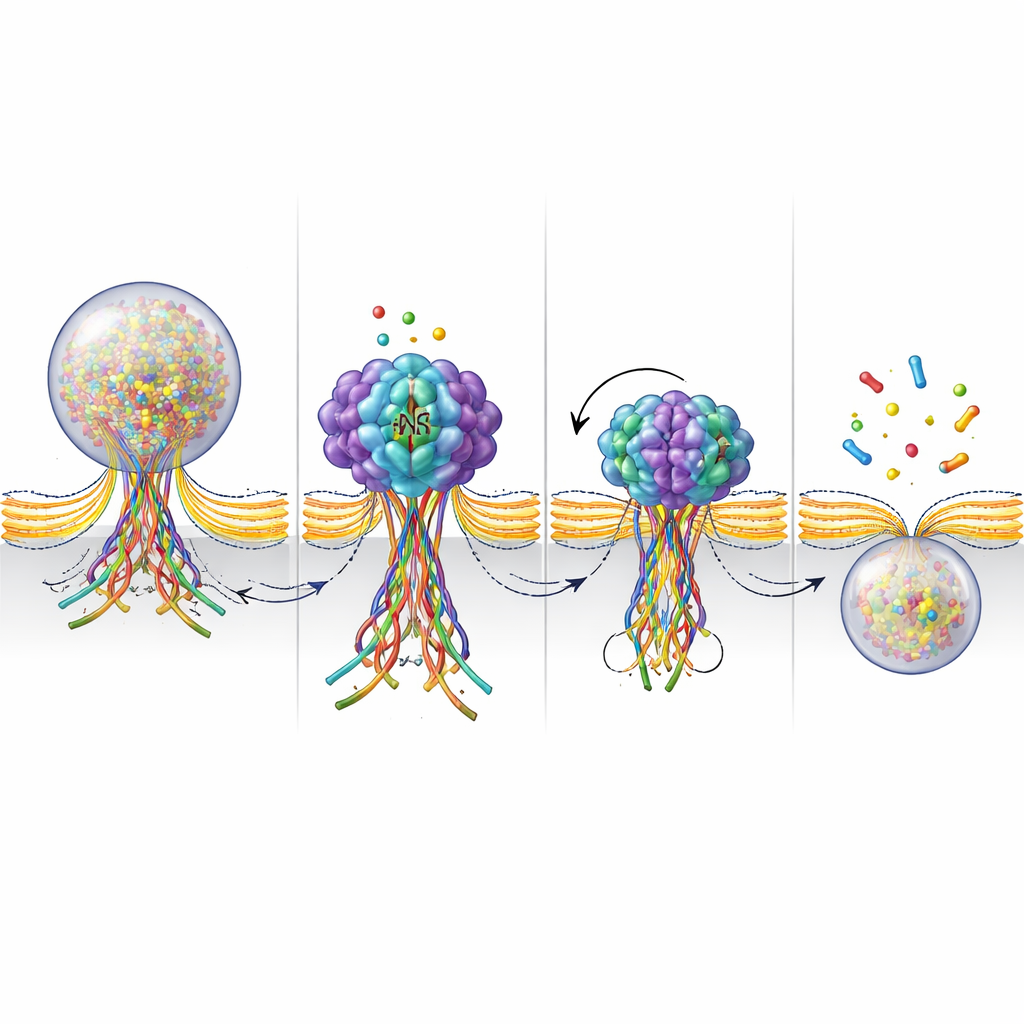
これは健康と病気にとってなぜ重要か
NSFのエネルギー駆動作用が融合ポアの閉鎖と小胞リサイクルの引き金となる中心的なスイッチであることを示すことで、この研究はよく知られた分子モーターを細胞間コミュニケーションの精密な制御につなげます。ホルモン分泌細胞、副腎クロマフィン細胞、特定のニューロンでは、この機構によりカルシウムの急増が起きるたびに小胞が迅速かつ確実に再利用されます。NSF機能が障害されるとポアが適切に閉じずリサイクルが遅れ、細胞は需要に追いつけなくなり、ストレス応答、痛みのシグナル、血糖調節などに問題をもたらす可能性があります。ポア閉鎖のこの段階を理解することは、小胞リサイクルの微妙な欠陥が神経学的・内分泌的疾患の基盤になり得る道を探る新たな手がかりを与え、将来の治療戦略の標的としてNSFを浮かび上がらせます。
引用: Wang, Y., Ma, S., Song, S. et al. ATPase N-ethylmaleimide-sensitive factor mediated calcium dependent fusion pore closure and endocytosis. Commun Biol 9, 495 (2026). https://doi.org/10.1038/s42003-026-09743-3
キーワード: 小胞リサイクリング, 融合ポア, エンドサイトーシス, カルシウムシグナル伝達, NSF ATPアーゼ