Clear Sky Science · es
Clausura del poro de fusión dependiente de calcio mediada por la ATPasa N-ethylmaleimide-sensitive factor y endocitosis
Cómo las células reutilizan sus paquetes secretos
Cada segundo, las células cerebrales, las células secretoras de hormonas y las células del sistema inmunitario liberan diminutos paquetes de mensajeros químicos y luego recuperan rápidamente los paquetes vacíos para reutilizarlos. Este sistema rápido de envío y reciclaje mantiene en marcha el pensamiento, el control de la glucemia y la inmunidad. El estudio que hay detrás de este artículo descubre una pieza faltante del rompecabezas del reciclaje: cómo la pequeña apertura que deja salir la carga —el “poro de fusión”— sabe cuándo y cómo cerrarse para que el paquete vacío pueda ser recogido de nuevo por la célula.
El ciclo de vida de un paquete secreto
Muchas células se comunican cargando señales como neurotransmisores, hormonas o moléculas inflamatorias en paquetes en forma de burbuja llamados vesículas. Estas vesículas se desplazan hasta la superficie celular y se unen brevemente con la membrana externa, formando un diminuto túnel lleno de agua —el poro de fusión— a través del cual escapan sus contenidos. A menudo, en lugar de fusionarse por completo, la vesícula realiza un “beso y huida”: toca la superficie, abre un poro el tiempo justo para liberar su carga, luego el poro se cierra y la vesícula se recupera para volver a usarse. Este ciclo rápido y económico depende de un tiempo crítico: si el poro se abre demasiado poco, no sale suficiente señal; si no se cierra, el sistema de reciclaje se atasca. 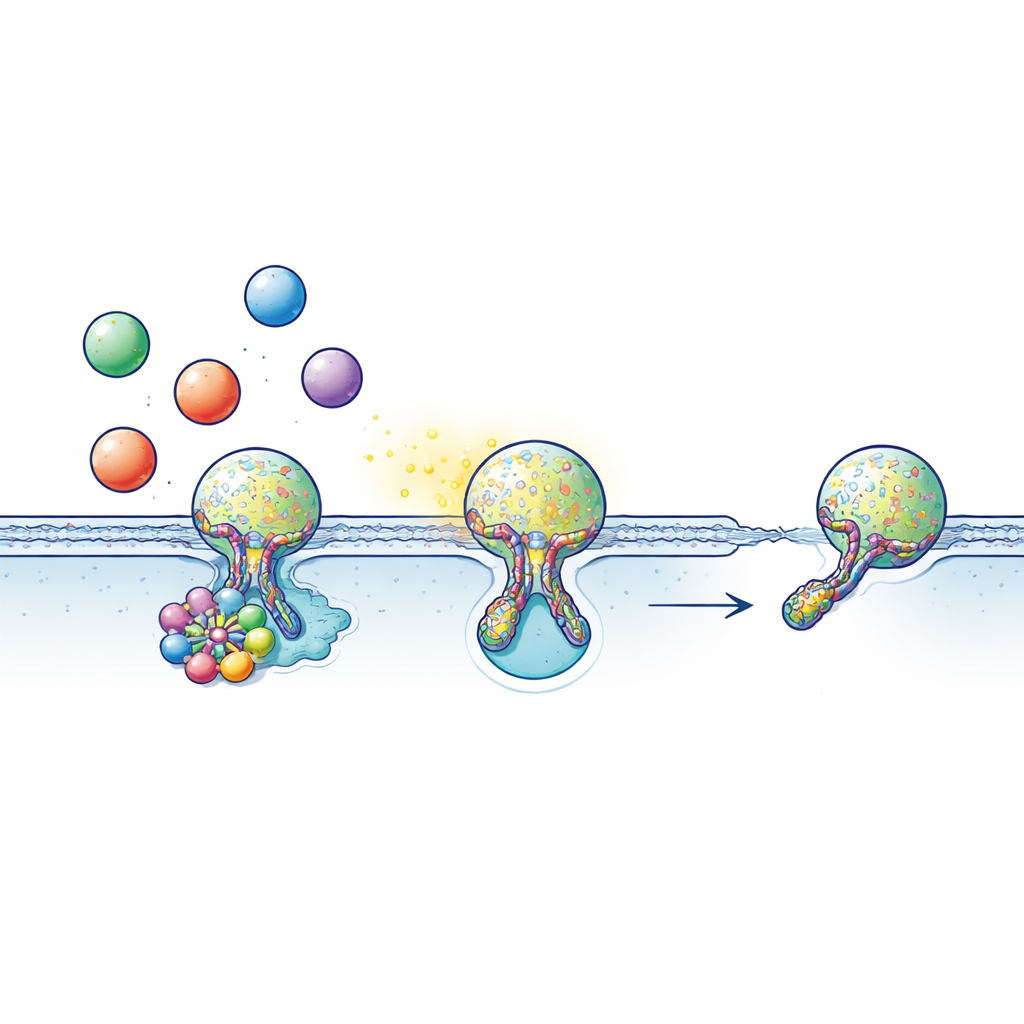
Un motor molecular en el poro
La fusión y la recuperación de vesículas están impulsadas por proteínas que agarran la vesícula y la membrana celular y las acercan como si tiraran de un cordón. Estas proteínas “SNARE” forman haces estrechos que acercan las dos membranas y abren el poro de fusión. El nuevo estudio se centra en otra proteína, NSF, una enzima que utiliza la energía del ATP —el combustible de la célula— para desmontar los haces SNARE después de que han cumplido su función. Mediante registros eléctricos sensibles a cambios en el área de la superficie celular junto con imágenes confocales en vivo, los autores observaron vesículas individuales fusionarse y ser recuperadas en células secretoras de hormonas de la glándula suprarrenal de rata, neuronas sensoriales y células productoras de insulina. Al bloquear químicamente NSF o eliminarlo genéticamente, pudieron comprobar si su actividad era necesaria no solo antes de la fusión, sino también para cerrar el poro después.
Cuando NSF se detiene, los poros se niegan a cerrarse
En condiciones normales, muchas vesículas en estas células realizan beso y huida: el poro de fusión se abre, permanece abierto un tiempo corto y bien definido, y luego se cierra para que la vesícula pueda ser recogida. Cuando los investigadores inhibieron la actividad impulsada por ATP de NSF con fármacos o lo suprimieron, observaron un cambio de comportamiento llamativo. Las vesículas seguían alcanzando la membrana y los poros aún podían abrirse, pero una fracción mucho menor de eventos completaba el cierre del poro. En su lugar, las vesículas tendían a permanecer adheridas a la superficie con poros que se mantenían abiertos durante mucho más tiempo de lo habitual. Este cambio se acompañó de una fuerte desaceleración o bloqueo de varias formas de endocitosis, incluyendo la recuperación muy rápida, más lenta y la denominada recuperación por “exceso” en la que se retira membrana adicional. El reservorio de vesículas listo para la liberación rápida también se rellenó más despacio, lo que demuestra que el cierre del poro y el reciclaje de vesículas son pasos estrechamente vinculados.
Opciones de reciclaje guiadas por calcio
Las células pueden reciclar vesículas de maneras dependientes e independientes del calcio. En neuronas sensoriales del ganglio de la raíz dorsal, el equipo comparó estas dos vías. Con calcio presente, bloquear NSF de nuevo ralentizó la recuperación tras la fusión vesicular, lo que indica que NSF es esencial para el reciclaje desencadenado por calcio. Pero cuando los científicos emplearon un patrón de estimulación que provoca un modo de reciclaje inducido por voltaje y sin calcio, los bloqueadores de NSF tuvieron poco efecto. Este contraste sugiere que las células reservan a NSF como una herramienta especializada para manejar ráfagas de actividad impulsadas por calcio, como las que ocurren durante señalizaciones intensas, mientras que mantienen una vía separada e independiente del calcio para sostener el reciclaje de fondo más tranquilo.
Cómo NSF tira de los hilos
Para observar más de cerca lo que hace NSF en el poro de fusión, los investigadores construyeron un sensor fluorescente que brilla cuando las proteínas SNARE forman un haz y se atenúa cuando ese haz se desmonta. Durante la estimulación, vieron aparecer estas señales donde las vesículas se fusionaban y luego desvanecerse en unos pocos segundos conforme el poro se cerraba y la vesícula se recuperaba. Cuando NSF fue bloqueado, la señal luminosa persistió mucho más tiempo, lo que indica que el haz SNARE permanecía ensamblado en lugar de desarmarse. Junto con mediciones de la actividad ATPasa —la acción de quema de combustible de NSF—, estos resultados apoyan un marco en el que NSF desmonta activamente los haces SNARE en una etapa tardía de la fusión. Ese desensamblaje parece ayudar a apretar y finalmente pinzar el poro, completando el ciclo de beso y huida. 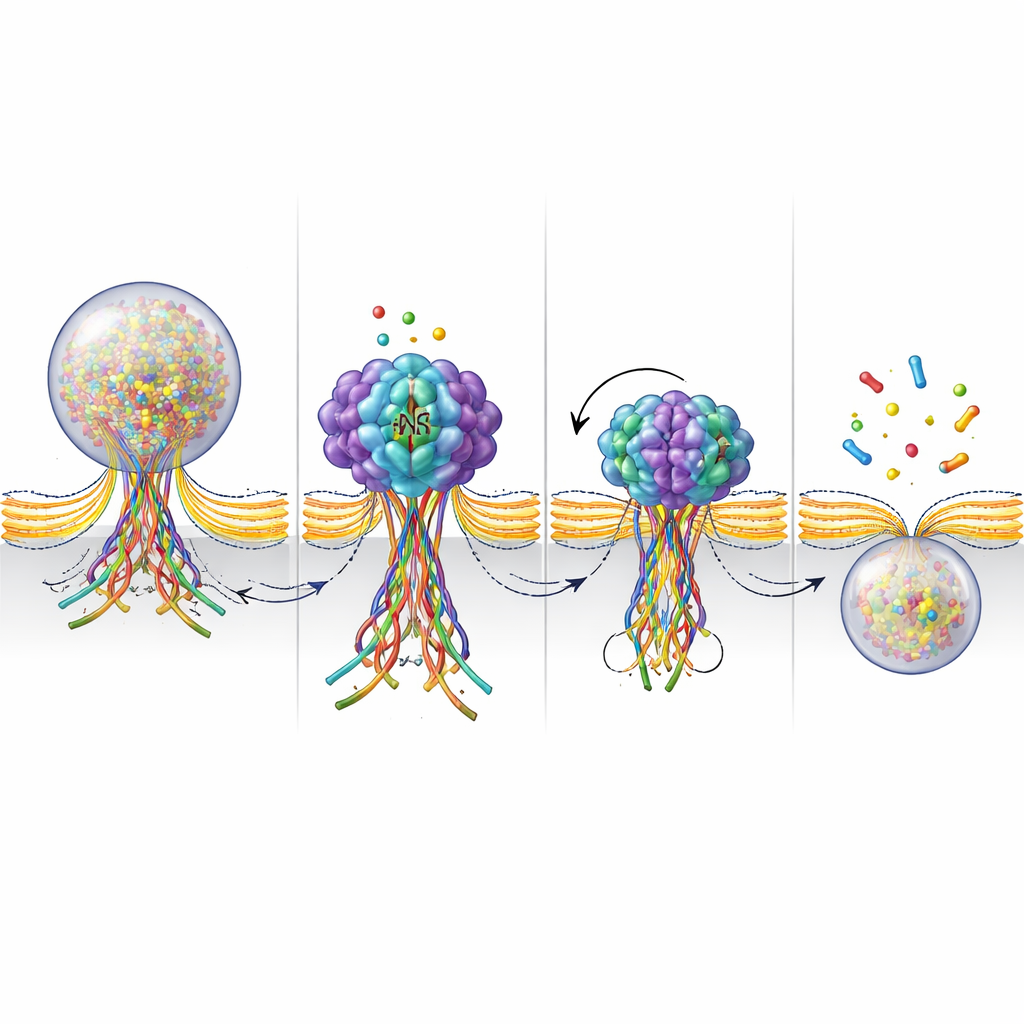
Por qué esto importa para la salud y la enfermedad
Al mostrar que la acción impulsada por energía de NSF es un interruptor central para cerrar el poro de fusión y desencadenar el reciclaje de vesículas, este trabajo vincula un motor molecular bien conocido con el control fino de la comunicación entre células. En células secretoras de hormonas, células cromafines suprarrenales y ciertas neuronas, este mecanismo asegura que las vesículas puedan reutilizarse de forma rápida y fiable cuando se producen picos de calcio. Si la función de NSF se ve alterada, los poros pueden no cerrarse correctamente, el reciclaje se ralentiza y las células pueden tener dificultades para mantener la demanda, lo que podría contribuir a problemas en las respuestas al estrés, la señalización del dolor o el control de la glucosa. Comprender este paso final de cierre abre nuevas vías para explorar cómo defectos sutiles en el reciclaje de vesículas podrían subyacer a trastornos neurológicos y endocrinos, y destaca a NSF como un posible blanco para futuras estrategias terapéuticas.
Cita: Wang, Y., Ma, S., Song, S. et al. ATPase N-ethylmaleimide-sensitive factor mediated calcium dependent fusion pore closure and endocytosis. Commun Biol 9, 495 (2026). https://doi.org/10.1038/s42003-026-09743-3
Palabras clave: reciclaje de vesículas, poro de fusión, endocitosis, señalización por calcio, ATPasa NSF