Clear Sky Science · nl
ATPase N-ethylmaleimide-sensitive factor gemedieerde calciumafhankelijke sluiting van de fusiepoort en endocytose
Hoe cellen hun geheime pakketjes hergebruiken
Elke seconde geven je hersencellen, hormoonafgevende cellen en immuuncellen kleine pakketjes chemische boodschappers af en nemen daarna snel de lege pakketjes weer in om ze opnieuw te gebruiken. Dit snelle zend-en-recycle-systeem houdt denken, bloedsuikerregulatie en immuniteit soepel draaiende. De studie achter dit artikel onthult een ontbrekend stuk van die recyclingpuzzel: hoe de kleine opening die de lading naar buiten laat — de “fusiepoort” — weet wanneer en hoe hij moet sluiten zodat het lege pakketje weer in de cel kan worden teruggetrokken.
De levenscyclus van een geheim pakketje
Veel cellen communiceren door signalen zoals neurotransmitters, hormonen of ontstekingsmoleculen in belachtige pakketjes te laden, vesikels genoemd. Deze vesikels bewegen naar het celoppervlak en verbinden zich kort met het buitenmembraan, waardoor een klein met water gevuld tunnelletje ontstaat — de fusiepoort — waardoor hun inhoud ontsnapt. Vaak, in plaats van volledig te fuseren, voert het vesikel een “kiss-and-run” uit: het raakt het oppervlak aan, opent een poort net lang genoeg om zijn lading vrij te geven, daarna sluit de poort en wordt het vesikel teruggehaald om opnieuw te worden gebruikt. Deze snelle, zuinige cyclus hangt kritisch af van timing: open de fusiepoort te kort en er komt te weinig signaal uit; faalt de sluiting dan stokt het recyclingsysteem. 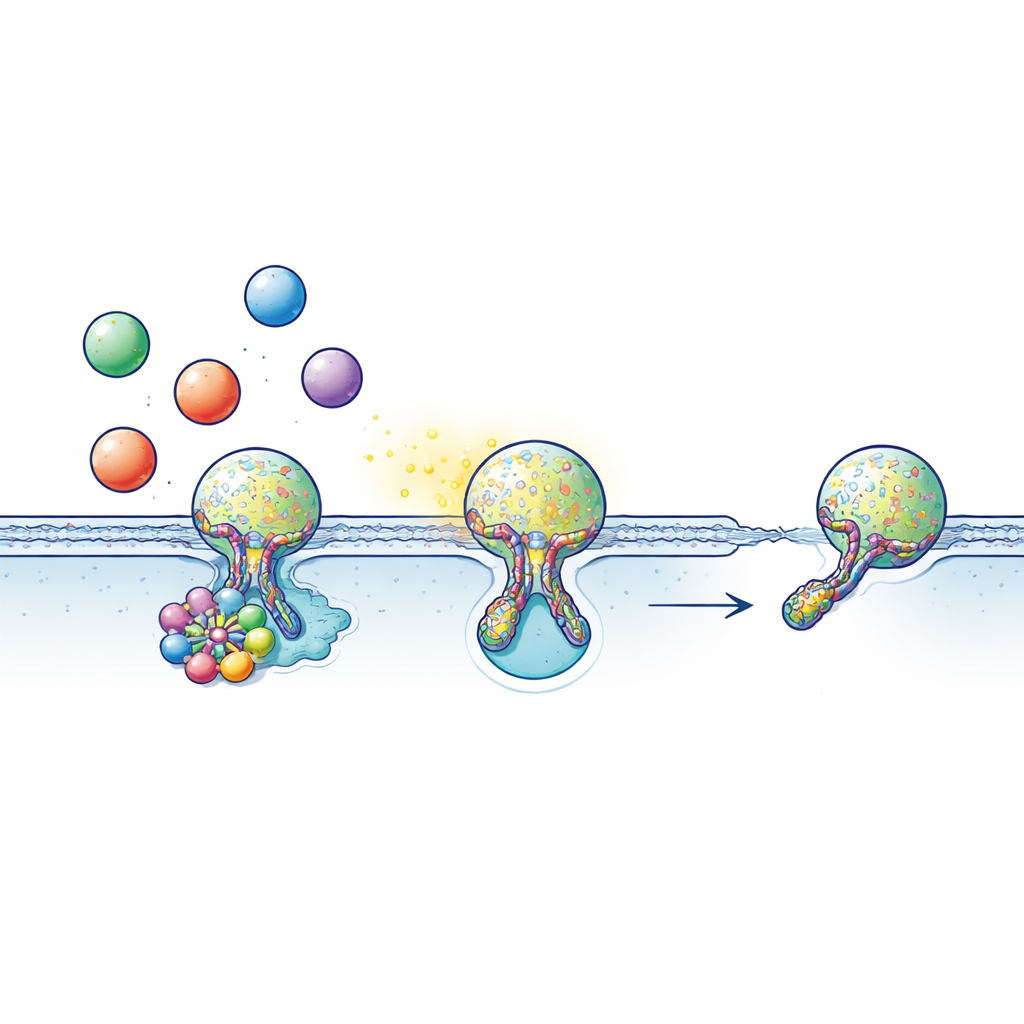
Een moleculaire motor bij de poort
Vesikelversmelting en terugwinning worden aangedreven door eiwitten die het vesikel en het celmembraan vastgrijpen en ze samen trekken als een treksluiting. Deze “SNARE”-eiwitten vormen strakke bundels die de twee membranen in contact brengen en de fusiepoort openen. De nieuwe studie richt zich op een ander eiwit, NSF, een enzym dat energie van ATP — de brandstof van de cel — gebruikt om SNARE-bundels uit elkaar te halen nadat ze hun werk hebben gedaan. Met elektrische opnames die gevoelig zijn voor veranderingen in celoppervlakte, gecombineerd met levende confocale beeldvorming, observeerden de auteurs individuele vesikels die fuseerden en werden teruggewonnen in ratten bijnierhormoon-afgevende cellen, sensorische neuronen en insulineproducerende cellen. Door NSF chemisch te blokkeren of genetisch te verwijderen, konden ze testen of de activiteit ervan niet alleen vóór fusie nodig is, maar ook voor het sluiten van de poort daarna.
Wanneer NSF hapert, weigeren poorten te sluiten
Onder normale omstandigheden ondergaan veel vesikels in deze cellen kiss-and-run: de fusiepoort opent, blijft een korte, goed gedefinieerde tijd open en sluit dan zodat het vesikel weer naar binnen kan worden getrokken. Toen de onderzoekers NSF’s ATP-gedreven activiteit met geneesmiddelen inhibeerden of het uitschakelden, zagen ze een opvallende gedragsverandering. Vesikels bereikten nog steeds het membraan en poorten konden nog steeds openen, maar een veel kleiner deel van de gebeurtenissen voltooide de sluiting van de poort. In plaats daarvan bleven vesikels vaak aan het oppervlak vastzitten met poorten die veel langer openbleven dan gebruikelijk. Deze verandering ging gepaard met een sterke vertraging of blokkade van verschillende vormen van endocytose, inclusief zeer snelle, langzamere en ‘overshoot’-terugwinning waarbij extra membraan teruggenomen wordt. De pool van vesikels die klaarstonden voor snelle vrijgave werd ook trager bijgevuld, wat laat zien dat poortsluiting en vesikelrecycling nauw verbonden stappen zijn.
Calciumgestuurde recyclingkeuzes
Cellen kunnen vesikels recyclen op zowel calciumafhankelijke als calciumonafhankelijke manieren. In sensorische neuronen van de dorsale ganglion vergeleek het team deze twee routes. Met calcium aanwezig vertraagde het blokkeren van NSF opnieuw de terugwinning na vesikelfusie, wat aangeeft dat NSF essentieel is voor calcium-geïnduceerde recycling. Maar toen de wetenschappers een stimuleringspatroon gebruikten dat een calciumvrije, spanningsgestuurde recyclagemodus uitlokte, hadden NSF-blokkers weinig effect. Dit contrast suggereert dat cellen NSF reserveren als een gespecialiseerd instrument voor het omgaan met uitbarstingen van calcium-gestuurde activiteit, zoals die optreden tijdens intense signalering, terwijl een afzonderlijke, calciumonafhankelijke route de rustigere, achtergrondrecycling ondersteunt.
Hoe NSF aan de touwtjes trekt
Om beter te begrijpen wat NSF doet bij de fusiepoort, bouwden de onderzoekers een fluorescerende sensor die oplicht wanneer SNARE-eiwitten een bundel vormen en dimt wanneer die bundel uit elkaar wordt gehaald. Tijdens stimulatie zagen ze deze signalen verschijnen op de plekken waar vesikels fuseerden en daarna binnen enkele seconden vervagen terwijl de poort sloot en het vesikel werd teruggewonnen. Wanneer NSF werd geblokkeerd, bleef het oplichtende signaal veel langer aanwezig, wat aangeeft dat de SNARE-bundel gemonteerd bleef in plaats van te worden gedemonteerd. Samen met metingen van ATPase-activiteit — NSF’s brandstofverbruikende werking — ondersteunen deze resultaten een beeld waarin NSF actief SNARE-bundels ontmantelt in een laat stadium van fusie. Die ontmanteling lijkt te helpen de poort aan te trekken en uiteindelijk af te knellen, waarmee de kiss-and-run-cyclus wordt voltooid. 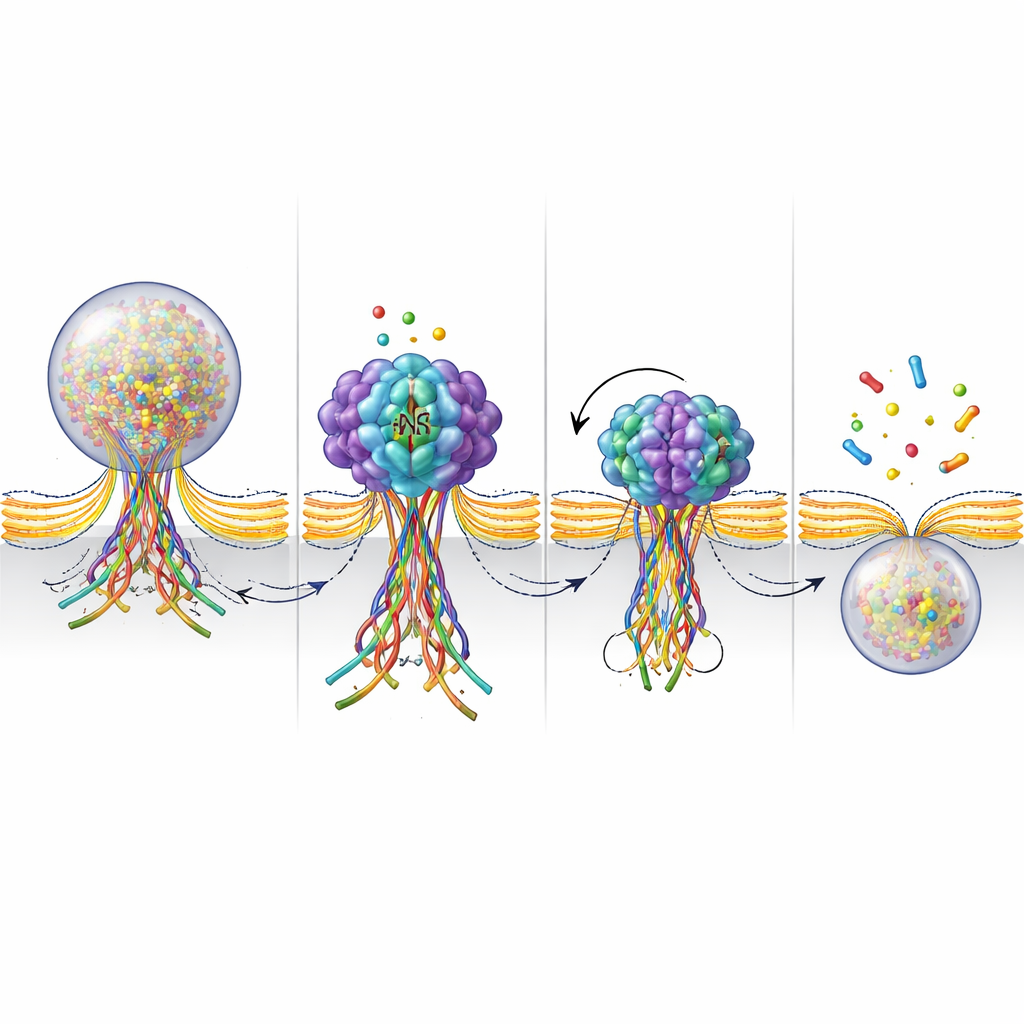
Waarom dit belangrijk is voor gezondheid en ziekte
Door aan te tonen dat NSF’s energiegedreven werking een centrale schakel is voor het sluiten van de fusiepoort en het in gang zetten van vesikelrecycling, koppelt dit werk een bekend moleculair motor aan de fijne regeling van cel-tot-celcommunicatie. In hormoonafgevende cellen, bijnier-chromaffine cellen en bepaalde neuronen zorgt dit mechanisme ervoor dat vesikels snel en betrouwbaar kunnen worden hergebruikt telkens wanneer calciumpiekjes optreden. Als NSF-functie verstoord is, kunnen poorten mogelijk niet goed sluiten, vertraagt recycling en worstelen cellen om aan de vraag te voldoen, wat mogelijk bijdraagt aan problemen in stressreacties, pijnsignalisatie of bloedsuikerregulatie. Het begrijpen van deze sluitingsstap opent nieuwe wegen om te onderzoeken hoe subtiele defecten in vesikelrecycling ten grondslag kunnen liggen aan neurologische en endocriene aandoeningen, en benadrukt NSF als een potentiële doelwit voor toekomstige therapeutische strategieën.
Bronvermelding: Wang, Y., Ma, S., Song, S. et al. ATPase N-ethylmaleimide-sensitive factor mediated calcium dependent fusion pore closure and endocytosis. Commun Biol 9, 495 (2026). https://doi.org/10.1038/s42003-026-09743-3
Trefwoorden: vesikelrecycling, fusiepoort, endocytose, calciumsignaal, NSF ATPase