Clear Sky Science · pl
ATPaza N-ethylmaleimidowrażliwy czynnik (NSF) pośredniczy w zależnym od wapnia zamykaniu poru fuzji i endocytozie
Jak komórki ponownie wykorzystują swoje sekretorowe paczki
Co sekundę komórki mózgowe, komórki wydzielające hormony i komórki układu odpornościowego uwalniają maleńkie pakunki chemicznych przekaźników, a następnie szybko pobierają opróżnione pakunki z powrotem do wnętrza w celu ponownego użycia. Ten szybki system wysyłki i recyklingu utrzymuje w sprawności myślenie, kontrolę poziomu glukozy we krwi i odporność. Badanie opisane w tym tekście odsłania brakujące ogniwo układanki recyklingowej: w jaki sposób małe ujście pozwalające na wypływ ładunku — „por fuzji” — wie, kiedy i jak się zamknąć, aby puste pęcherzyki mogły zostać ponownie pobrane do komórki.
Cykl życia sekretorowego pakunku
Wiele komórek komunikuje się, ładując sygnały takie jak neuroprzekaźniki, hormony czy cząsteczki zapalne do pęcherzyków przypominających bańki. Te pęcherzyki przemieszczają się do powierzchni komórki i krótkotrwale łączą z błoną zewnętrzną, tworząc maleńki wypełniony wodą tunel — por fuzji — przez który wydostają się ich treści. Często zamiast całkowitego scalenia, pęcherzyk wykonuje tzw. „kiss-and-run”: dotyka powierzchni, otwiera por na tyle długo, by uwolnić ładunek, potem por zamyka się i pęcherzyk jest odzyskiwany do ponownego użycia. Ten szybki, oszczędny cykl zależy krytycznie od czasu: jeśli por jest otwarty zbyt krótko, za mało sygnału zostanie uwolnione; jeśli nie zamknie się, system recyklingu zablokuje się. 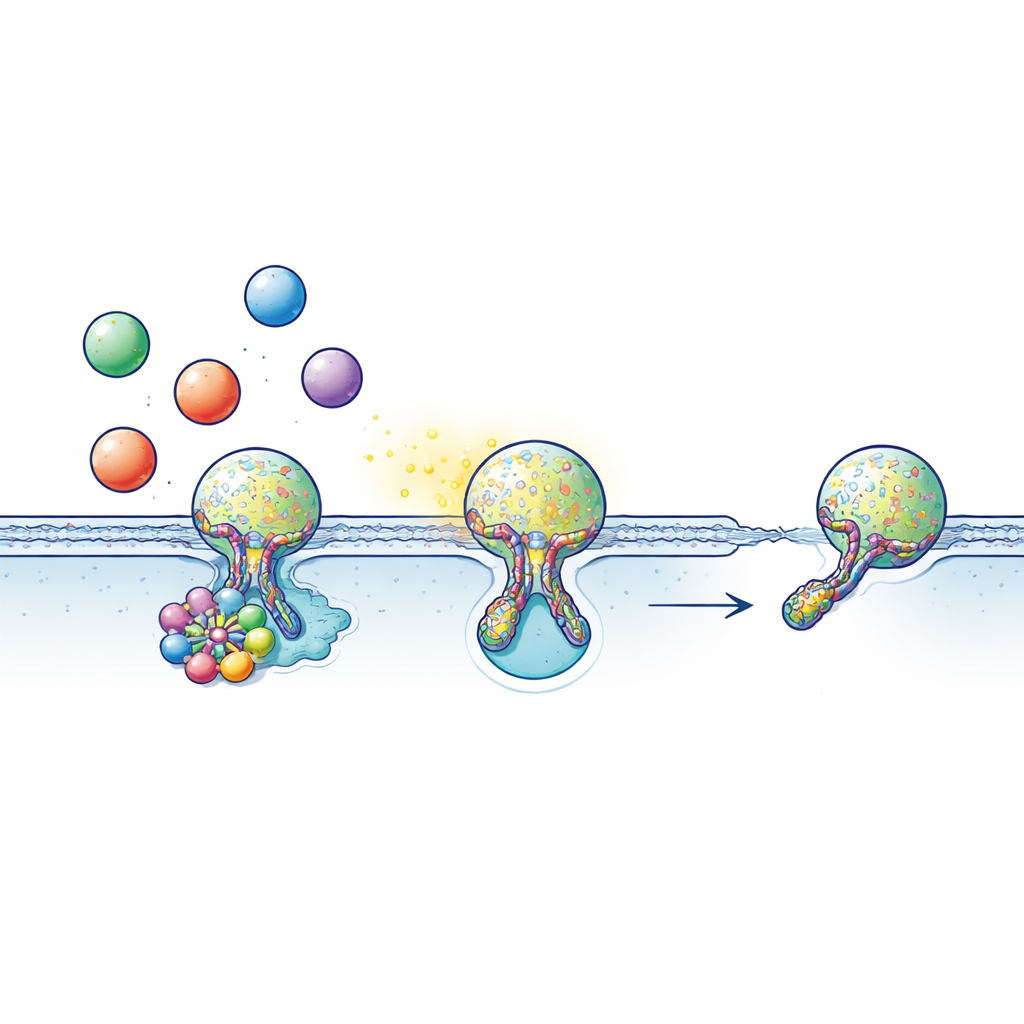
Molekularny motor przy porze
Fuzja pęcherzyków i ich odzyskiwanie są napędzane przez białka, które chwytają pęcherzyk i błonę komórkową i zaciągają je razem jak sznurek w worku. Te białka „SNARE” tworzą zwarte wiązki, które zbliżają dwie błony i otwierają por fuzji. Nowe badanie koncentruje się na innym białku, NSF — enzymie wykorzystującym energię z ATP, paliwa komórkowego — do rozmontowywania wiązek SNARE po wykonaniu przez nie zadania. Korzystając z zapisu elektrycznego wrażliwego na zmiany powierzchni komórki oraz obrazowania konfokalnego na żywo, autorzy obserwowali pojedyncze pęcherzyki łączące się i odzyskiwane w komórkach nadnerczowych wydzielających hormony, neuronach czuciowych i komórkach produkujących insulinę. Chemicznie blokując NSF lub usuwając je genetycznie, mogli przetestować, czy jego aktywność jest potrzebna nie tylko przed fuzją, ale także do zamknięcia poru po niej.
Gdy NSF zaciąga hamulec, pory odmawiają zamknięcia
W normalnych warunkach wiele pęcherzyków w tych komórkach podlega mechanizmowi kiss-and-run: por fuzji otwiera się, pozostaje otwarty przez krótki, dobrze określony czas, a następnie zamyka się, by pęcherzyk mógł zostać wciągnięty z powrotem. Gdy badacze zahamowali aktywność ATP-ową NSF za pomocą leków lub wyeliminowali je, zaobserwowali uderzającą zmianę zachowania. Pęcherzyki nadal docierały do błony i pory nadal mogły się otwierać, ale znacznie mniejsza część zdarzeń kończyła się zamknięciem poru. Zamiast tego pęcherzyki miały tendencję do pozostawania przyczepionymi do powierzchni z porami, które pozostawały otwarte znacznie dłużej niż zwykle. Zmiana ta szła w parze ze znacznym spowolnieniem lub zablokowaniem kilku rodzajów endocytozy, włączając bardzo szybki, wolniejszy i tzw. „overshoot” — odzyskiwanie z nadmiarem pobranej błony. pula pęcherzyków gotowych do szybkiego uwolnienia również była uzupełniana wolniej, co pokazuje, że zamknięcie poru i recykling pęcherzyków są ze sobą ściśle powiązanymi etapami.
Recykling sterowany wapniem
Komórki mogą recyklingować pęcherzyki zarówno w sposób zależny od wapnia, jak i niezależny od wapnia. W neuronach czuciowych z zwoju rdzeniowego grzbietowego zespół porównał te dwie ścieżki. W obecności wapnia blokowanie NSF ponownie spowolniło odzyskiwanie po fuzji pęcherzyków, co wskazuje, że NSF jest niezbędne dla wapniem wywołanego recyklingu. Jednak gdy naukowcy zastosowali wzorzec stymulacji wywołujący tryb recyklingu zależny od napięcia i pozbawiony wapnia, bloker NSF miał niewielki efekt. Ten kontrast sugeruje, że komórki rezerwują NSF jako wyspecjalizowane narzędzie do obsługiwania napływów aktywności zależnej od wapnia, takich jak te występujące podczas intensywnego sygnalizowania, pozostawiając jednocześnie oddzielną ścieżkę niezależną od wapnia do obsługi spokojniejszego, tła recyklingu.
Jak NSF pociąga za sznurki
Aby przyjrzeć się bliżej funkcji NSF przy porze fuzji, badacze skonstruowali fluorescencyjny sensor, który świeci, gdy białka SNARE tworzą wiązkę, i przygasa, gdy ta wiązka zostaje rozebrana. Podczas stymulacji widziano te sygnały pojawiające się w miejscach, gdzie pęcherzyki się łączyły, a potem gasnące w ciągu kilku sekund, gdy por zamykał się, a pęcherzyk był odzyskiwany. Gdy NSF było zablokowane, świecący sygnał utrzymywał się znacznie dłużej, co wskazuje, że wiązka SNARE pozostawała złożona zamiast być rozmontowana. W połączeniu z pomiarami aktywności ATPazy — paliwowego działania NSF — wyniki te wspierają obraz, w którym NSF aktywnie rozkłada wiązki SNARE na późnym etapie fuzji. Ten rozkład wydaje się pomagać w domknięciu i ostatecznym odcięciu poru, kończąc cykl kiss-and-run. 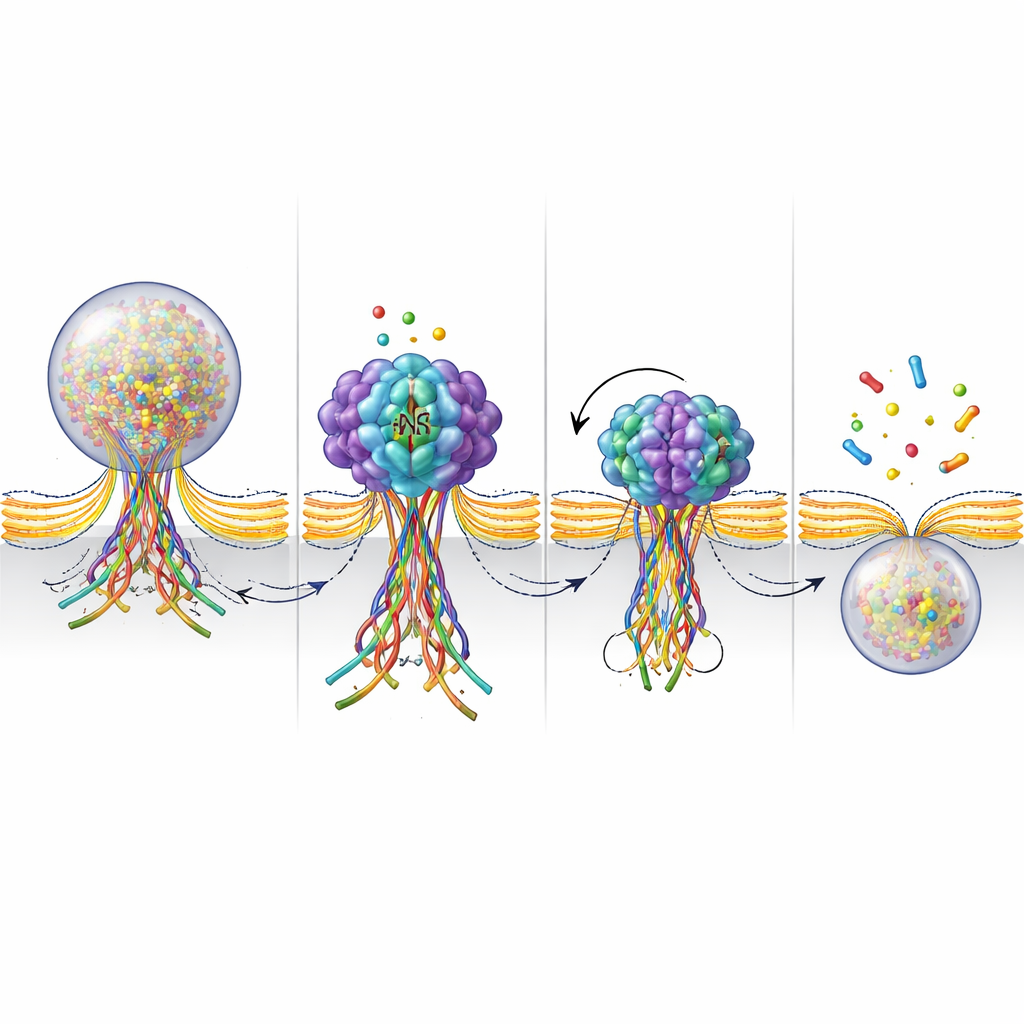
Znaczenie dla zdrowia i chorób
Pokazując, że działanie napędzane energią NSF jest centralnym przełącznikiem zamykającym por fuzji i wyzwalającym recykling pęcherzyków, ta praca łączy dobrze znany molekularny motor z precyzyjną kontrolą komunikacji międzykomórkowej. W komórkach wydzielających hormony, komórkach chromafinowych nadnerczy i niektórych neuronach mechanizm ten zapewnia, że pęcherzyki mogą być ponownie wykorzystywane szybko i niezawodnie za każdym razem, gdy pojawiają się skoki wapnia. Jeśli funkcja NSF zostanie zaburzona, pory mogą nie zamykać się prawidłowo, recykling zwalnia, a komórki mogą mieć trudności z nadążeniem za zapotrzebowaniem, co potencjalnie przyczynia się do zaburzeń w odpowiedzi na stres, przekazywaniu bólu czy kontroli poziomu glukozy. Zrozumienie tego etapu zamykania otwiera nowe drogi do badania, w jaki sposób subtelne defekty w recyklingu pęcherzyków mogą leżeć u podstaw zaburzeń neurologicznych i endokrynologicznych, oraz wskazuje NSF jako potencjalny cel przyszłych strategii terapeutycznych.
Cytowanie: Wang, Y., Ma, S., Song, S. et al. ATPase N-ethylmaleimide-sensitive factor mediated calcium dependent fusion pore closure and endocytosis. Commun Biol 9, 495 (2026). https://doi.org/10.1038/s42003-026-09743-3
Słowa kluczowe: recykling pęcherzyków, por fuzji, endocytoza, sygnalizacja wapniowa, ATPaza NSF