Clear Sky Science · it
Chiusura del poro di fusione dipendente dal calcio mediata dall’ATPasi sensibile a N-etilmaleimmide (NSF) e endocitosi
Come le cellule riutilizzano i loro pacchetti segreti
Ogni secondo, le cellule del cervello, le cellule che secernono ormoni e le cellule del sistema immunitario rilasciano minuscoli pacchetti di messaggeri chimici per poi recuperare rapidamente i pacchetti vuoti per un riutilizzo. Questo sistema rapido di invio e riciclo mantiene fluidi processi come il pensiero, il controllo della glicemia e l’immunità. Lo studio descritto in questo articolo svela un pezzo mancante del puzzle del riciclo: come la piccola apertura che lascia uscire il carico — il “poro di fusione” — sa quando e come richiudersi così che il pacchetto vuoto possa essere riportato dentro la cellula.
Il ciclo di vita di un pacchetto segreto
Molte cellule comunicano caricando segnali come neurotrasmettitori, ormoni o molecole infiammatorie in pacchetti a forma di bolla chiamati vescicole. Queste vescicole si avvicinano alla superficie cellulare e si uniscono brevemente con la membrana esterna, formando un piccolo tunnel riempito d’acqua — il poro di fusione — attraverso il quale il contenuto fuoriesce. Spesso, invece di fondersi completamente, la vescicola compie un “kiss-and-run”: tocca la superficie, apre un poro appena il tempo necessario per rilasciare il carico, poi il poro si richiude e la vescicola viene recuperata per essere riutilizzata. Questo ciclo rapido ed economico dipende in modo critico dal timing: aprire il poro troppo poco significa che non esce abbastanza segnale; non chiuderlo significa che il sistema di riciclo si blocca. 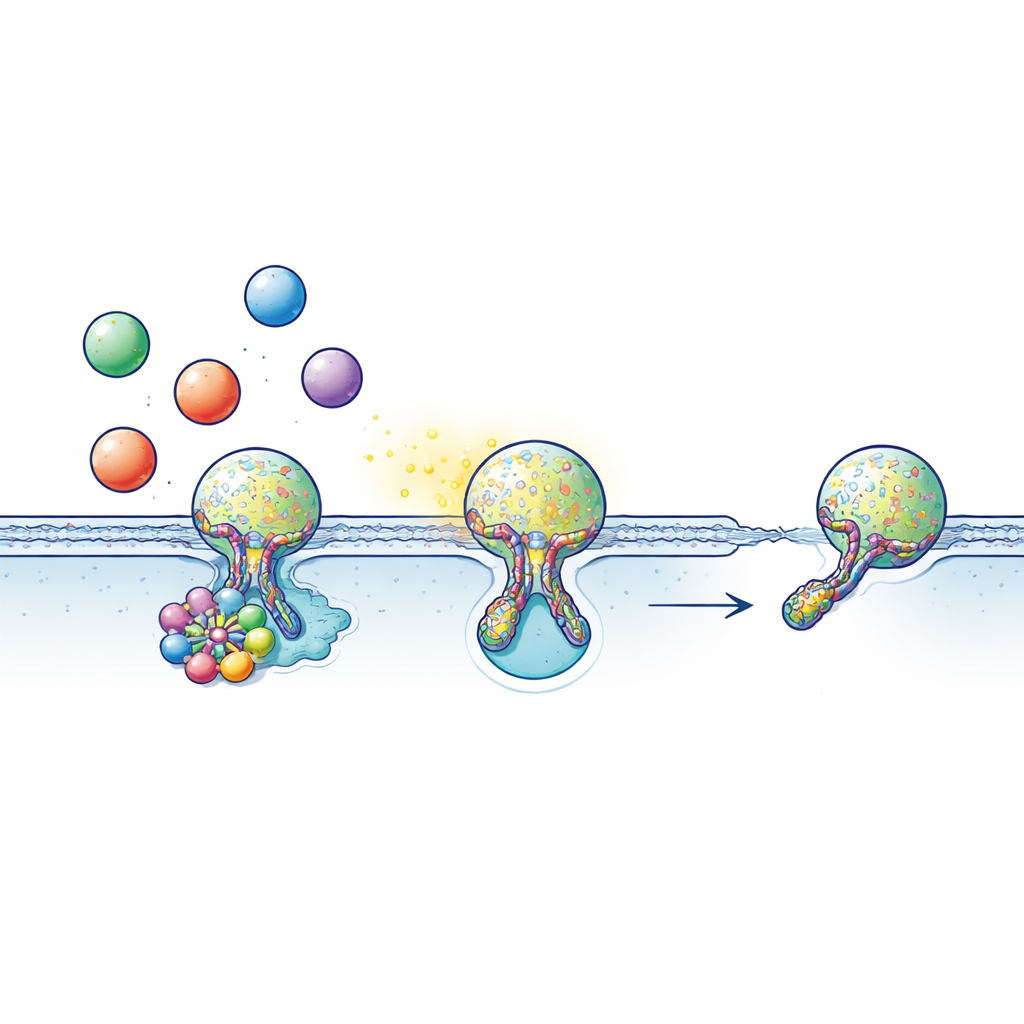
Un motore molecolare al poro
La fusione e il recupero delle vescicole sono guidati da proteine che afferrano la vescicola e la membrana cellulare e le tirano insieme come un cordoncino. Queste proteine “SNARE” formano fasci stretti che avvicinano le due membrane e aprono il poro di fusione. Il nuovo studio si concentra su un’altra proteina, NSF, un enzima che usa l’energia dell’ATP — il carburante della cellula — per smontare i fasci di SNARE una volta che hanno svolto il loro compito. Utilizzando registrazioni elettriche sensibili ai cambiamenti dell’area della superficie cellulare insieme all’imaging confocale in vivo, gli autori hanno osservato singole vescicole fondersi e venire recuperate in cellule cromaffini surrenali di ratto, neuroni sensoriali e cellule produttrici di insulina. Bloccando chimicamente NSF o rimuovendolo geneticamente, hanno potuto testare se la sua attività sia necessaria non solo prima della fusione, ma anche per la chiusura del poro successiva.
Quando NSF si blocca, i pori si rifiutano di chiudere
In condizioni normali, molte vescicole in queste cellule seguono il comportamento kiss-and-run: il poro di fusione si apre, rimane aperto per un breve e definito intervallo, poi si richiude così che la vescicola possa essere riportata all’interno. Quando i ricercatori hanno inibito l’attività ATP-dipendente di NSF con farmaci o lo hanno eliminato, hanno osservato un marcato cambiamento nel comportamento. Le vescicole raggiungevano comunque la membrana e i pori potevano ancora aprirsi, ma una frazione molto più piccola di eventi completava la chiusura del poro. Invece, le vescicole tendevano a rimanere attaccate alla superficie con pori che restavano aperti molto più a lungo del normale. Questo cambiamento è andato di pari passo con un forte rallentamento o blocco di diverse modalità di endocitosi, incluse forme molto rapide, più lente e l’indagine “overshoot” in cui viene riassorbita una quantità supplementare di membrana. Anche il serbatoio di vescicole pronte per il rilascio rapido veniva ricaricato più lentamente, mostrando che la chiusura del poro e il riciclo delle vescicole sono fasi strettamente collegate.
Scelte di riciclo guidate dal calcio
Le cellule possono riciclare le vescicole sia in modo dipendente dal calcio sia in modo indipendente dal calcio. Nei neuroni sensoriali del ganglio della radice dorsale, il gruppo ha confrontato queste due vie. In presenza di calcio, bloccare NSF ha nuovamente rallentato il recupero dopo la fusione delle vescicole, indicando che NSF è essenziale per il riciclo innescato dal calcio. Ma quando gli scienziati hanno usato un pattern di stimolazione che provoca una modalità di riciclo indotta dalla variazione di potenziale e priva di calcio, gli inibitori di NSF hanno avuto poco effetto. Questo contrasto suggerisce che le cellule riservino NSF come strumento specializzato per gestire esplosioni di attività guidate dal calcio, come quelle che si verificano durante una segnalazione intensa, lasciando invece una via separata e indipendente dal calcio per sostenere il riciclo di fondo più tranquillo.
Come NSF tira le fila
Per osservare più da vicino cosa fa NSF al poro di fusione, i ricercatori hanno costruito un sensore fluorescente che si illumina quando le proteine SNARE formano un fascio e si attenua quando quel fascio viene smontato. Durante la stimolazione, hanno visto questi segnali apparire nei punti in cui le vescicole si fondevano e poi svanire entro pochi secondi mentre il poro si chiudeva e la vescicola veniva recuperata. Quando NSF era bloccato, il segnale luminoso persisteva molto più a lungo, indicando che il fascio di SNARE rimaneva assemblato invece di essere smantellato. Insieme alle misure dell’attività ATPasica — l’azione di consumo di carburante di NSF — questi risultati supportano un quadro in cui NSF smonta attivamente i fasci di SNARE in una fase tardiva della fusione. Questo smontaggio sembra aiutare a stringere e infine staccare il poro, completando il ciclo kiss-and-run. 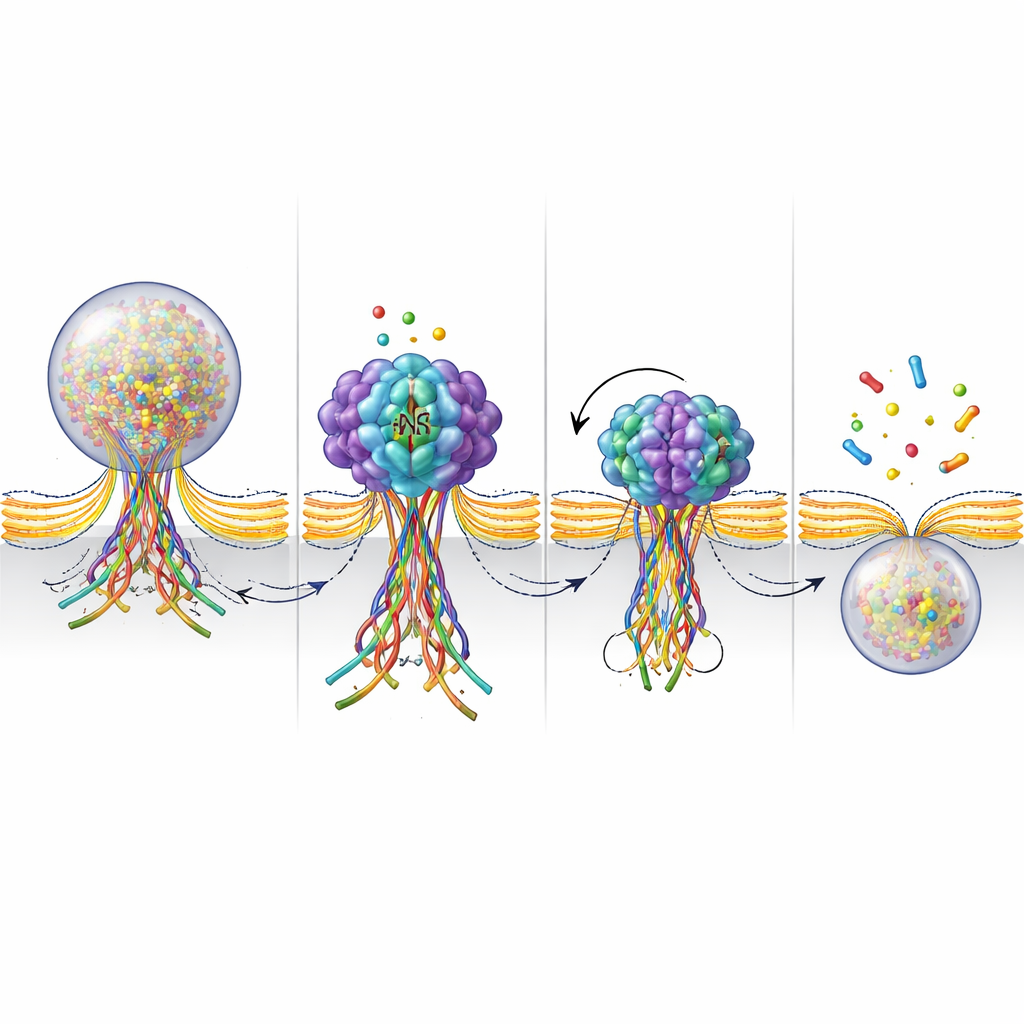
Perché questo conta per la salute e la malattia
Dimostrando che l’azione guidata dall’energia di NSF è un interruttore centrale per la chiusura del poro di fusione e l’innesco del riciclo delle vescicole, questo lavoro collega un noto motore molecolare al controllo fine della comunicazione cellula-cellula. Nelle cellule che secernono ormoni, nelle cellule cromaffini surrenali e in alcuni neuroni, questo meccanismo garantisce che le vescicole possano essere riutilizzate rapidamente e in modo affidabile ogni volta che ci sono ondate di calcio. Se la funzione di NSF viene alterata, i pori potrebbero non chiudersi correttamente, il riciclo rallentare e le cellule faticare a far fronte alla domanda, contribuendo potenzialmente a problemi nelle risposte allo stress, nella trasmissione del dolore o nel controllo della glicemia. Comprendere questo passaggio di chiusura apre nuove strade per esplorare come difetti sottili nel riciclo delle vescicole possano essere alla base di disturbi neurologici ed endocrini, e mette in evidenza NSF come possibile bersaglio per future strategie terapeutiche.
Citazione: Wang, Y., Ma, S., Song, S. et al. ATPase N-ethylmaleimide-sensitive factor mediated calcium dependent fusion pore closure and endocytosis. Commun Biol 9, 495 (2026). https://doi.org/10.1038/s42003-026-09743-3
Parole chiave: riciclo delle vescicole, poro di fusione, endocitosi, segnalazione del calcio, ATPasi NSF