Clear Sky Science · ar
إغلاق منفذ الاندماج المعتمد على الكالسيوم بوساطة إنزيم ATPase الحساس لـ N-ethylmaleimide والالتقام الخلوي
كيف تعيد الخلايا استخدام طرودها الإفرازية
كل ثانية، تُطلق خلايا الدماغ وخلايا إفراز الهرمونات والخلايا المناعية حزمًا صغيرة من الرسل الكيميائية ثم تعيد سريعًا استرجاع الحزم الفارغة لاستخدامها مجددًا. هذا النظام السريع للشحن وإعادة التدوير يحافظ على سير العمليات مثل التفكير وتنظيم سكر الدم والمناعة بسلاسة. تكشف الدراسة الواردة في هذا المقال عن قطعة مفقودة من لغز إعادة التدوير: كيف يعرف الفتحة الصغيرة التي تخرّج الحمولة — «منفذ الاندماج» — متى وكيف تُغلق حتى يمكن سحب الحويصلة الفارغة إلى داخل الخلية.
دورة حياة الحزمة الإفرازية
تتواصل كثير من الخلايا بتحميل إشارات مثل الناقلات العصبية أو الهرمونات أو الجزيئات الالتهابية داخل حويصلات تشبه الفقاعات. تتحرك هذه الحويصلات إلى سطح الخلية وتندمج لفترة وجيزة مع الغشاء الخارجي، مكونة نفقًا مملوءًا بالماء — منفذ الاندماج — الذي تهرب عبره المحتويات. غالبًا، بدلًا من الاندماج الكامل، تقوم الحويصلة بما يُسمى «التقبيل والهرب»: تلامس السطح، تفتح منفذًا لفترة وجيزة كافية لإطلاق حمولة، ثم يُغلق المنفذ وتُسترجع الحويصلة لاستخدامها مجددًا. تعتمد هذه الدورة السريعة والاقتصادية اعتمادًا حاسمًا على التوقيت: إن غُلف المنفذ قليلًا فلا يخرج إشعار كافٍ؛ وإن فشل الإغلاق يتعطّل نظام إعادة التدوير. 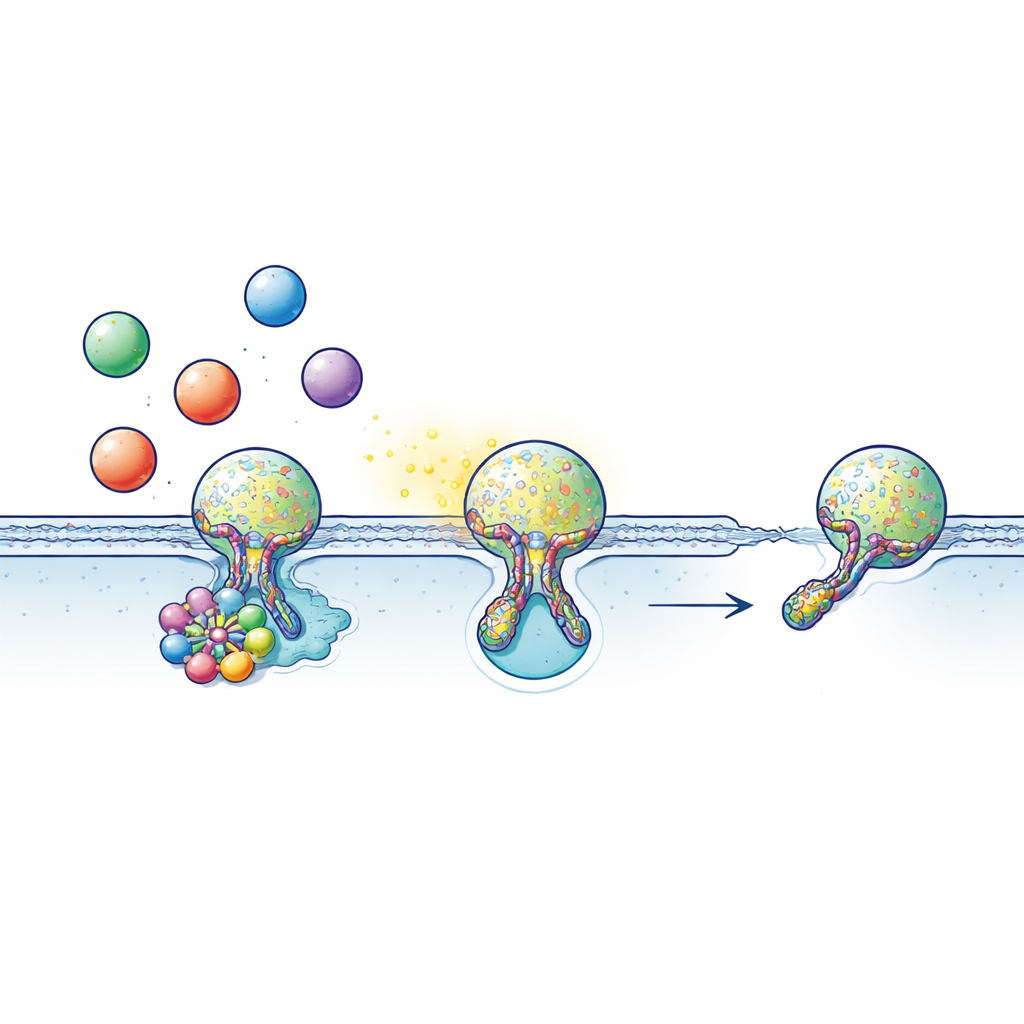
محرك جزيئي عند المنفذ
تقود بروتينات تمسك الحويصلة وغشاء الخلية وتشدّهما معًا مثل حبل مشدود عملية اندماج الحويصلات واسترجاعها. تشكل هذه البروتينات المسماة «SNARE» حزمًا محكمة تقرب الغشاءين من بعضهما وتفتح منفذ الاندماج. تركز الدراسة الجديدة على بروتين آخر، NSF، وهو إنزيم يستخدم طاقة ATP — وقود الخلية — لتفكيك حزم SNARE بعد أن تنتهي من عملها. باستخدام تسجيلات كهربائية حساسة لتغيرات مساحة سطح الخلية إلى جانب تصوير كونفوكالي حي، راقب المؤلفون اندماج حويصلات مفردة واسترجاعها في خلايا إفراز هرمونات الغدة الكظرية للفئران، والخلايا العصبية الحسية، وخلايا إنتاج الإنسولين. من خلال حجب NSF كيميائيًا أو إزالته جينيًا، تمكنوا من اختبار ما إذا كانت نشاطاته مطلوبة ليس فقط قبل الاندماج، بل أيضًا لإغلاق المنفذ بعده.
عندما يتعطل NSF، ترفض المنافذ الإغلاق
في الظروف الطبيعية، تمر العديد من الحويصلات في هذه الخلايا بعملية التقبيل والهرب: يفتح منفذ الاندماج، يبقى مفتوحًا لفترة قصيرة ومحددة، ثم يُغلق حتى تُسحب الحويصلة إلى الداخل. عندما أوقف الباحثون نشاط NSF المعتمد على ATP بواسطة أدوية أو حذفوه جينيًا، لاحظوا تغيرًا لافتًا في السلوك. لا تزال الحويصلات تصل إلى الغشاء ولا تزال الفتحات تُفتح، لكن جزءًا أصغر بكثير من الأحداث يكمل إغلاق المنفذ. بدلًا من ذلك، تميل الحويصلات إلى البقاء متصلة بالسطح مع منافذ تبقى مفتوحة لفترات أطول بكثير من المعتاد. جاء هذا التغير مصحوبًا بتباطؤ شديد أو حجب لأنماط متعددة من الالتقام الخلوي، بما في ذلك الاسترجاع السريع جدًا والأبطأ ونمط «الارتداد الزائد» الذي يُؤخذ فيه غشاء إضافي إلى الداخل. كما أعيد ملء مخزون الحويصلات الجاهزة للإفراز السريع ببطء أكبر، مما يدل على أن إغلاق المنفذ وإعادة تدوير الحويصلات خطوتان مرتبطتان ارتباطًا وثيقًا.
خيارات إعادة التدوير الموجهة بالكالسيوم
يمكن للخلايا إعادة تدوير الحويصلات بطرق معتمدة على الكالسيوم وأخرى مستقلة عنه. في الخلايا العصبية الحسية للعقدة الجذرية الظهرية، قارن الفريق بين هذين المسارين. بوجود الكالسيوم، أدى حجب NSF مرة أخرى إلى إبطاء الاسترجاع بعد اندماج الحويصلة، مما يشير إلى أن NSF أساسي لإعادة التدوير المحفزة بالكالسيوم. لكن عندما استخدم العلماء نمط تحفيز يثير نمط إعادة تدوير معتمد على فرق الجهد وخالٍ من الكالسيوم، كان لمثبطات NSF تأثير ضئيل. يقترح هذا التباين أن الخلايا تحتفظ بـ NSF كأداة متخصصة للتعامل مع دفعات النشاط المحفزة بالكالسيوم، مثل تلك الحادثة أثناء الإشارات المكثفة، بينما تترك مسارًا منفصلًا مستقلًا عن الكالسيوم لدعم إعادة التدوير الأهدأ والخلفي.
كيف يشد NSF الخيوط
للحصول على صورة أدق لما يفعله NSF عند منفذ الاندماج، بنى الباحثون مستشعرًا فلوريًا يضيء عندما تتجمع بروتينات SNARE في حزمة ويخفت عندما تُفكك تلك الحزمة. أثناء التحفيز، رصدوا هذه الإشارات تظهر في مواقع اندماج الحويصلات ثم تتلاشى خلال ثوانٍ قليلة مع إغلاق المنفذ واسترجاع الحويصلة. عندما حُجب NSF، ظلّت الإشارة المضيئة لفترة أطول بكثير، مما يشير إلى أن حزمة SNARE بقيت متجمعة بدلًا من أن تُفكك. إلى جانب قياسات نشاط ATPase — عمل حرق الوقود لدى NSF — تدعم هذه النتائج صورة مفادها أن NSF يفكك بنشاط حزم SNARE في مرحلة متأخرة من الاندماج. ويبدو أن هذا التفكيك يساعد على تضييق المنفذ وفي النهاية قَصْفه، مُكملًا دورة التقبيل والهرب. 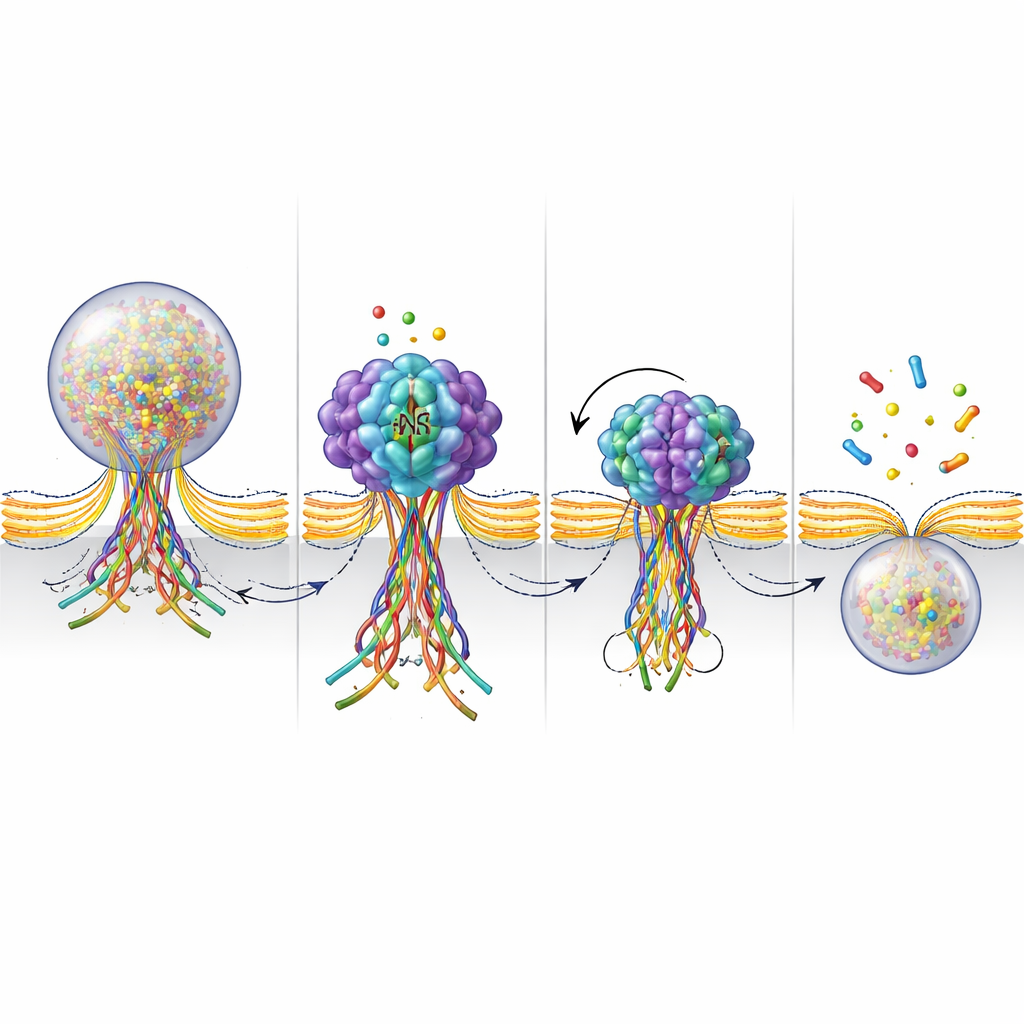
لماذا يهم هذا للصحة والمرض
من خلال إظهار أن فعل NSF المعتمد على الطاقة يعد مفتاحًا مركزيًا لإغلاق منفذ الاندماج وتحفيز إعادة تدوير الحويصلات، تربط هذه الدراسة محركًا جزيئيًا معروفًا بالتحكم الدقيق في التواصل بين الخلايا. في خلايا إفراز الهرمونات وخلايا الكرومافين في الغدة الكظرية وبعض الخلايا العصبية، تضمن هذه الآلية أن الحويصلات قابلة لإعادة الاستخدام بسرعة وبثبات كلما ارتفعت موجات الكالسيوم. إذا تعطلت وظيفة NSF، فقد تفشل المنافذ في الإغلاق بشكل صحيح، ويتباطأ إعادة التدوير، وقد تكافح الخلايا لمجاراة الطلب، مما قد يسهم في مشكلات في استجابات التوتر، ونقل إحساس الألم، أو تنظيم سكر الدم. يفتح فهم هذه الخطوة النهائية مسارات جديدة لاستكشاف كيف قد تكمن العيوب الطفيفة في إعادة تدوير الحويصلات وراء اضطرابات عصبية وغدية، ويبرز NSF كهدف محتمل لاستراتيجيات علاجية مستقبلية.
الاستشهاد: Wang, Y., Ma, S., Song, S. et al. ATPase N-ethylmaleimide-sensitive factor mediated calcium dependent fusion pore closure and endocytosis. Commun Biol 9, 495 (2026). https://doi.org/10.1038/s42003-026-09743-3
الكلمات المفتاحية: إعادة تدوير الحويصلات, منفذ الاندماج, الالتقام الخلوي, إشارات الكالسيوم, NSF ATPase