Clear Sky Science · fr
Fermeture du pore de fusion dépendante du calcium médiée par l’ATPase N‑ethylmaleimide‑sensitive factor et endocytose
Comment les cellules réutilisent leurs paquets secrets
Chaque seconde, vos cellules cérébrales, les cellules sécrétant des hormones et les cellules immunitaires libèrent de minuscules paquets de messagers chimiques puis récupèrent rapidement les paquets vidés pour les réutiliser. Ce système rapide d’envoi et de recyclage maintient la pensée, la régulation de la glycémie et l’immunité en bon ordre. L’étude à l’origine de cet article révèle un élément manquant de ce puzzle du recyclage : comment la petite ouverture qui laisse sortir le contenu — le « pore de fusion » — sait quand et comment se refermer pour que le paquet vide puisse être repris dans la cellule.
Le cycle de vie d’un paquet secret
Beaucoup de cellules communiquent en chargeant des signaux tels que des neurotransmetteurs, des hormones ou des molécules inflammatoires dans des emballages en forme de bulle appelés vésicules. Ces vésicules se déplacent vers la surface cellulaire et se joignent brièvement à la membrane externe, formant un minuscule tunnel rempli d’eau — le pore de fusion — par lequel leur contenu s’échappe. Souvent, au lieu de fusionner complètement, la vésicule effectue un « kiss‑and‑run » : elle touche la surface, ouvre un pore juste assez longtemps pour libérer sa cargaison, puis le pore se referme et la vésicule est récupérée pour être réutilisée. Ce cycle rapide et économique dépend de manière critique du timing : ouvrir le pore de fusion trop peu longtemps et le signal ne sort pas suffisamment ; ne pas le refermer et le système de recyclage s’enraye. 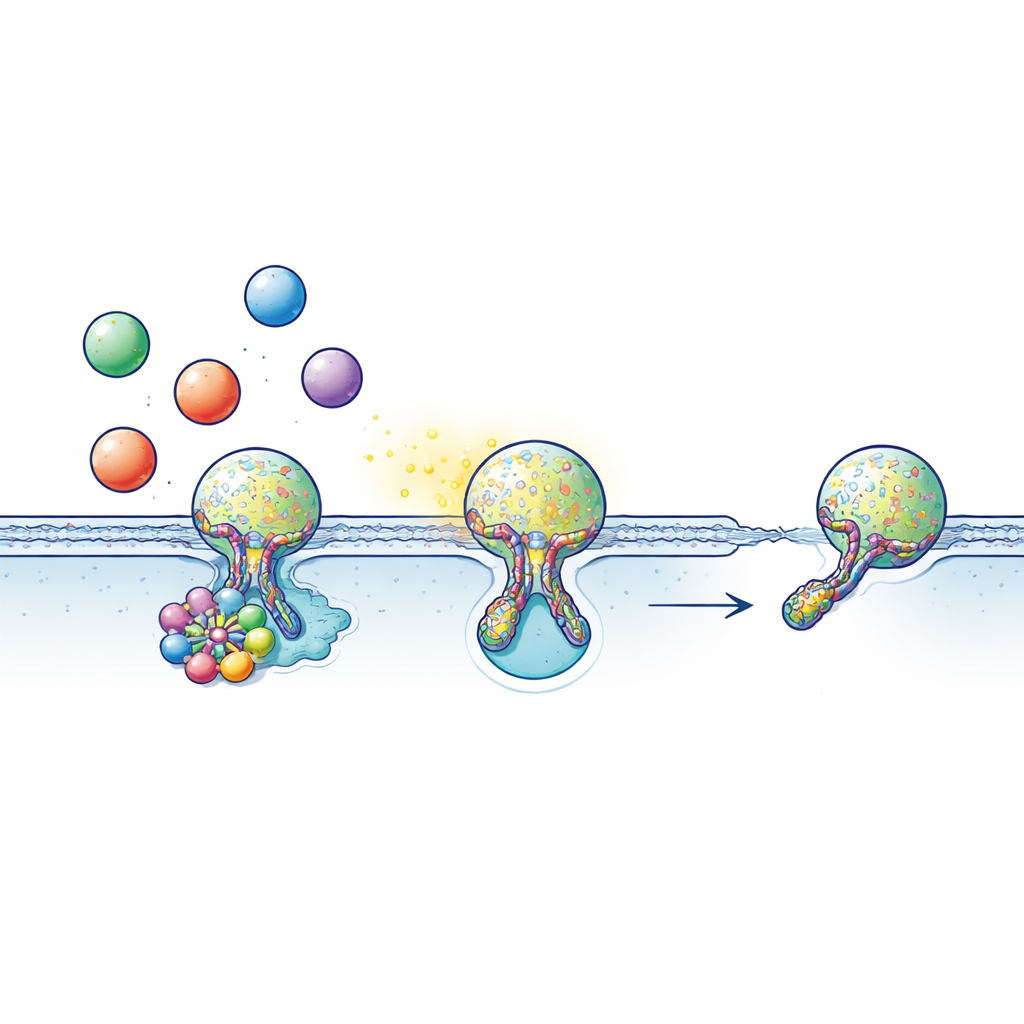
Un moteur moléculaire au niveau du pore
La fusion et la récupération des vésicules sont assurées par des protéines qui saisissent la vésicule et la membrane cellulaire et les rapprochent comme un cordon de serrage. Ces protéines « SNARE » forment des faisceaux serrés qui mettent les deux membranes en contact et ouvrent le pore de fusion. La nouvelle étude se concentre sur une autre protéine, NSF, une enzyme qui utilise l’énergie de l’ATP — le carburant de la cellule — pour défaire les faisceaux SNARE une fois leur travail accompli. En combinant des enregistrements électriques sensibles aux changements de surface cellulaire et de l’imagerie confocale en direct, les auteurs ont observé des vésicules individuelles fusionner et être récupérées dans des cellules endocrines médullosurrénales de rat, des neurones sensoriels et des cellules productrices d’insuline. En bloquant chimiquement NSF ou en le supprimant génétiquement, ils ont pu tester si son activité est requise non seulement avant la fusion, mais aussi pour la fermeture du pore ensuite.
Quand NSF cale, les pores refusent de se fermer
Dans des conditions normales, de nombreuses vésicules dans ces cellules suivent le mode kiss‑and‑run : le pore de fusion s’ouvre, reste ouvert pendant un temps court et bien défini, puis se referme pour que la vésicule puisse être ramenée à l’intérieur. Lorsque les chercheurs ont inhibé l’activité ATP‑dépendante de NSF avec des médicaments ou l’ont supprimé, ils ont observé un changement de comportement frappant. Les vésicules atteignaient encore la membrane et les pores pouvaient toujours s’ouvrir, mais une fraction beaucoup plus faible d’événements aboutissait à la fermeture du pore. Au lieu de cela, les vésicules restaient souvent attachées à la surface avec des pores ouverts bien plus longtemps que d’habitude. Ce changement s’accompagnait d’un fort ralentissement ou d’un blocage de plusieurs formes d’endocytose, y compris la récupération très rapide, plus lente, et la récupération en « overshoot » où une quantité supplémentaire de membrane est reprise. Le pool de vésicules prêtes à la libération rapide se reconstituait aussi plus lentement, montrant que la fermeture du pore et le recyclage des vésicules sont des étapes étroitement liées.
Des choix de recyclage guidés par le calcium
Les cellules peuvent recycler les vésicules de façon dépendante ou indépendante du calcium. Dans les neurones sensoriels du ganglion de la racine dorsale, l’équipe a comparé ces deux voies. En présence de calcium, le blocage de NSF ralentissait à nouveau la récupération après fusion des vésicules, indiquant que NSF est essentiel pour le recyclage déclenché par le calcium. Mais lorsque les scientifiques ont utilisé un protocole de stimulation favorisant un mode de recyclage induit par la tension sans calcium, les bloqueurs de NSF eurent peu d’effet. Ce contraste suggère que les cellules réservent NSF comme un outil spécialisé pour gérer les poussées d’activité dépendantes du calcium, comme celles qui se produisent lors d’une signalisation intense, tout en laissant une voie distincte, indépendante du calcium, pour soutenir un recyclage de fond plus discret.
Comment NSF tire les ficelles
Pour examiner de plus près le rôle de NSF au niveau du pore de fusion, les chercheurs ont construit un capteur fluorescent qui s’allume quand les protéines SNARE forment un faisceau et s’éteint quand ce faisceau est démonté. Lors de la stimulation, ils ont observé ces signaux apparaître là où les vésicules fusionnaient puis s’estomper en quelques secondes à mesure que le pore se refermait et que la vésicule était récupérée. Quand NSF était bloqué, le signal lumineux persistait beaucoup plus longtemps, indiquant que le faisceau SNARE restait assemblé au lieu d’être démonté. Avec des mesures de l’activité ATPase — l’action de combustion de carburant de NSF — ces résultats soutiennent l’idée que NSF désassemble activement les faisceaux SNARE à un stade tardif de la fusion. Ce démontage semble aider à resserrer et finalement à « pincer » le pore, accomplissant ainsi le cycle kiss‑and‑run. 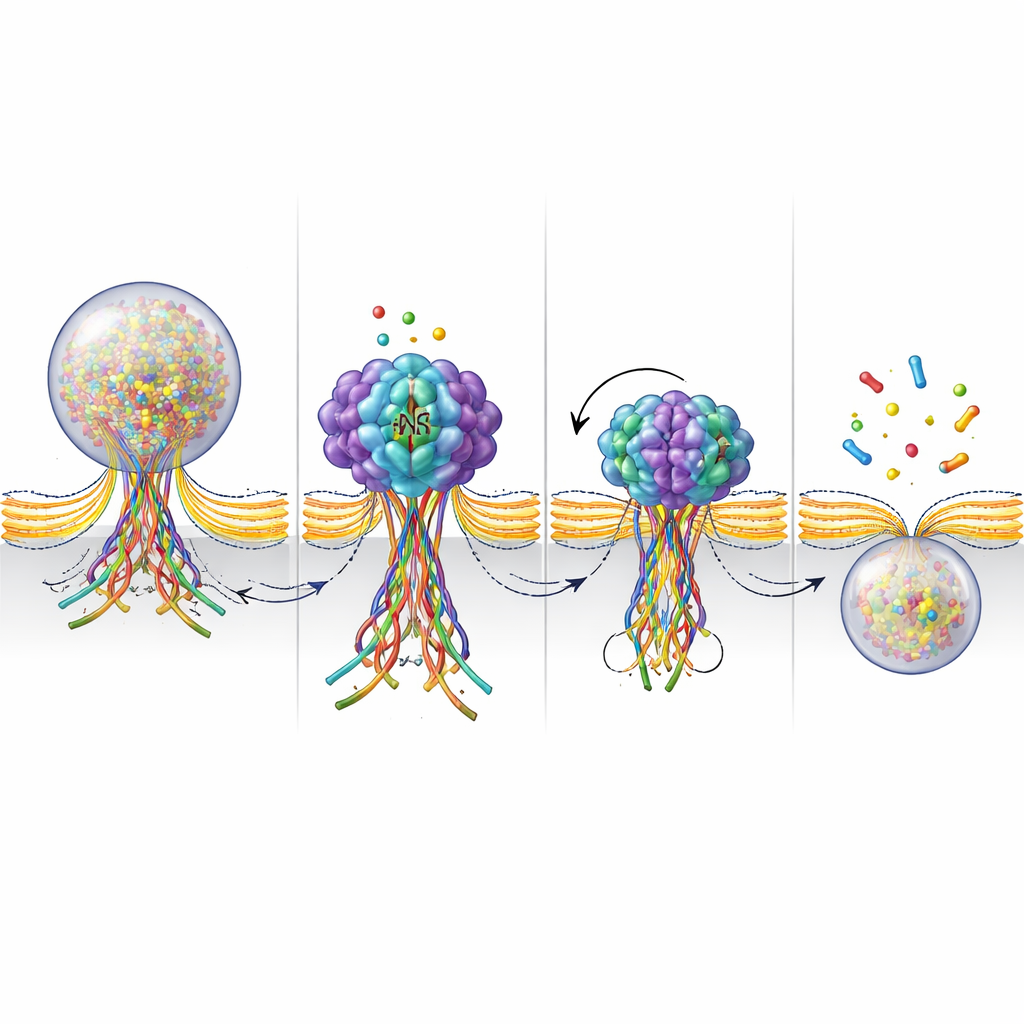
Pourquoi c’est important pour la santé et la maladie
En montrant que l’action énergétique de NSF est un commutateur central pour fermer le pore de fusion et déclencher le recyclage des vésicules, ce travail relie un moteur moléculaire bien connu au contrôle fin de la communication intercellulaire. Dans les cellules sécrétrices d’hormones, les cellules chromaffines de la médulla surrénale et certains neurones, ce mécanisme garantit que les vésicules peuvent être réutilisées rapidement et de manière fiable lors des surgissements de calcium. Si la fonction de NSF est perturbée, les pores peuvent ne pas se refermer correctement, le recyclage ralentit et les cellules peuvent avoir du mal à suivre la demande, contribuant potentiellement à des problèmes dans les réponses au stress, la transmission de la douleur ou la régulation de la glycémie. Comprendre cette étape de fermeture ouvre de nouvelles pistes pour explorer comment des défauts subtils du recyclage des vésicules pourraient sous‑tendre des troubles neurologiques et endocriniens, et met en lumière NSF comme une cible potentielle pour de futures stratégies thérapeutiques.
Citation: Wang, Y., Ma, S., Song, S. et al. ATPase N-ethylmaleimide-sensitive factor mediated calcium dependent fusion pore closure and endocytosis. Commun Biol 9, 495 (2026). https://doi.org/10.1038/s42003-026-09743-3
Mots-clés: recyclage des vésicules, pore de fusion, endocytose, signalisation calcique, ATPase NSF