Clear Sky Science · sv
ATPase N-ethylmaleimide-känsligt faktor medierad kalciumberoende fusionpor-stängning och endocytos
Hur celler återanvänder sina sekretpaket
Varje sekund släpper dina hjärnceller, hormonutsöndrande celler och immunceller ut små paket med kemiska budbärare och tar sedan snabbt in de tömda paketen för återanvändning. Detta snabba skepp-och-återvinn-system håller tänkande, blodsockerreglering och immunförsvar igång smidigt. Studien bakom denna artikel avslöjar en saknad pusselbit i den återvinningsprocessen: hur den lilla öppningen som släpper ut lasten – ”fusionporen” – vet när och hur den ska stängas så att det tomma paketet kan dras tillbaka in i cellen.
Livscykeln för ett sekretpaket
Många celler kommunicerar genom att fylla signalmolekyler som neurotransmittorer, hormoner eller inflammatoriska ämnen i bubliknande paket kallade vesiklar. Dessa vesiklar rör sig mot cellens yta och förenar sig kort med det yttre membranet, vilket bildar en liten vattenfylld kanal – fusionporen – genom vilken innehållet kan läcka ut. Ofta, istället för att helt smälta samman, utför vesikeln en ”kiss-and-run”: den vidrör ytan, öppnar en por precis tillräckligt länge för att släppa ut lasten, sedan stängs poren och vesikeln tas tillbaka för att användas igen. Denna snabba, ekonomiska cykel är mycket beroende av timing: öppnas fusionporen för kort blir för lite signal frigiven; misslyckas den att stängas stannar återvinningssystemet. 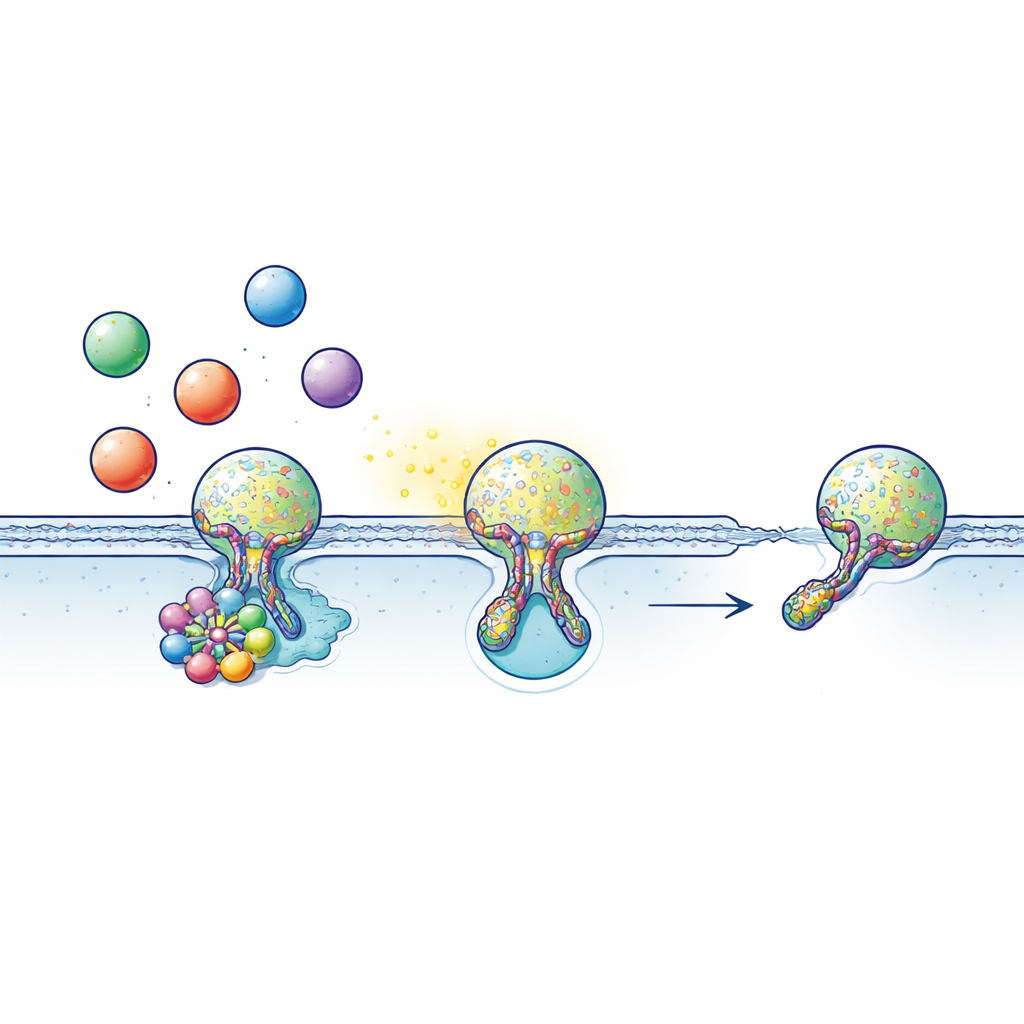
En molekylär motor vid poren
Vesikelfusion och återtagande drivs av proteiner som griper vesikeln och cellmembranet och drar dem samman som en dragsko. Dessa ”SNARE”-proteiner bildar täta buntar som för de två membranen i kontakt och öppnar fusionporen. Den nya studien fokuserar på ett annat protein, NSF, ett enzym som använder energi från ATP – cellens bränsle – för att ta isär SNARE-buntar efter att de gjort sitt jobb. Med elektriska inspelningar känsliga för förändringar i cellens yta tillsammans med levande konfokalavbildning såg författarna enskilda vesiklar fusa och tas tillbaka i råtters binjurehormonutsöndrande celler, sensoriska neuroner och insulinproducerande celler. Genom att kemiskt blockera NSF eller ta bort det genetiskt kunde de testa om dess aktivitet behövs inte bara före fusion utan också för att stänga poren i efterhand.
När NSF stannar upp vägrar porerna att stängas
Under normala förhållanden genomgår många vesiklar i dessa celler kiss-and-run: fusionporen öppnas, förblir öppen en kort, väl definierad tid och stängs sedan så att vesikeln kan dras in. När forskarna hämmade NSFs ATP-drivna aktivitet med läkemedel eller slog ut det såg de en iögonfallande beteendeförändring. Vesiklar nådde fortfarande membranet och porer kunde fortfarande öppnas, men en mycket mindre andel av händelserna fullbordade porstängningen. Istället tenderade vesiklar att förbli fästa vid ytan med porer som förblev öppna mycket längre än vanligt. Denna förändring gick hand i hand med en kraftig inbromsning eller blockering av flera former av endocytos, inklusive mycket snabb, långsammare och så kallad "overshoot"-återtagning där extra membran tas tillbaka. Poolen av vesiklar redo för snabb frisättning fylldes också på långsammare, vilket visar att porstängning och vesikelåtervinning är tätt sammankopplade steg.
Kalciumstyrda återvinningsval
Celler kan återvinna vesiklar på både kalciumberoende och kalciumoberoende sätt. I sensoriska neuroner i dorsalrotsgangliet jämförde teamet dessa två vägar. Med kalcium närvarande saktade blockering av NSF återhämtningen efter vesikelfusion åter ned, vilket visar att NSF är avgörande för kalciumutlöst återvinning. Men när forskarna använde ett stimuleringsmönster som framkallar ett kalciumfritt, spänningsdrivet återvinningsläge hade NSF-hämmare liten effekt. Denna kontrast tyder på att celler reserverar NSF som ett specialiserat verktyg för att hantera utbrott av kalciumdriven aktivitet, såsom de som uppstår under intensiv signalering, samtidigt som en separat, kalciumoberoende väg stödjer lugnare, bakgrundsåtervinning.
Hur NSF drar i trådarna
För att få en närmare bild av vad NSF gör vid fusionporen byggde forskarna en fluorescerande sensor som lyser när SNARE-proteiner bildar en bunt och avtar när den buntet dras isär. Under stimulering såg de dessa signaler dyka upp där vesiklar fusionerade och sedan blekna inom några sekunder när poren stängdes och vesikeln togs tillbaka. När NSF blockerades dröjde den lysande signalen kvar mycket längre, vilket indikerar att SNARE-bunten förblev sammansatt istället för att demonteras. Tillsammans med mätningar av ATPasaktivitet – NSFs bränsleförbrukande handling – stöder dessa resultat en bild där NSF aktivt demonterar SNARE-buntar i ett sent skede av fusionen. Den demonteringen tycks hjälpa till att dra åt och slutligen nypa av poren, vilket avslutar kiss-and-run-cykeln. 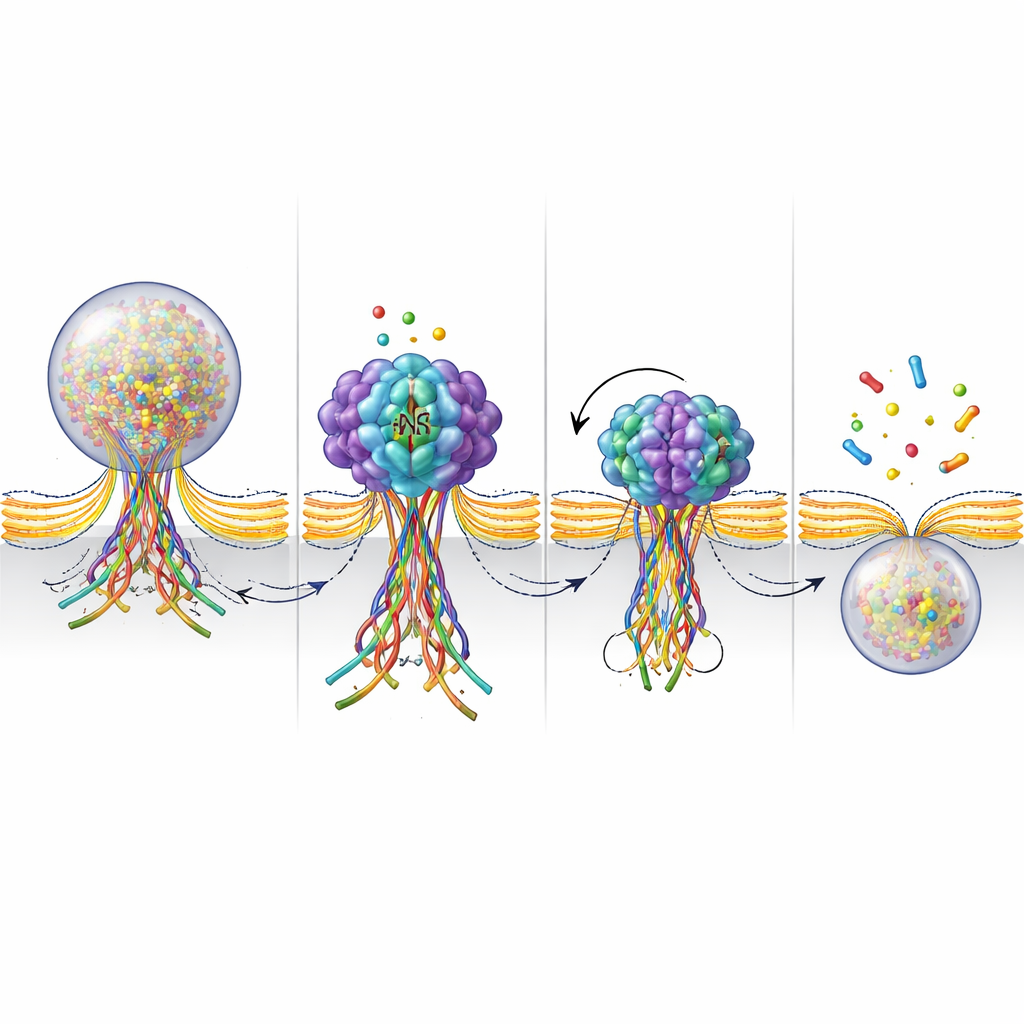
Varför detta är viktigt för hälsa och sjukdom
Genom att visa att NSFs energidrivna handling är en central brytare för att stänga fusionporen och utlösa vesikelåtervinning kopplar detta arbete en välkänd molekylär motor till finstyrningen av cell-till-cell-kommunikation. I hormonutsöndrande celler, binjurekromaffinceller och vissa neuroner säkerställer denna mekanism att vesiklar kan återanvändas snabbt och pålitligt vid kalciumtoppar. Om NSF-funktionen störs kan porer misslyckas med att stängas ordentligt, återvinningen saktar ner och celler kan få svårt att möta efterfrågan, vilket potentiellt bidrar till problem i stressrespons, smärtsignalering eller blodsockerreglering. Att förstå detta stängningssteg öppnar nya vägar för att undersöka hur subtila fel i vesikelåtervinning kan ligga bakom neurologiska och endokrina störningar, och lyfter fram NSF som ett potentiellt mål för framtida terapeutiska strategier.
Citering: Wang, Y., Ma, S., Song, S. et al. ATPase N-ethylmaleimide-sensitive factor mediated calcium dependent fusion pore closure and endocytosis. Commun Biol 9, 495 (2026). https://doi.org/10.1038/s42003-026-09743-3
Nyckelord: vesikelåtervinning, fusionpor, endocytos, kalciumsignalering, NSF ATPas