Clear Sky Science · ru
АТФаза NSF (N‑ethylmaleimide‑sensitive factor), опосредующая кальций‑зависимое закрытие места слияния и эндоцитоз
Как клетки повторно используют свои секреторные пакеты
Каждую секунду ваши клетки мозга, клетки, выделяющие гормоны, и клетки иммунной системы выпускают крошечные пакеты химических посредников, а затем быстро захватывают опустевшие пакеты обратно для повторного использования. Эта быстрая система «отправить‑и‑переработать» поддерживает работу мышления, регулирование уровня сахара в крови и иммунитет. Исследование, лежащее в основе этой статьи, выявляет недостающую звено в головоломке рециркуляции: как маленькое отверстие, через которое выходит груз — «место слияния» — узнает, когда и как закрыться, чтобы опустевший пакет можно было вернуть в клетку.
Жизненный цикл секреторного пакета
Многие клетки общаются, загружая сигналы, такие как нейромедиаторы, гормоны или воспалительные молекулы, в пузырьковые образования, называемые везикулами. Эти везикулы перемещаются к поверхности клетки и кратко сливаются с наружной мембраной, формируя крошечный заполненный водой туннель — место слияния — через который их содержимое выходит наружу. Часто, вместо полного слияния, везикула выполняет «поцелуй‑и‑побег»: она касается поверхности, открывает канал ровно настолько, чтобы выпустить груз, затем отверстие закрывается и везикула возвращается для повторного использования. Этот быстрый и экономный цикл критически зависит от точного тайминга: если место слияния открыто слишком мало — сигнал не успевает выйти; если не закрыть — система рециркуляции ломается. 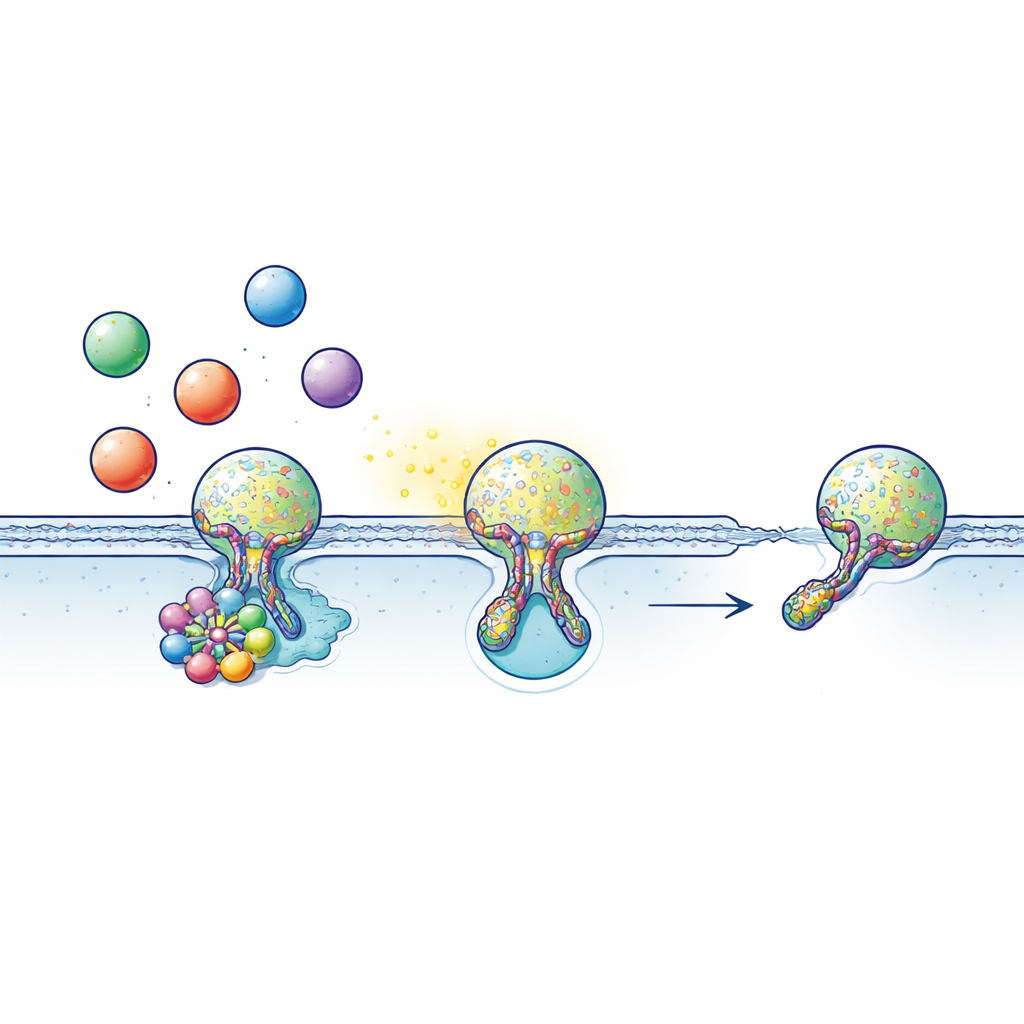
Молекулярный мотор у отверстия
Слияние везикул и их повторный захват обеспечиваются белками, которые захватывают везикулу и мембрану клетки и стягивают их вместе, как шнуровку. Эти белки «SNARE» образуют плотные пучки, сближающие две мембраны и открывающие место слияния. Новое исследование сосредоточено на другом белке — NSF, ферменте, который использует энергию АТФ — топливо клетки — чтобы разъединять пучки SNARE после того, как они выполнили свою функцию. Применяя электрические записи, чувствительные к изменениям площади поверхности клетки, в сочетании с живой конфокальной визуализацией, авторы наблюдали отдельные везикулы при слиянии и их возврате в адреналовые гормон‑секретирующие клетки крысы, сенсорные нейроны и инсунообразующие клетки. Химически блокируя NSF или удаляя его генетически, они проверяли, нужна ли его активность не только до слияния, но и для закрытия отверстия после него.
Когда NSF застревает, отверстия отказываются закрываться
При нормальных условиях многие везикулы в этих клетках проходят через поцелуй‑и‑побег: место слияния открывается, остается открытым в течение короткого, четко определенного времени, затем закрывается, и везикула может быть втянута обратно внутрь. Когда исследователи ингибировали АТФ‑зависимую активность NSF препаратами или удаляли его, они наблюдали поразительное изменение поведения. Везикулы по‑прежнему достигали мембраны и отверстия могли открываться, но гораздо меньшая доля событий завершалась закрытием отверстия. Вместо этого везикулы, как правило, оставались прикрепленными к поверхности с отверстиями, которые оставались открытыми значительно дольше обычного. Это изменение сопровождалось резким замедлением или блокированием нескольких видов эндоцитоза, включая очень быстрый, более медленный и «переразбор» (overshoot), при котором захватывается лишняя мембрана. Пул везикул, готовых к быстрому высвобождению, также пополнялся медленнее, что показывает: закрытие отверстия и рециркуляция везикул — тесно связанные этапы.
Кальцием управляемый выбор пути рециркуляции
Клетки могут рециркулировать везикулы как в кальций‑зависимом, так и в кальций‑независимом режимах. В сенсорных нейронах дорсального узла исследователи сравнили эти два пути. В присутствии кальция блокирование NSF снова замедляло возврат после слияния везикул, что указывает на необходимость NSF для кальций‑индуцированной рециркуляции. Но когда ученые использовали стимуляцию, вызывающую кальций‑независимый, напряжением‑зависимый режим рециркуляции, блокаторы NSF практически не влияли на процесс. Это различие предполагает, что клетки резервируют NSF как специализированный инструмент для обработки всплесков кальций‑зависимой активности, например при интенсивной передаче сигналов, в то время как отдельный кальций‑независимый путь поддерживает более тихую, фоновую рециркуляцию.
Как NSF дергает за ниточки
Чтобы получше рассмотреть, что делает NSF у места слияния, исследователи создали флуоресцентный сенсор, который светится, когда белки SNARE формируют пучок, и гаснет, когда этот пучок распускают. Во время стимуляции они видели появление этих сигналов там, где происходило слияние везикул, и их затухание в течение нескольких секунд по мере закрытия отверстия и возвращения везикулы. Когда NSF был заблокирован, светящийся сигнал задерживался значительно дольше, что указывает на то, что пучок SNARE оставался собранным вместо того, чтобы быть разобранным. В сочетании с измерениями АТФазной активности — «сжигания топлива» NSF — эти результаты поддерживают картину, в которой NSF активно разъединяет пучки SNARE на поздней стадии слияния. Это разъединение, по‑видимому, помогает затянуть и окончательно перекусить отверстие, завершив цикл поцелуй‑и‑побег. 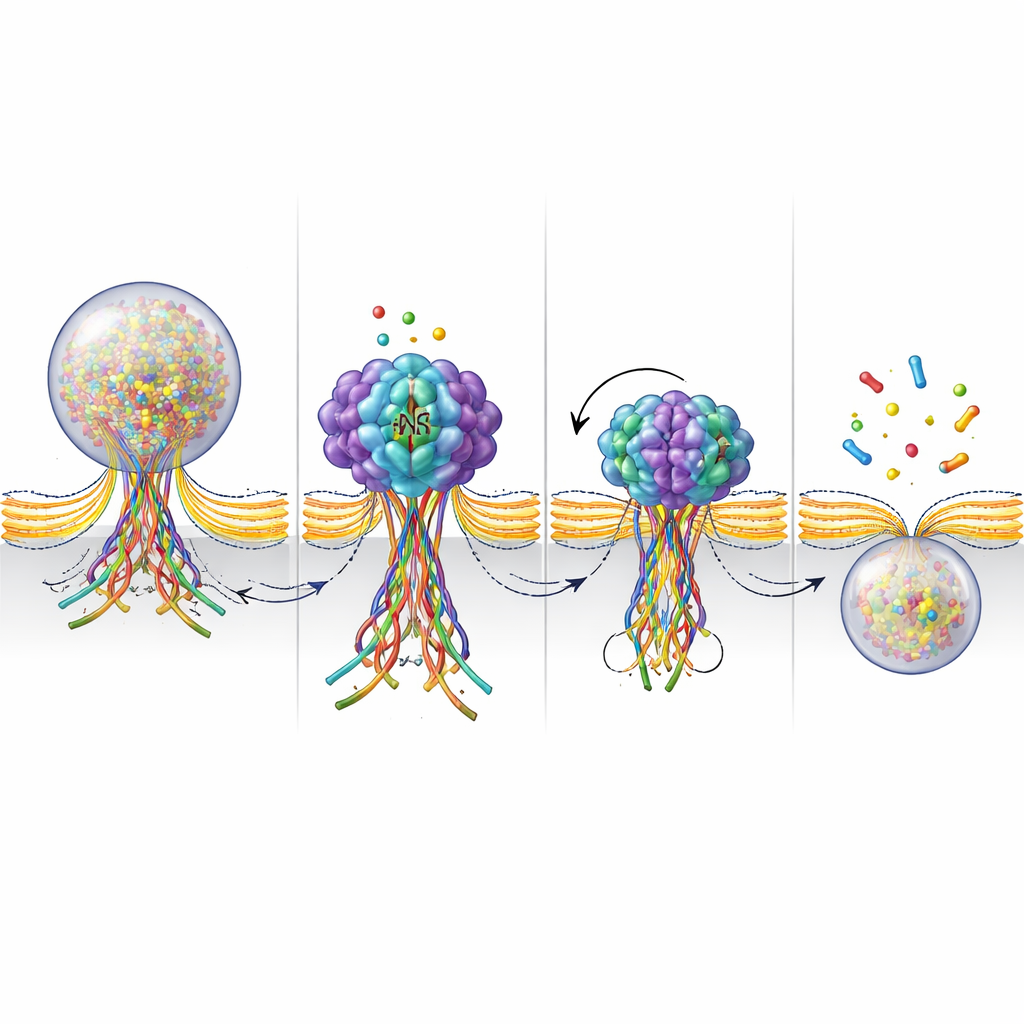
Почему это важно для здоровья и болезней
Показав, что энерго‑зависимое действие NSF является центральным переключателем для закрытия места слияния и запуска рециркуляции везикул, эта работа связывает хорошо известный молекулярный мотор с тонкой настройкой клеточной коммуникации. В гормон‑секретирующих клетках, адреналовых хромаффинных клетках и определенных нейронах этот механизм обеспечивает быстрое и надежное повторное использование везикул при всплесках кальция. Если функция NSF нарушена, отверстия могут не закрываться должным образом, рециркуляция замедляется, и клеткам становится сложнее справляться с нагрузкой, что потенциально может способствовать нарушениям в стресс‑ответах, передаче болевых сигналов или регуляции уровня глюкозы. Понимание этого этапа закрытия открывает новые пути для исследования того, как тонкие дефекты рециркуляции везикул могут лежать в основе неврологических и эндокринных расстройств, и выделяет NSF как потенциальную мишень для будущих терапевтических стратегий.
Цитирование: Wang, Y., Ma, S., Song, S. et al. ATPase N-ethylmaleimide-sensitive factor mediated calcium dependent fusion pore closure and endocytosis. Commun Biol 9, 495 (2026). https://doi.org/10.1038/s42003-026-09743-3
Ключевые слова: рециркуляция везикул, место слияния, эндоцитоз, кальциевая сигнализация, АТФаза NSF