Clear Sky Science · zh
使用下一代测序和定量蛋白质组学进行的泛癌种多组学 ERBB2-HER2 特征描绘
这对癌症患者为何重要
以 HER2 为靶点的抗癌药物已经改变了许多乳腺癌及其他类型癌症患者的治疗前景。然而,医生仍然难以准确预测哪些患者会从中受益。该研究表明,常规的基因检测和免疫染色检测可能错过真正依赖 HER2 相关信号通路的患者——同时也可能错误地将不太可能应答的患者判定为阳性。通过直接测量肿瘤中 HER2 及其伙伴 EGFR 的激活状态,研究者勾勒出一种更精确的方法来将患者与靶向疗法匹配。
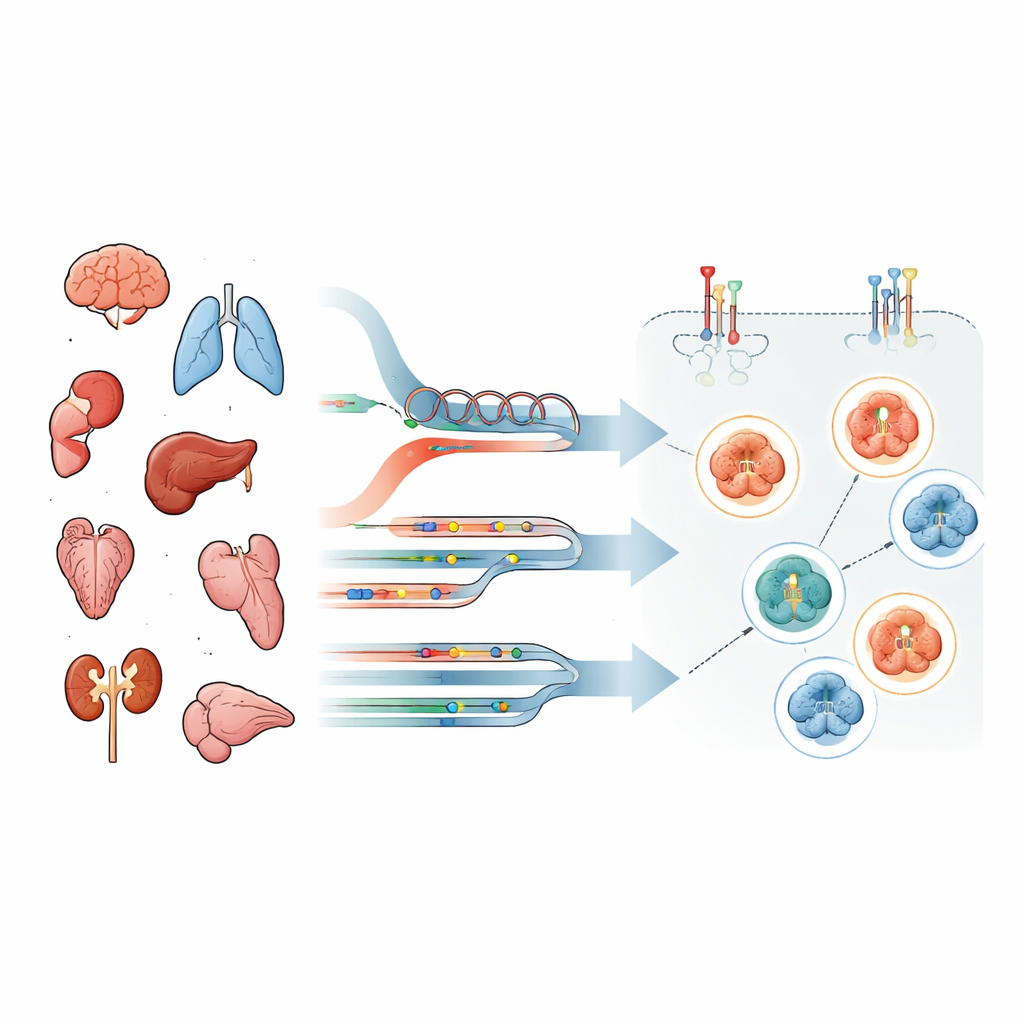
超越标准实验室检测
大多数医院判断肿瘤是否“HER2 阳性”依赖两种常规方法:一种是显微镜下的染色,显示细胞表面有多少 HER2 蛋白;另一种是检测 HER2 基因(即 ERBB2)是否有拷贝数增加或突变的 DNA 检测。这些方法侧重于未修饰的 HER2 的数量,而非其是否真正发出生长信号。但靶向药物并不完全相同:一些抗体–药物偶联物主要需要 HER2 作为结合位点,而酪氨酸激酶抑制剂则仅在 HER2/EGFR 信号开关真正被打开时才有效。因此,单看丰度可能会产生误导。
对肿瘤的多层次观测
为了解决这一问题,团队对 69 名不同类型晚期癌症患者(包括脑、肺和胃肠道肿瘤)的肿瘤进行了分层分析。从每位患者的样本中,他们使用临床下一代测序分析 DNA 和 RNA,并且关键是对激光显微切取的肿瘤细胞采用高度敏感的反相蛋白质芯片(reverse‑phase protein arrays)技术。这使得他们不仅能够定量总量的 HER2 蛋白,还能检测 HER2 和 EGFR 以及下游关键信号蛋白上的特定“开启”修饰——磷酸化标记。研究者根据肿瘤是否显示 HER2 基因改变、RNA 过表达、两者兼有或两者均无,将患者分组。
当基因与信号不一致时
结果显示基因水平的改变与实际通路活性之间存在显著不匹配。许多具有 HER2 或 EGFR 突变或基因拷贝数增加的患者,其 HER2 激活性(磷酸化)却很少或不存在。相反,一些在 DNA 或 RNA 水平没有可检测异常的患者,HER2 和 EGFR 却强烈激活,尤其在两个决定性位点上呈现出名为 HARPS 的签名。这类共同激活的肿瘤表现出明显的下游通路参与,驱动细胞生长与生存。例如在脑肿瘤中,超过一半的胶质母细胞瘤显示出这种激活签名,尽管缺乏经典的 HER2 DNA 改变,而脑膜瘤通常则不显示该特征。
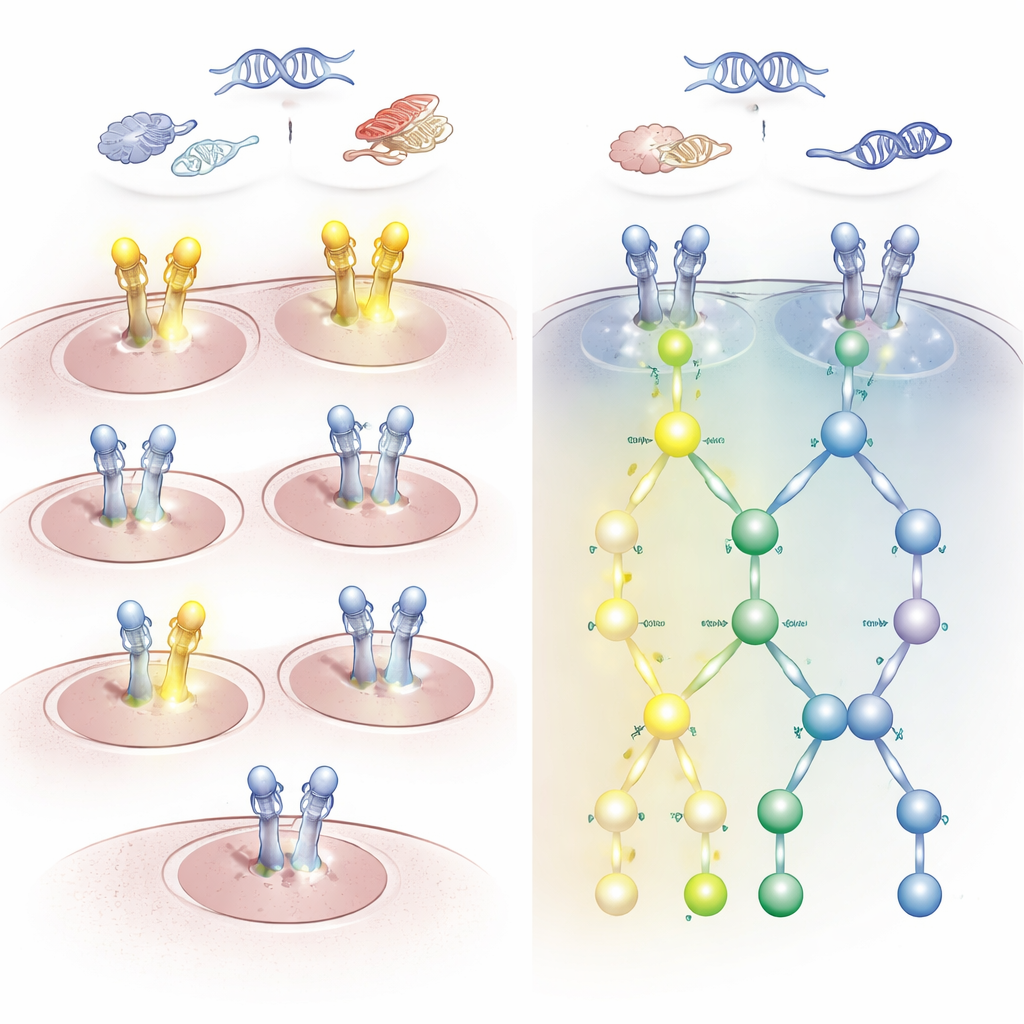
对选择合适药物的影响
这些差异不仅仅是学术上的。根据常规检测被判定为 HER2 阴性的某些患者,如果其信号通路被激活,仍可能对针对 HER2 或 EGFR 的药物产生应答。另一方面,通过染色或 DNA 检测看起来强阳性的患者实际上可能 HER2 信号处于静默状态,因而不太可能从这些治疗中获益。研究还指出,在某些病例中,其他驱动突变(如 KRAS 或 BRAF)与缺乏 HER2/EGFR 激活同时存在;这类患者可能更适合针对这些替代驱动因素的疗法,而非针对 HER2 的治疗。
迈向更智能的精准肿瘤学
作者得出结论:要真正实现 HER2 定向治疗的个体化,医生必须超越仅靠 DNA 测序和简单的蛋白丰度测定。对功能性蛋白活性的直接衡量——尤其是对 HER2 和 EGFR 的磷酸化检测——应当整合到精准肿瘤学的工作流程中。加入这一层信息后,临床医生可以更准确地识别出更可能从激酶抑制剂、抗体及抗体–药物偶联物中获益的患者。通俗地说,仅知道肿瘤中装有开关还不够;我们必须知道这个开关是否真正被打开。
引用: Hunt, A.L., Randall, J., Ogata, J.D. et al. Pan-cancer multi-omic ERBB2-HER2 characterization using next-generation sequencing and quantitative proteomics. npj Precis. Onc. 10, 153 (2026). https://doi.org/10.1038/s41698-026-01351-y
关键词: HER2, EGFR, 精准肿瘤学, 磷酸化蛋白质组学, 靶向疗法