Clear Sky Science · he
מיפוי ERBB2-HER2 רב-אומי בחצי-סרטן בעזרת רצף הדור הבא ופרוטאומיקה כמותית
למה זה חשוב לחולי סרטן
תרופות שמכוונות מולקולה בשם HER2 שינו את ניהול הטיפול עבור רבים החולים בסרטן השד ובממאירויות אחרות. ועדיין, רופאים נאבקים לחזות במדויק מי יפיק תועלת. המאמר מציג כי הבדיקות הגנטיות והצביעת מיקרוסקופ השגרתיות עלולות לפספס חולים שלגידולם אכן תלוי באיתות הקשור ל‑HER2 — ובמקביל לסמן בטעות אחרים שלא צפויים להגיב. על ידי מדידה ישירה של מידת ההפעלה של HER2 ובן־זוגו EGFR בתוך הגידולים, החוקרים מתארים דרך מדויקת יותר להתאים מטופלים לטיפולים ממוקדים.
מעבר לבדיקות מעבדה סטנדרטיות
ברוב בתי החולים קובעים האם גידול הוא "חיובי ל‑HER2" באמצעות שתי כלים שגרתיים: צביעת מיקרוסקופ שמראה כמה חלבון HER2 מצוי על פני התא, ובדיקות DNA שמאתרות העתקים נוספים או מוטציות של הגן HER2 (קרוי ERBB2). שיטות אלה מתמקדות בכמות ה‑HER2 הלא־ממוטבנת, לא בשאלה האם הוא פעיל ומשדר אותות גדילה. עם זאת, תרופות ממוקדות נחלקות למספר קבוצות: קונוגטים של אנטיבודי–סמים זקוקים בעיקר לכך ש‑HER2 יהיה נוכח כמשטח עגינה, בעוד מעכבי טירוזין קינאז פועלים רק אם מתג האיתות של HER2/EGFR באמת דלוק. כלומר, השפע בלבד עלול להטעות.
מבט רב‑שכבתי על הגידולים
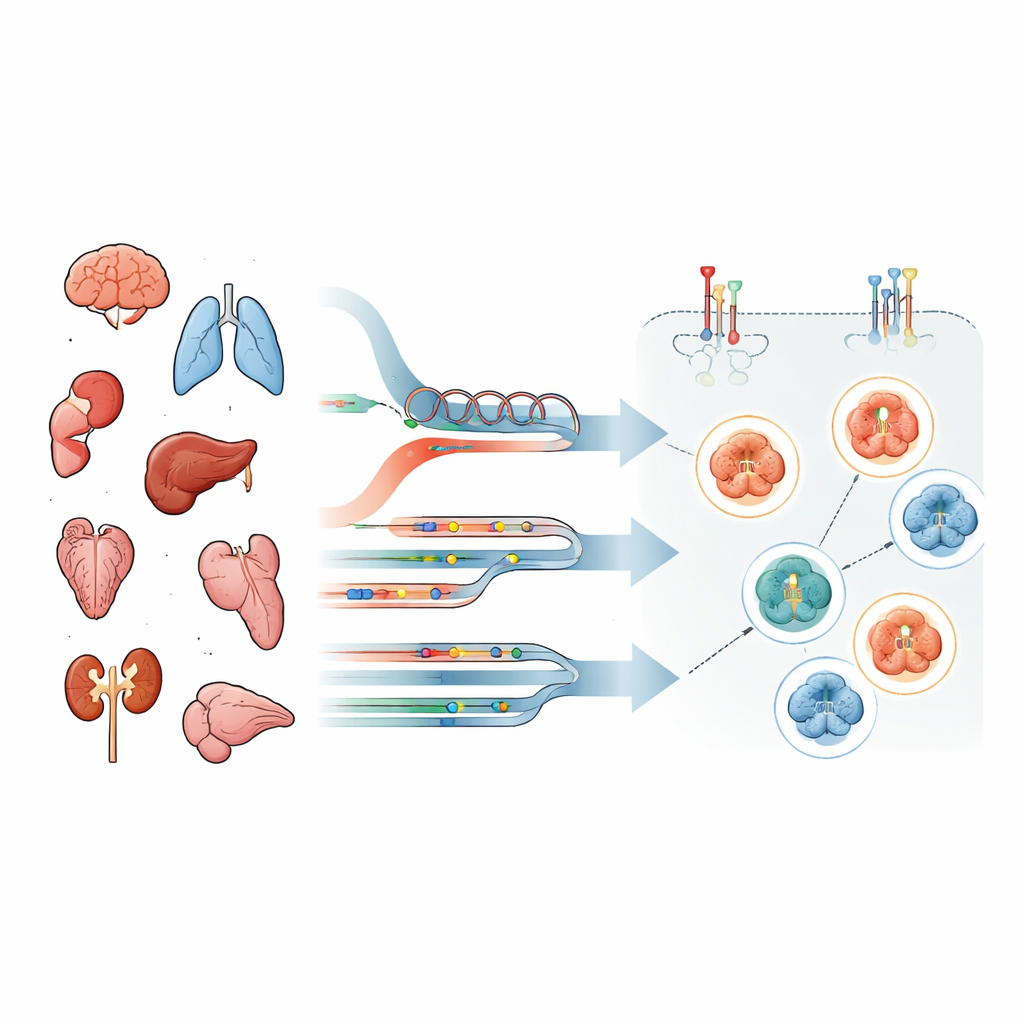
כדי להתמודד עם הבעיה, הצוות פרופילג גידולים מ‑69 חולים עם ממאירויות מתקדמות מסוגים שונים, כולל גידולי מוח, ריאה ומערכת העיכול. מכל מטופל ניתח הצוות DNA ו‑RNA ברצף קליני של הדור הבא ובנוסף — והחשוב מכך — השתמש בטכניקה רבת־רגישות שנקראת מערכי חלבון הפוכים (reverse‑phase protein arrays) על תאים מיקרו‑מנתחים בלייזר. זה איפשר לכמת לא רק את סה"כ חלבון HER2 אלא גם מודיפיקציות "דלק" ספציפיות — סימני פוספורילציה — על HER2 ו‑EGFR ועל חלבונים מרכזיים במורד הזרם. המטופלים סווגו לקבוצות בהתאם לשאלה האם בגידול נמצאו שינויים בגן HER2, ביטוי יתר של RNA, שניהם או לא־אף אחד מהם.
כשגנים ואיתותים לא מסכימים
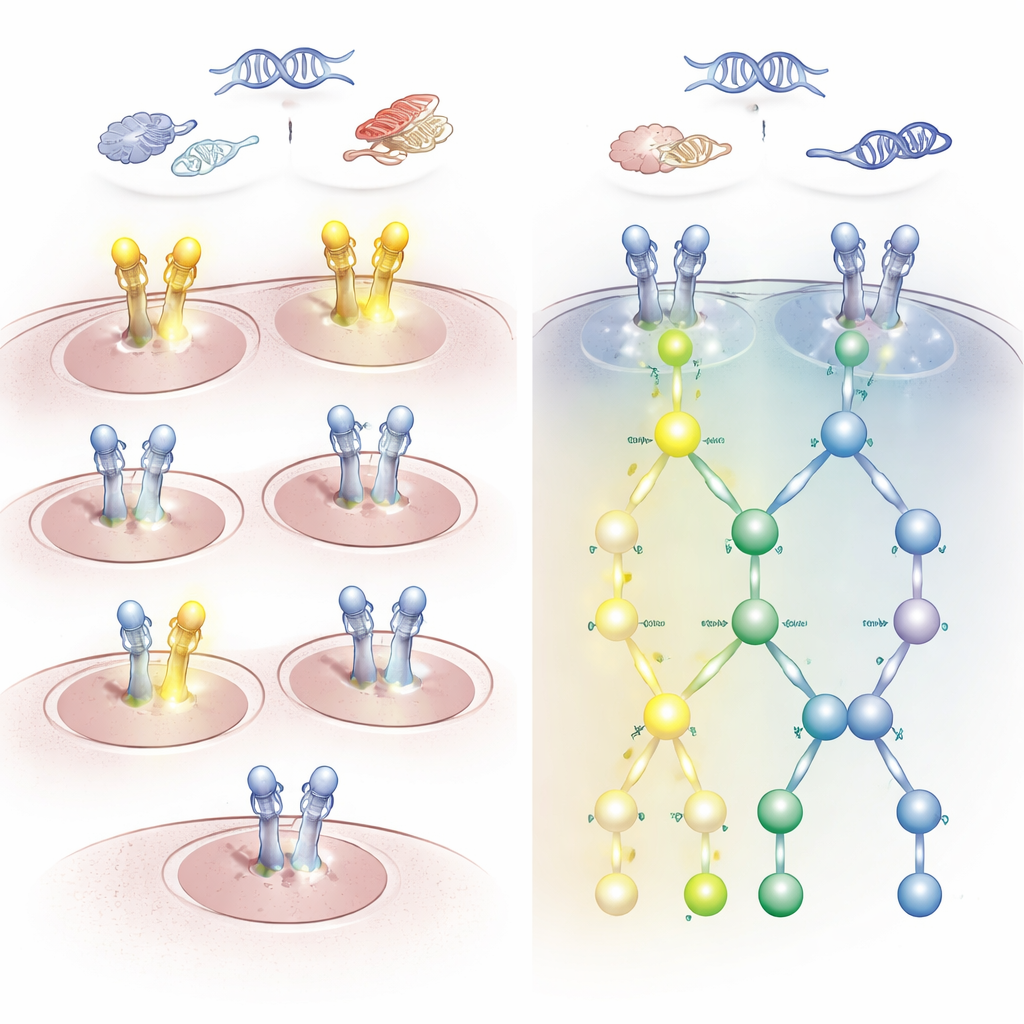
התוצאות חשפו חוסר התאמה בולט בין שינויים ברמה הגנטית לבין פעילות המסלול בפועל. מטופלים רבים עם מוטציות או העתקים נוספים של HER2 או EGFR הציגו מעט או לא הציגו פוספורילציה מפעילה על HER2. מנגד, אצל חלק מהחולים ללא אנומליות ניתנות לזיהוי בגן או ב‑RNA של HER2 נמצאה פעילות חזקה של HER2 ו‑EGFR, במיוחד בשני אתרים מרכזיים שמגדירים דפוס שנקרא חתימת HARPS. גידולים עם שפעול משותף זה הראו מעורבות ברורה של מסלולי מורד‑זרם שמניעים גדילה והישרדות תאית. לדוגמה, בגידולי מוח, יותר ממחצית הגליוובלסטומות הראו חתימה מופעלת זו למרות חוסר בשינויים גנומיים אופייניים של HER2, בעוד מנינגיומות בדרך כלל לא הראו זאת.
השלכות על בחירת התרופה הנכונה
הסתירות הללו אינן סתם עניין תאורטי. חלק מהמטופלים שאובחנו כשליליים ל‑HER2 בבדיקות הסטנדרטיות עשויים עדיין להגיב לתרופות המכוונות ל‑HER2 או ל‑EGFR אם מסלולי האיתות שלהם פעילים. אחרים שנראים חיוביים בצביעה או בבדיקות DNA עלולים למעשה להציג איתות שקט של HER2 ולכן צפויים להפיק תועלת מועטה מטיפולים כאלה. המחקר גם הדגיש מקרים שבהם מוטציות מניעות אחרות, כגון ב‑KRAS או BRAF, צפוים יחד עם חוסר פעילות של HER2/EGFR; מטופלים אלה צפויים כנראה להרוויח יותר מטיפולים שמכוונים לאותם דרייברים חלופיים מאשר ל‑HER2.
לקראת אונקולוגיה מדויקת חכמה יותר
המחברים מסכמים שעל מנת להתאים בצורה אמיתית טיפול מכוון ל‑HER2 יש להרחיב את מערכי האבחון מעבר לריצוף DNA ולכימות פשוט של כמות החלבון. מדידות ישירות של פעילות פונקציונלית של חלבונים — ובפרט פוספורילציה של HER2 ו‑EGFR — צריכות להשתלב בתהליכי האונקולוגיה המדויקת. על ידי הוספת שכבת מידע זו, קלינאים יוכלו לזהות ביתר דיוק מי צפוי להפיק תועלת ממעכבי קינאז, אנטיבודיות וקונוגטים של אנטיבודי–סמים שמכוונים למשפחת HER. במילים פשוטות, לא מספיק לדעת שהמתג מותקן בגידול; עלינו לדעת האם הוא אכן מופעל.
ציטוט: Hunt, A.L., Randall, J., Ogata, J.D. et al. Pan-cancer multi-omic ERBB2-HER2 characterization using next-generation sequencing and quantitative proteomics. npj Precis. Onc. 10, 153 (2026). https://doi.org/10.1038/s41698-026-01351-y
מילות מפתח: HER2, EGFR, אונקולוגיה מדויקת, פוספואומיקה, טיפול ממוקד