Clear Sky Science · pt
Caracterização pan‑câncer multiômica de ERBB2‑HER2 usando sequenciamento de nova geração e proteômica quantitativa
Por que isso importa para pacientes com câncer
Medicamentos contra o câncer que miram uma molécula chamada HER2 transformaram o tratamento de muitas pessoas com câncer de mama e outros tipos. Ainda assim, os médicos têm dificuldade em prever exatamente quem se beneficiará. Este estudo mostra que os testes genéticos e de coloração usuais podem deixar passar pacientes cujos tumores realmente dependem do sinal HER2 — e, ao mesmo tempo, identificar erroneamente outros que provavelmente não responderão. Ao medir diretamente como HER2 e seu parceiro EGFR estão ativados dentro dos tumores, os pesquisadores delineiam uma maneira mais precisa de combinar pacientes com terapias direcionadas.
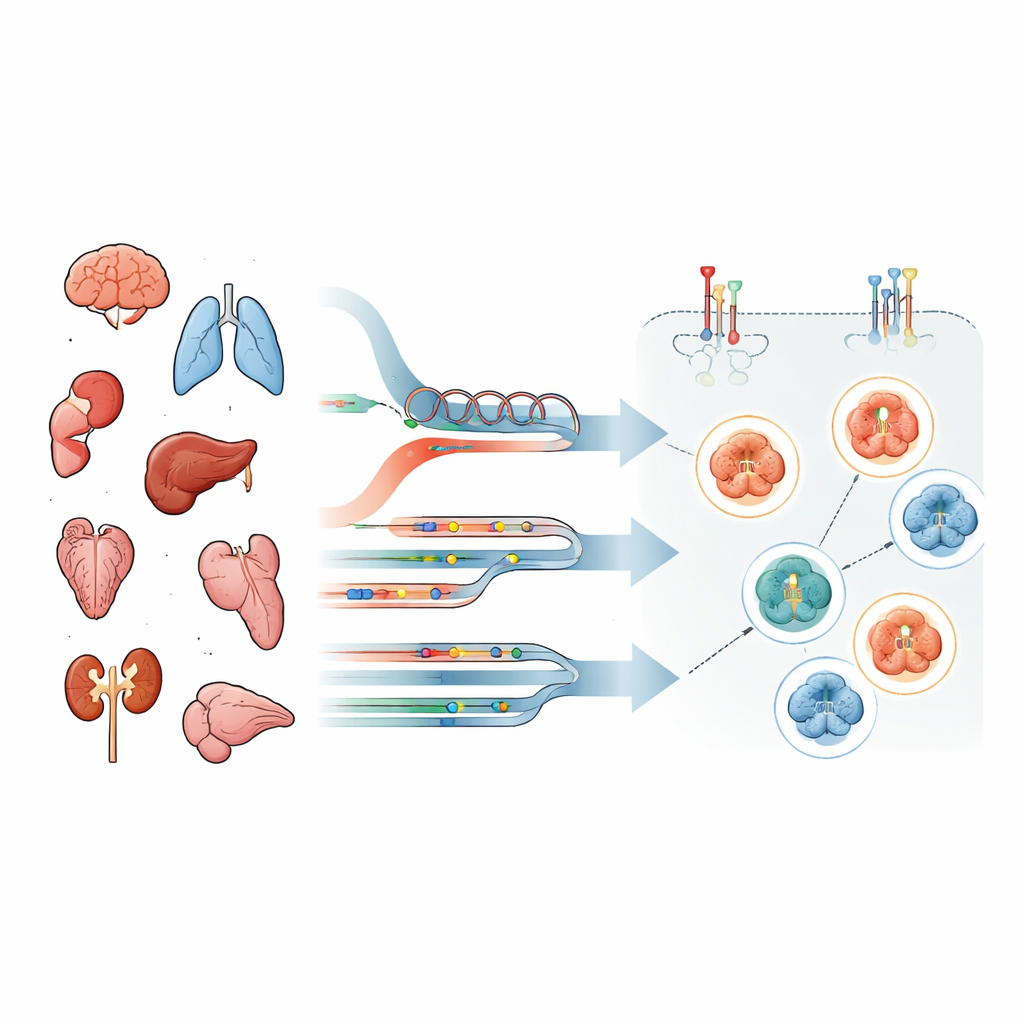
Olhando além dos testes laboratoriais padrão
A maioria dos hospitais determina se um tumor é “HER2‑positivo” usando duas ferramentas rotineiras: uma coloração ao microscópio que mostra quanto da proteína HER2 está na superfície celular e testes de DNA que detectam cópias extras ou mutações do gene HER2 (chamado ERBB2). Essas abordagens focam em quanto HER2 não modificado está presente, não em se ele está ativamente enviando sinais de crescimento. No entanto, os medicamentos direcionados pertencem a classes diferentes. Alguns conjugados anticorpo‑fármaco precisam principalmente que o HER2 esteja presente como um ponto de ancoragem, enquanto os inibidores de tirosina‑quinase funcionam apenas se o interruptor de sinalização HER2/EGFR estiver realmente ligado. Isso significa que a abundância por si só pode ser enganosa.
Uma visão em múltiplas camadas dos tumores
Para enfrentar esse problema, a equipe perfilou tumores de 69 pessoas com cânceres avançados de diversos tipos, incluindo tumores cerebrais, pulmonares e gastrointestinais. De cada paciente, analisaram DNA e RNA com sequenciamento clínico de nova geração e, de forma crucial, usaram uma técnica altamente sensível chamada matrizes de proteínas em fase reversa (reverse‑phase protein arrays) em células tumorais microdissecadas a laser. Isso lhes permitiu quantificar não apenas a proteína HER2 total, mas também modificações específicas de “ligado” — marcas de fosforilação — em HER2 e EGFR e em proteínas de sinalização chave a montante. Os pacientes foram classificados em grupos com base em se seus tumores apresentavam alterações no gene HER2, superexpressão de RNA, ambos ou nenhum dos dois.
Quando genes e sinais discordam
Os resultados revelaram uma discrepância marcante entre alterações ao nível dos genes e a real atividade da via. Muitos pacientes com mutações ou cópias extras de HER2 ou EGFR apresentaram pouca ou nenhuma fosforilação ativadora em HER2. Por outro lado, alguns pacientes sem anormalidades detectáveis no gene ou RNA de HER2 tinham HER2 e EGFR fortemente ativados, especialmente em dois sítios-chave que definem um padrão chamado assinatura HARPS. Tumores com essa coativação mostraram claro engajamento de vias a jusante que impulsionam o crescimento e a sobrevivência celular. Em tumores cerebrais, por exemplo, mais da metade dos glioblastomas exibiu essa assinatura ativada apesar de faltar alterações clássicas de DNA em HER2, enquanto os meningiomas, em geral, não mostraram.
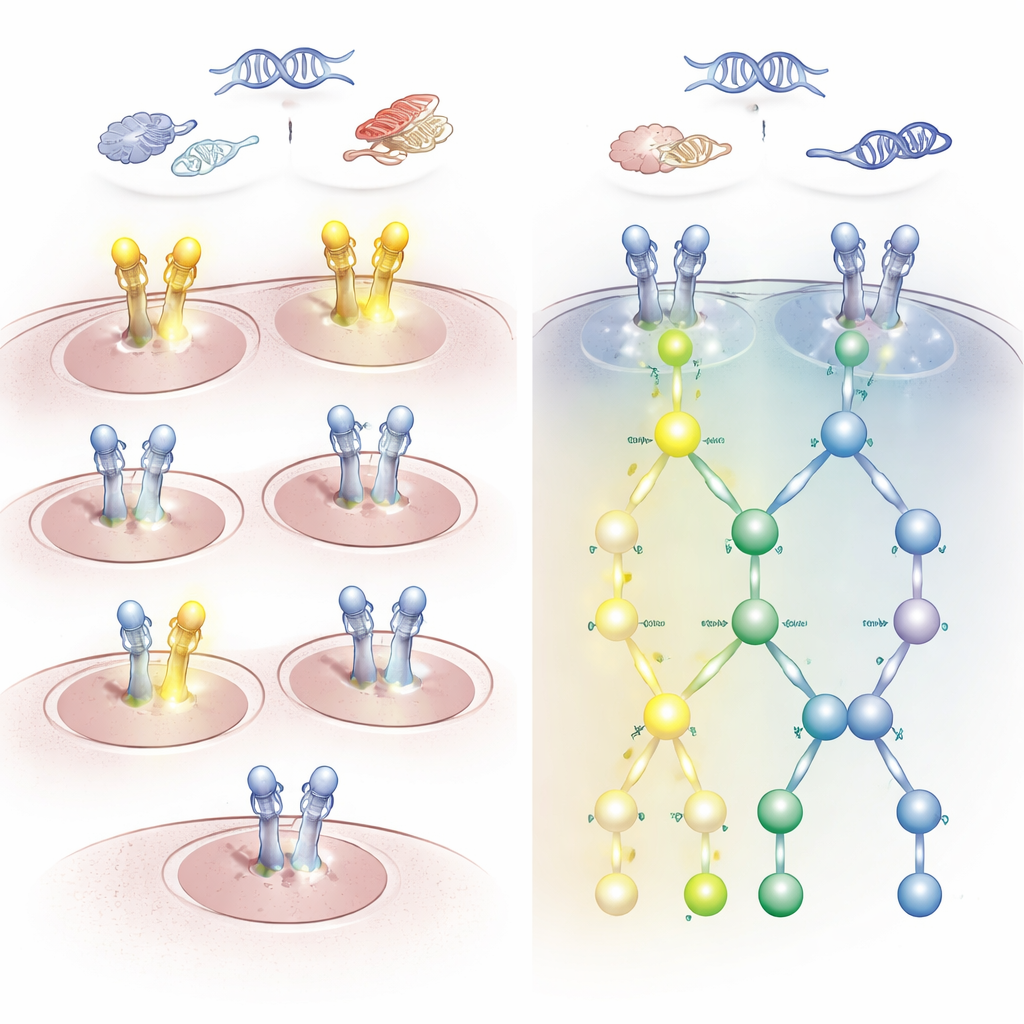
Implicações para a escolha do medicamento certo
Essas discrepâncias não são apenas questões acadêmicas. Alguns pacientes cujos tumores teriam sido rotulados como HER2‑negativos pelos testes padrão ainda podem responder a drogas direcionadas a HER2 ou EGFR se suas vias de sinalização estiverem ativadas. Outros que parecem fortemente positivos por coloração ou testes de DNA podem, na verdade, ter sinalização HER2 silenciosa e provavelmente não se beneficiarão desses tratamentos. O estudo também destacou casos em que outras mutações motoras, como em KRAS ou BRAF, coincidiram com ausência de ativação HER2/EGFR; esses pacientes provavelmente se beneficiariam mais de terapias direcionadas a esses motores alternativos do que a HER2.
Rumo a uma oncologia de precisão mais inteligente
Os autores concluem que, para realmente personalizar a terapia direcionada a HER2, os médicos devem ir além do sequenciamento de DNA e da simples abundância proteica. Medidas diretas da atividade funcional das proteínas — especialmente a fosforilação de HER2 e EGFR — devem ser integradas aos fluxos de trabalho da oncologia de precisão. Ao adicionar essa camada de informação, os clínicos podem identificar com mais precisão quem tem probabilidade de se beneficiar de inibidores de quinase, anticorpos e conjugados anticorpo‑fármaco que miram a família HER. Em termos práticos, não basta saber que o interruptor está instalado no tumor; é preciso saber se ele está realmente ligado.
Citação: Hunt, A.L., Randall, J., Ogata, J.D. et al. Pan-cancer multi-omic ERBB2-HER2 characterization using next-generation sequencing and quantitative proteomics. npj Precis. Onc. 10, 153 (2026). https://doi.org/10.1038/s41698-026-01351-y
Palavras-chave: HER2, EGFR, oncologia de precisão, fosfoproteômica, terapia direcionada