Clear Sky Science · pl
Pan‑nowotworowa wieloomiczna charakterystyka ERBB2‑HER2 przy użyciu sekwencjonowania następnej generacji i ilościowej proteomiki
Dlaczego to ma znaczenie dla pacjentów onkologicznych
Leki przeciwnowotworowe ukierunkowane na białko o nazwie HER2 zrewolucjonizowały leczenie wielu osób z rakiem piersi i innymi nowotworami. Mimo to lekarze wciąż mają trudności z przewidzeniem, kto dokładnie odniesie korzyść. Badanie to pokazuje, że standardowe testy genetyczne i barwienia mogą przeoczyć pacjentów, których guzy faktycznie zależą od sygnalizacji związanej z HER2 — i błędnie wskazać innych, którzy raczej nie zareagują. Poprzez bezpośrednie mierzenie, na ile HER2 i jego partner EGFR są aktywowane wewnątrz guzów, badacze przedstawiają bardziej precyzyjny sposób dopasowania pacjentów do terapii celowanych.
Patrząc poza standardowe testy laboratoryjne
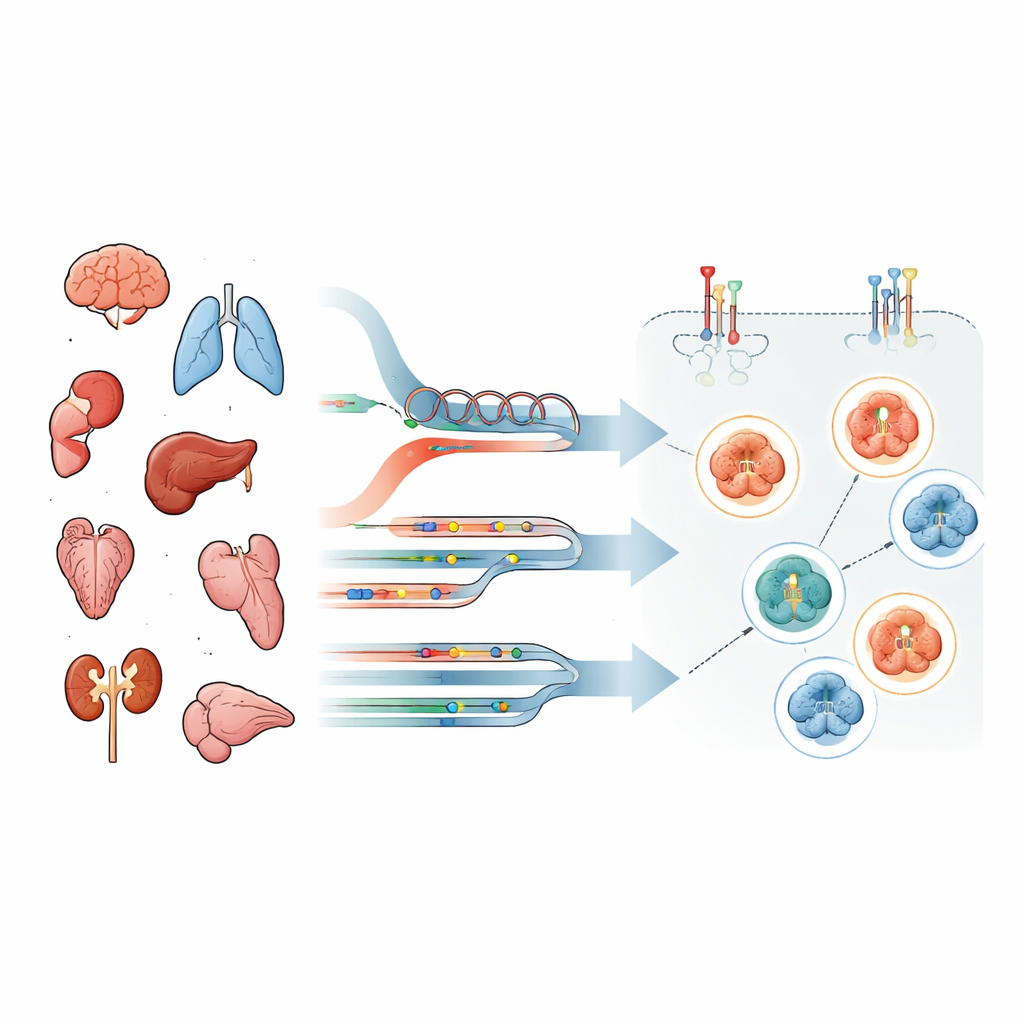
W większości szpitali status „HER2‑pozytywny” ocenia się przy użyciu dwóch rutynowych metod: barwienia mikroskopowego pokazującego, ile białka HER2 znajduje się na powierzchni komórki, oraz testów DNA wykrywających dodatkowe kopie lub mutacje genu HER2 (zwanego ERBB2). Te podejścia koncentrują się na ilości niezmodyfikowanego HER2, a nie na tym, czy aktywnie przekazuje sygnały wzrostu. Tymczasem leki celowane należą do różnych klas. Niektóre koniugaty przeciwciało‑lek wymagają głównie obecności HER2 jako „lądowiska”, podczas gdy inhibitory kinaz tyrozynowych działają tylko wtedy, gdy przełącznik sygnalizacyjny HER2/EGFR rzeczywiście jest włączony. Oznacza to, że sama obfitość może wprowadzać w błąd.
Wielo‑warstwowy widok guzów
Aby rozwiązać ten problem, zespół scharakteryzował guzy od 69 osób z zaawansowanymi nowotworami różnych typów, w tym mózgu, płuc i przewodu pokarmowego. Od każdego pacjenta analizowano DNA i RNA przy użyciu klinicznego sekwencjonowania następnej generacji i, co kluczowe, zastosowano wysoce czułą technikę zwaną odwrotną fazową macierzą białkową (reverse‑phase protein arrays) na laserowo mikrodysekowanych komórkach nowotworowych. Pozwoliło to na ilościowe określenie nie tylko całkowitej ilości białka HER2, ale także specyficznych modyfikacji „włączających” — znaków fosforylacji — na HER2 i EGFR oraz na kluczowych białkach sygnalizacyjnych w dół szlaku. Pacjentów podzielono na grupy w zależności od tego, czy ich guzy wykazywały zmiany w genie HER2, nadekspresję RNA, oba zjawiska, czy żadne z nich.
Kiedy geny i sygnały się nie zgadzają
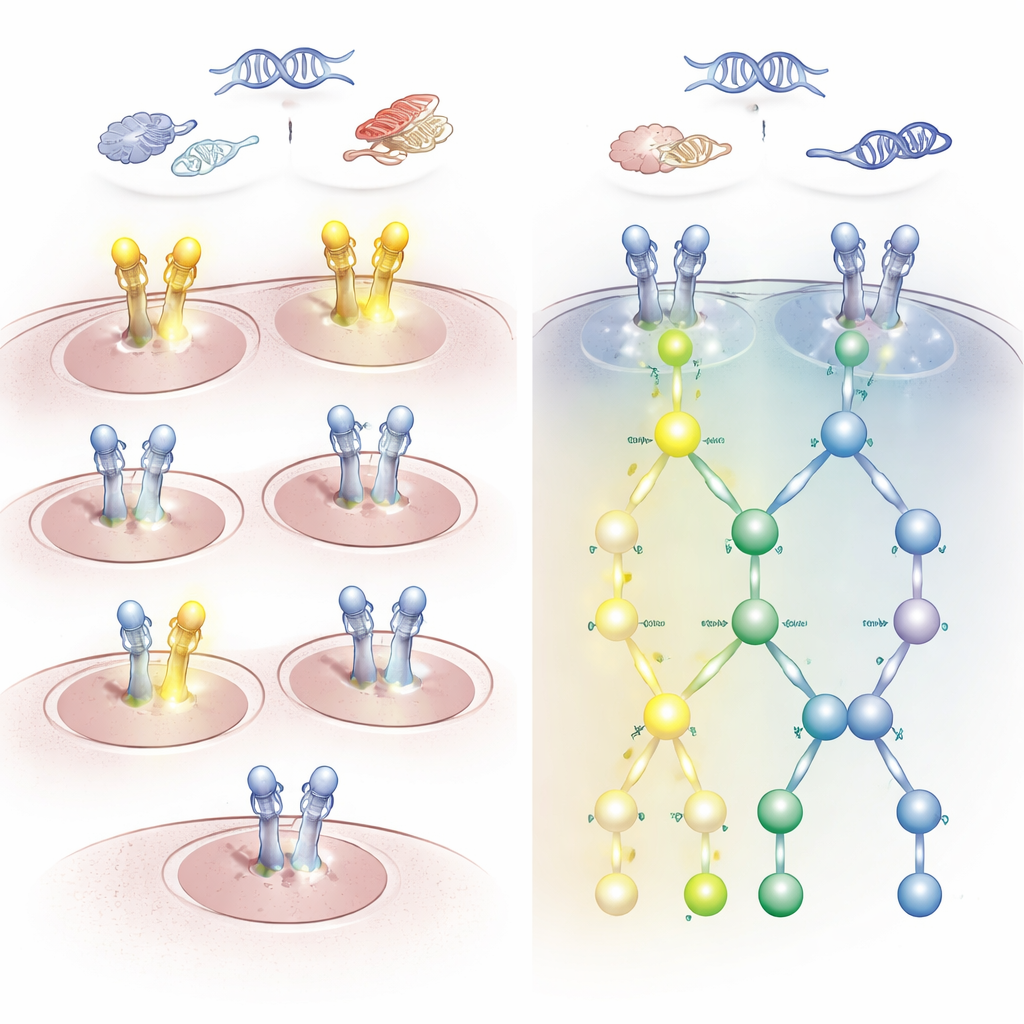
Wyniki ujawniły uderzającą rozbieżność między zmianami na poziomie genów a rzeczywistą aktywnością szlaku. Wielu pacjentów z mutacjami HER2 lub EGFR albo z dodatkowymi kopiami genu wykazywało niewiele lub brak aktywującej fosforylacji HER2. Odwrotnie — niektórzy pacjenci bez wykrywalnych nieprawidłowości w genie czy RNA HER2 mieli silnie aktywowany HER2 i EGFR, szczególnie w dwóch kluczowych miejscach definiujących wzorzec zwany sygnaturą HARPS. Guzy z tą współaktywacją wykazywały wyraźne zaangażowanie szlaków downstream napędzających wzrost i przeżycie komórek. W nowotworach mózgu, na przykład, ponad połowa glejaków wykazywała tę aktywowaną sygnaturę mimo braku klasycznych zmian DNA w HER2, podczas gdy oponiaki generalnie jej nie prezentowały.
Implikacje dla wyboru właściwego leku
Te rozbieżności nie są tylko akademicką ciekawostką. Niektórzy pacjenci, których guzy zostałyby oznaczone jako HER2‑negatywne przy standardowych testach, mogą jednak odpowiedzieć na leki ukierunkowane na HER2 lub EGFR, jeśli ich szlaki sygnalizacyjne są aktywne. Inni, którzy wyglądają na silnie pozytywnych w barwieniach lub testach DNA, mogą w rzeczywistości mieć uśpioną sygnalizację HER2 i prawdopodobnie nie skorzystają z takich terapii. Badanie wskazało też przypadki, w których inne mutacje napędowe, na przykład w KRAS lub BRAF, współwystępowały z brakiem aktywacji HER2/EGFR; tacy pacjenci prawdopodobnie lepiej skorzystają z terapii ukierunkowanych na te alternatywne cele niż na HER2.
W kierunku mądrzejszej precyzyjnej onkologii
Autorzy konkludują, że aby naprawdę spersonalizować terapię ukierunkowaną na HER2, lekarze muszą wyjść poza sekwencjonowanie DNA i prostą ocenę obfitości białka. Bezpośrednie pomiary funkcjonalnej aktywności białek — zwłaszcza fosforylacji HER2 i EGFR — powinny być zintegrowane z praktyką precyzyjnej onkologii. Dodając tę warstwę informacji, klinicyści mogą dokładniej identyfikować osoby, które prawdopodobnie skorzystają z inhibitorów kinaz, przeciwciał i koniugatów przeciwciało‑lek celujących w rodzinę HER. Mówiąc prościej: nie wystarczy wiedzieć, że przełącznik jest zainstalowany w guzie; musimy wiedzieć, czy jest on rzeczywiście włączony.
Cytowanie: Hunt, A.L., Randall, J., Ogata, J.D. et al. Pan-cancer multi-omic ERBB2-HER2 characterization using next-generation sequencing and quantitative proteomics. npj Precis. Onc. 10, 153 (2026). https://doi.org/10.1038/s41698-026-01351-y
Słowa kluczowe: HER2, EGFR, precyzyjna onkologia, fosfoproteomika, terapia celowana