Clear Sky Science · nl
Pan-cancer multi-omic ERBB2-HER2-characterisering met next-generation sequencing en kwantitatieve proteomica
Waarom dit ertoe doet voor kankerpatiënten
Kankergeneesmiddelen die zich richten op een molecuul genaamd HER2 hebben de behandeling van veel mensen met borstkanker en andere tumoren veranderd. Toch hebben artsen nog steeds moeite om precies te voorspellen wie er baat bij zal hebben. Deze studie toont aan dat de gebruikelijke genetische en kleuringstests patiënten kunnen missen waarvan de tumor werkelijk afhankelijk is van HER2-gerelateerde signalering — en ten onrechte anderen kunnen aanwijzen die waarschijnlijk niet reageren. Door direct te meten hoe HER2 en zijn partner EGFR in tumoren zijn geactiveerd, schetsen de onderzoekers een nauwkeuriger manier om patiënten aan gerichte therapieën te koppelen.
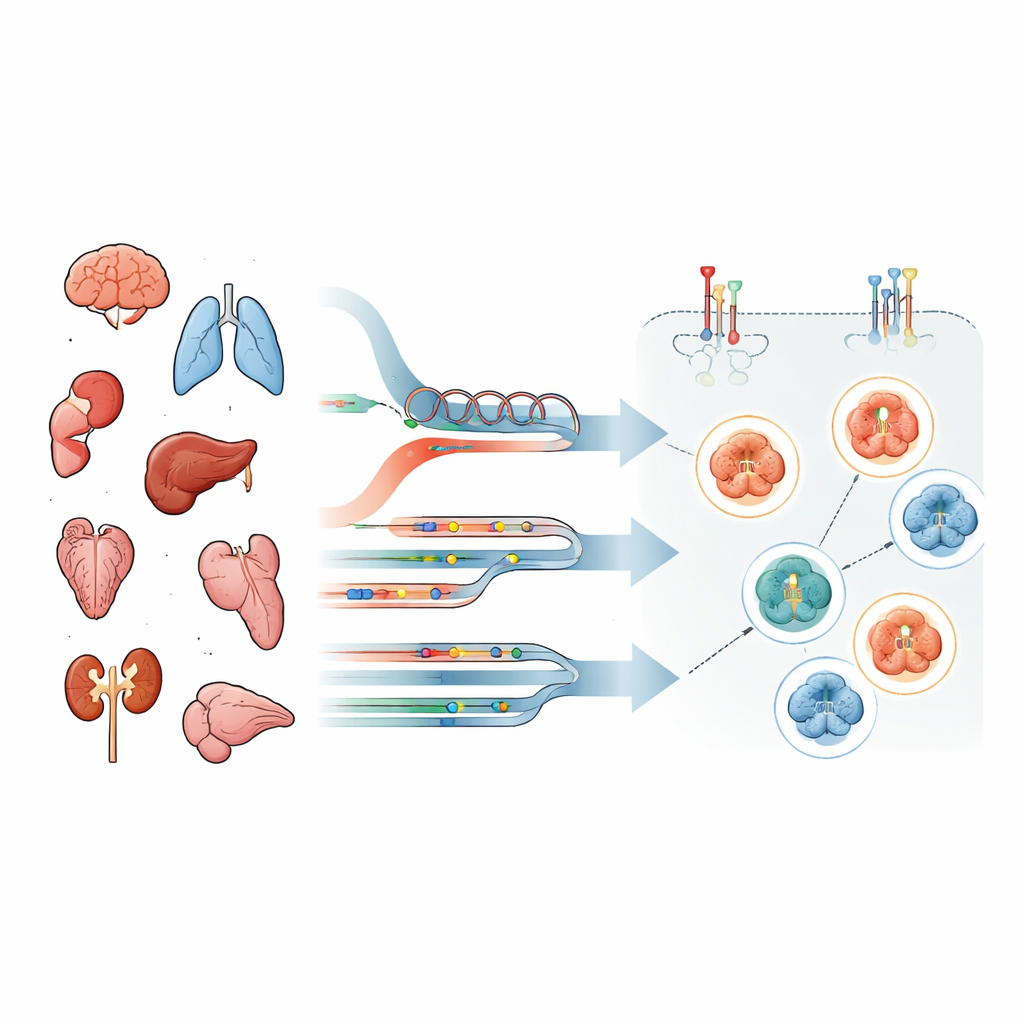
Voorbij standaardlaboratoriumtests kijken
De meeste ziekenhuizen bepalen of een tumor “HER2-positief” is met twee routinemethoden: een microscopische kleuring die laat zien hoeveel HER2-eiwit aan het celoppervlak aanwezig is, en DNA‑tests die extra kopieën of mutaties van het HER2-gen (ERBB2 genoemd) detecteren. Deze benaderingen richten zich op de hoeveelheid ongewijzigd HER2, niet op of het actief groeisignalen uitzendt. Gerichte medicijnen vallen echter in verschillende klassen. Sommige antilichaam–geneesmiddelconjugaten hebben vooral HER2 nodig als aanlegplaats, terwijl tyrosinekinaseremmers alleen werken als de HER2/EGFR‑signaalomschakeling daadwerkelijk is aangezet. Dat betekent dat louter abundantie misleidend kan zijn.
Een meerlagig beeld van tumoren
Om dit probleem aan te pakken, profuleerde het team tumoren van 69 mensen met gevorderde kankers van verschillende typen, waaronder hersen-, long- en gastro-intestinale tumoren. Van elke patiënt analyseerden ze DNA en RNA met klinische next‑generation sequencing en gebruikten ze, cruciaal, een zeer gevoelige techniek genaamd reverse-phase proteïne-arrays op laser‑microgedisseceerde tumorcellen. Hierdoor konden ze niet alleen totaal HER2-eiwit kwantificeren, maar ook specifieke ‘‘aan’’-modificaties — fosforyleringsmerken — op HER2 en EGFR en op belangrijke signaaleiwitten stroomafwaarts. Patiënten werden ingedeeld in groepen op basis van of hun tumoren HER2-genveranderingen, RNA-overexpressie, beide of geen van beide vertoonden.
Wanneer genen en signalen het oneens zijn
De resultaten lieten een opvallende discrepantie zien tussen veranderingen op genniveau en de daadwerkelijke activiteit van de route. Veel patiënten met HER2- of EGFR-mutaties of extra genkopieën toonden weinig of geen activerende fosforylering op HER2. Omgekeerd hadden sommige patiënten zonder detecteerbare HER2-gen- of RNA-afwijkingen sterk geactiveerde HER2 en EGFR, vooral op twee sleutelplaatsen die een patroon definiëren dat het HARPS‑handtekening wordt genoemd. Tumoren met deze co‑activatie vertoonden duidelijke betrokkenheid van downstream paden die celgroei en overleving aansturen. In hersenkankers, bijvoorbeeld, vertoonde meer dan de helft van de glioblastomen deze geactiveerde handtekening ondanks het ontbreken van klassieke HER2‑DNA‑alteraties, terwijl meningeomen over het algemeen niet zo waren.
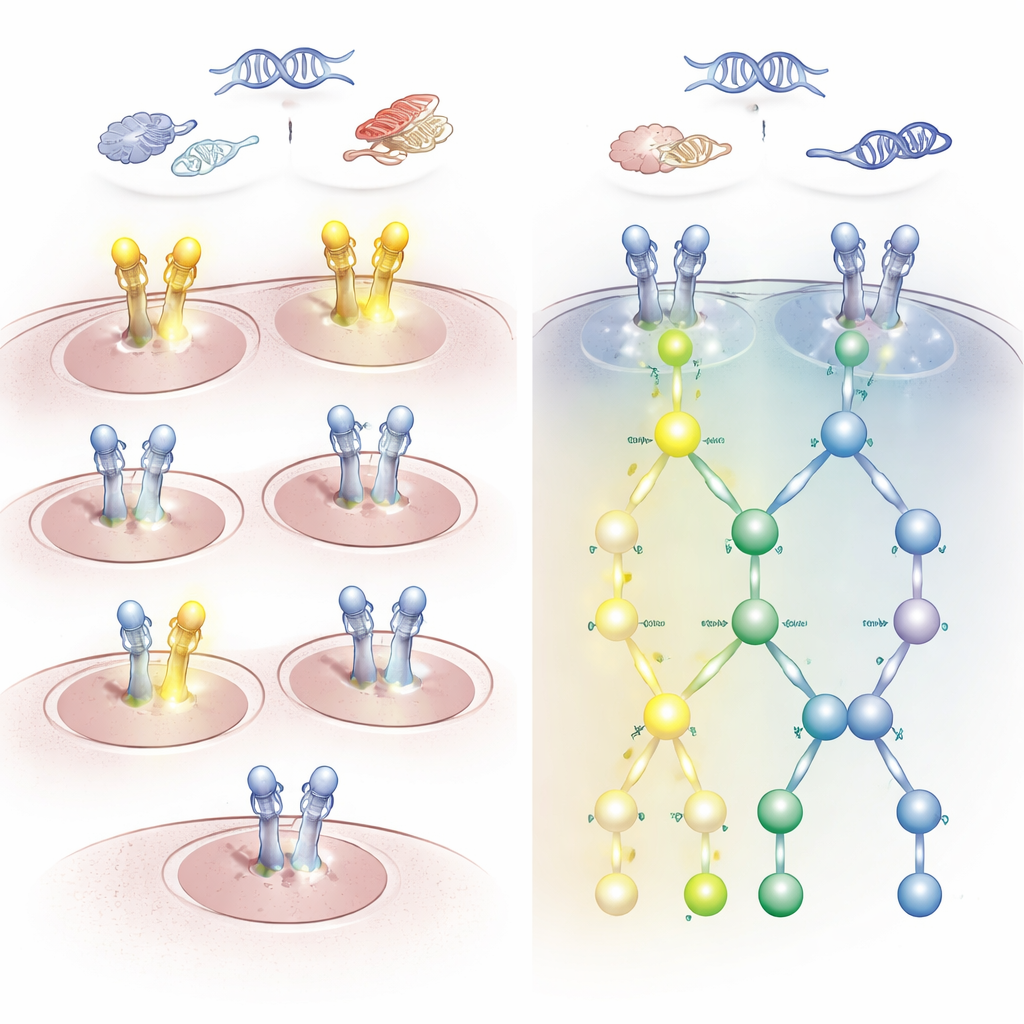
Gevolgen voor het kiezen van het juiste middel
Deze discrepanties zijn niet louter academisch. Sommige patiënten van wie de tumoren met standaardtests als HER2‑negatief zouden zijn bestempeld, zouden nog steeds kunnen reageren op HER2‑ of EGFR‑gerichte geneesmiddelen als hun signaalroutes geactiveerd zijn. Anderen die sterk positief lijken op basis van kleuring of DNA‑tests, kunnen in feite rustige HER2‑signalering hebben en waarschijnlijk geen baat hebben bij dergelijke behandelingen. De studie belichtte ook gevallen waarbij andere drijvende mutaties, zoals in KRAS of BRAF, samenvielen met het ontbreken van HER2/EGFR‑activatie; deze patiënten zouden waarschijnlijk beter worden behandeld met therapieën gericht op die alternatieve drijfveren in plaats van op HER2.
Naar slimmer precisiemedicine
De auteurs concluderen dat om HER2‑gerichte therapie werkelijk te personaliseren, artsen verder moeten kijken dan DNA‑sequencing en eenvoudige eiwithoeveelheid. Directe metingen van functionele eiwitactiviteit — vooral fosforylering van HER2 en EGFR — zouden moeten worden geïntegreerd in precisie‑oncologiewerkstromen. Door deze informatiefie laag toe te voegen, kunnen clinici nauwkeuriger bepalen wie waarschijnlijk baat heeft bij kinaseremmers, antilichamen en antilichaam–geneesmiddelconjugaten die zich richten op de HER‑familie. In alledaagse bewoordingen is het niet voldoende te weten dat de schakelaar in de tumor is geïnstalleerd; we moeten weten of hij daadwerkelijk is omgezet.
Bronvermelding: Hunt, A.L., Randall, J., Ogata, J.D. et al. Pan-cancer multi-omic ERBB2-HER2 characterization using next-generation sequencing and quantitative proteomics. npj Precis. Onc. 10, 153 (2026). https://doi.org/10.1038/s41698-026-01351-y
Trefwoorden: HER2, EGFR, precisie-oncologie, fosfoproteomica, gerichte therapie