Clear Sky Science · ru
Мультиомная пан‑раковая характеристика ERBB2‑HER2 с использованием секвенирования следующего поколения и количественной протеомики
Почему это важно для пациентов с раком
Препараты, нацеленные на молекулу HER2, изменили подход к лечению многих людей с раком молочной железы и другими опухолями. Тем не менее врачам по‑прежнему сложно точно предсказать, кто именно получит от этого пользу. В этом исследовании показано, что привычные генетические и окрашивающие тесты могут пропускать пациентов, чьи опухоли действительно зависят от сигнализации, связанной с HER2, и ошибочно отмечать других, которые вряд ли ответят на лечение. Прямое измерение того, насколько HER2 и его партнер EGFR активированы внутри опухолей, позволяет исследователям предложить более точный способ подбора таргетных препаратов.
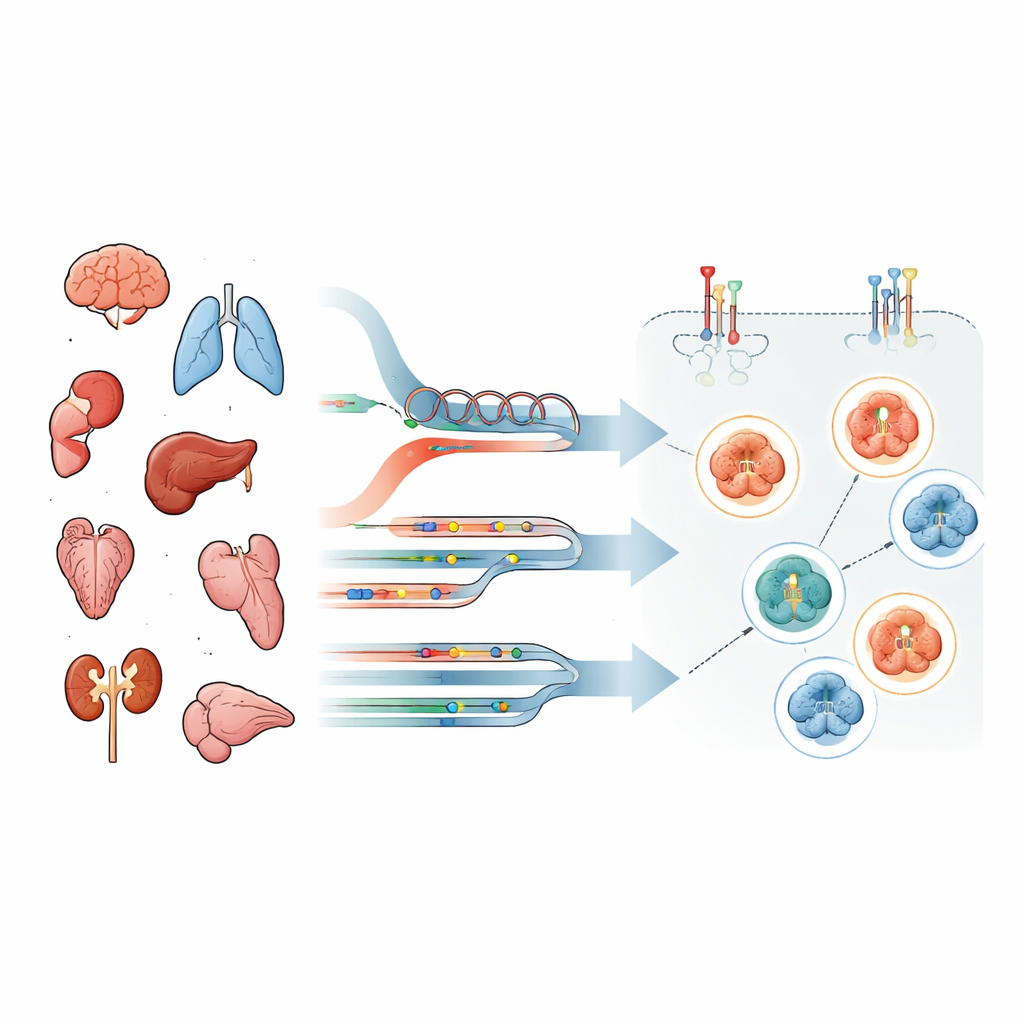
Смотреть дальше стандартных лабораторных тестов
В большинстве больниц статус «HER2‑положительной» определяют двумя обычными методами: окрашиванием под микроскопом, показывающим, сколько белка HER2 находится на поверхности клетки, и ДНК‑тестами, выявляющими дополнительные копии или мутации гена HER2 (ERBB2). Эти подходы оценивают количество немодифицированного HER2, но не указывают, активно ли он посылает сигналы роста. Между тем таргетные препараты различаются по механизму действия. Некоторые конъюгаты антител с лекарственным веществом в основном требуют присутствия HER2 в качестве «посадочной площадки», тогда как ингибиторы тирозинкиназы действуют только если переключатель сигнального пути HER2/EGFR действительно включён. Поэтому одной только экспрессии белка может быть недостаточно.
Многослойный взгляд на опухоли
Чтобы решить эту проблему, команда профилировала опухоли у 69 пациентов с прогрессирующими опухолями разных типов, включая опухоли головного мозга, лёгких и желудочно‑кишечного тракта. У каждого пациента проанализировали ДНК и РНК с помощью клинического секвенирования следующего поколения и, что важно, применили высокочувствительную методику reverse‑phase protein arrays к лазерно‑микродиссектированным опухолевым клеткам. Это позволило количественно оценить не только общий белок HER2, но и специфические «включающие» модификации — фосфорилирования — на HER2 и EGFR, а также на ключевых сигнальных белках вниз по каскаду. Пациентов разделили на группы в зависимости от того, имели ли их опухоли изменения гена HER2, избыточную экспрессию РНК, оба признака или ни одного из них.
Когда гены и сигналы расходятся
Результаты выявили заметное несоответствие между генетическими изменениями и реальной активностью пути. У многих пациентов с мутациями HER2 или EGFR либо дополнительными копиями гена отмечалось мало или вовсе не было активирующих фосфорилирований HER2. Напротив, у некоторых пациентов без выявленных генетических или РНК‑аномалий HER2 наблюдалась сильная активация HER2 и EGFR, особенно в двух ключевых сайтах, которые формируют паттерн, называемый HARPS‑сигнатурой. Опухоли с этой ко‑активацией демонстрировали явное вовлечение низлежащих путей, отвечающих за рост и выживание клеток. Например, в опухолях головного мозга более половины глиобластом показывали эту активированную сигнатуру, несмотря на отсутствие классических ДНК‑изменений HER2, тогда как менингиомы в целом таковой не обладали.
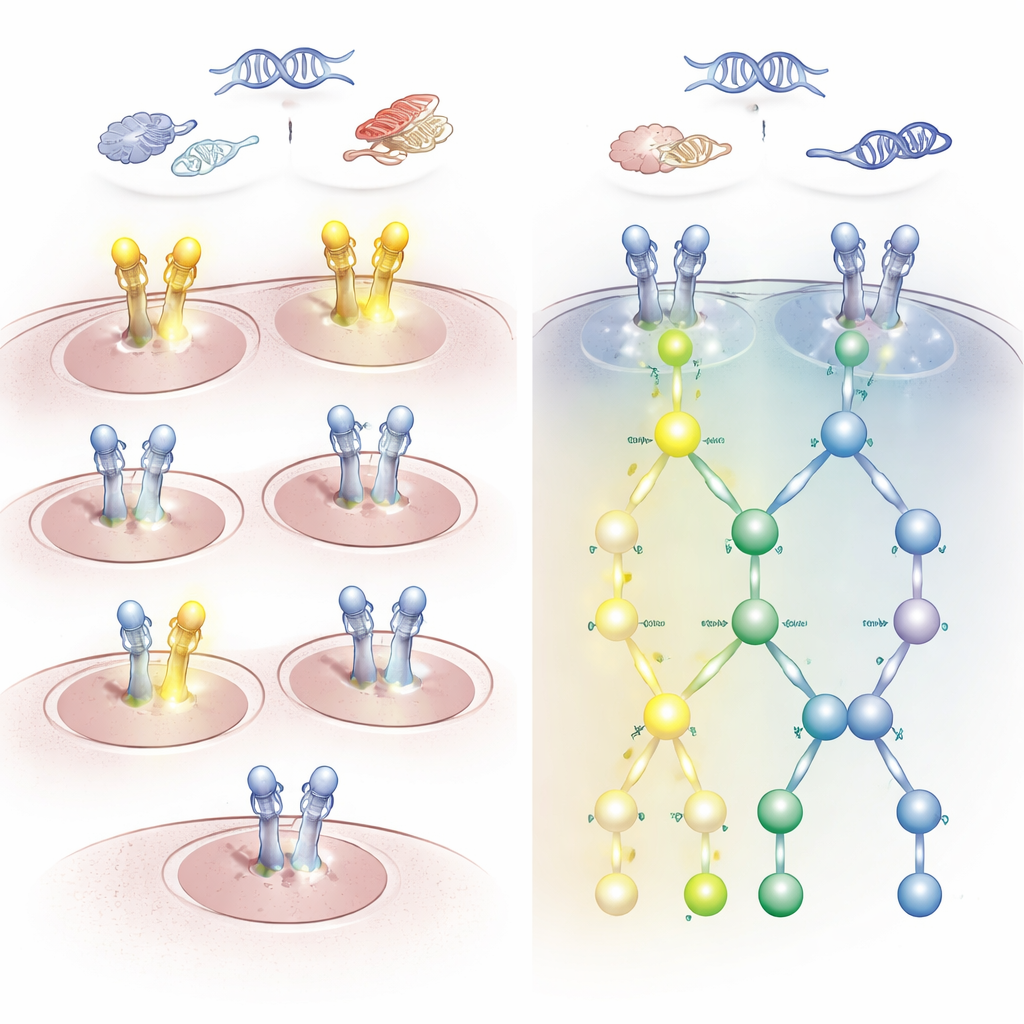
Последствия для выбора правильного лекарства
Эти расхождения имеют практическое значение. Некоторые пациенты, чьи опухоли по стандартным тестам были бы отнесены к HER2‑отрицательным, тем не менее могут ответить на препараты, нацеленные на HER2 или EGFR, если их сигнальные пути активированы. Другие же, выглядящие сильно позитивными по окрашиванию или ДНК‑тестам, фактически могут иметь тихую сигнализацию HER2 и вряд ли извлекут пользу из такой терапии. В исследовании также отмечены случаи, когда другие драйверные мутации, например в KRAS или BRAF, сопровождались отсутствием активации HER2/EGFR; таким пациентам, вероятно, больше подойдут терапии, направленные на эти альтернативные драйверы, а не на HER2.
К более умной прецизионной онкологии
Авторы приходят к выводу, что для реальной персонализации терапии, направленной против HER2, врачам необходимо выходить за пределы секвенирования ДНК и простой оценки количества белка. Прямые измерения функциональной активности белков — в первую очередь фосфорилирования HER2 и EGFR — следует интегрировать в рабочие процессы прецизионной онкологии. Добавив этот уровень информации, клиницисты смогут точнее определять, кто с наибольшей вероятностью выиграет от ингибиторов киназ, антител и конъюгатов антител с лекарственными средствами, нацеленных на семью HER. Проще говоря, важно не только знать, что переключатель установлен в опухоли; нужно знать, включён он или нет.
Цитирование: Hunt, A.L., Randall, J., Ogata, J.D. et al. Pan-cancer multi-omic ERBB2-HER2 characterization using next-generation sequencing and quantitative proteomics. npj Precis. Onc. 10, 153 (2026). https://doi.org/10.1038/s41698-026-01351-y
Ключевые слова: HER2, EGFR, онкологическая прецизионная медицина, фосфопротеомика, таргетная терапия