Clear Sky Science · fr
Caractérisation pan‑cancer multi‑omique d’ERBB2‑HER2 par séquençage de nouvelle génération et protéomique quantitative
Pourquoi cela compte pour les patients atteints de cancer
Les médicaments anticancéreux ciblant une molécule appelée HER2 ont transformé le traitement de nombreux patients atteints de cancers du sein et d’autres types de tumeurs. Pourtant, les médecins peinent encore à prédire précisément qui en bénéficiera. Cette étude montre que les tests génétiques et les colorations habituels peuvent manquer des patients dont les tumeurs dépendent réellement du signalement lié à HER2 — et, inversement, identifier à tort des patients peu susceptibles de répondre. En mesurant directement l’état d’activation de HER2 et de son partenaire EGFR au sein des tumeurs, les chercheurs proposent une méthode plus précise pour associer les patients aux thérapies ciblées.
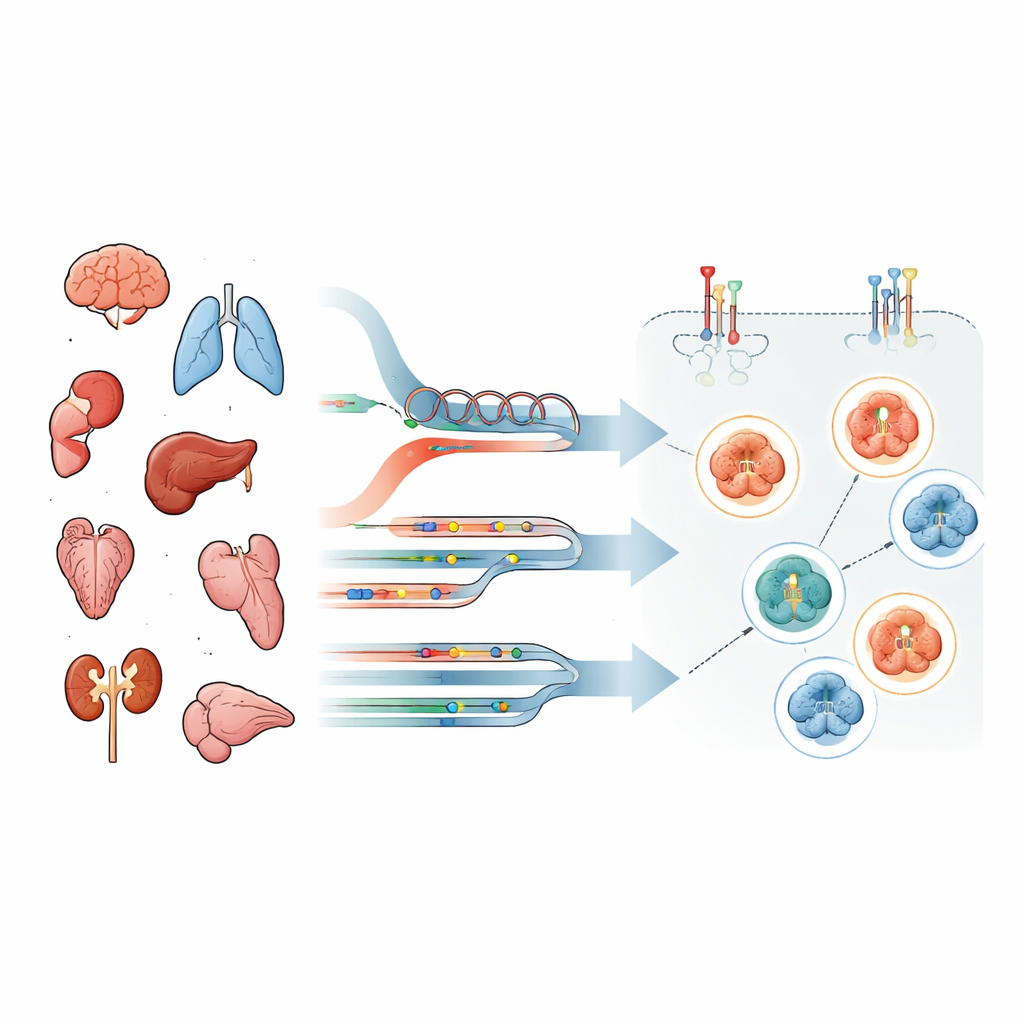
Au‑delà des tests de laboratoire standards
La plupart des hôpitaux déterminent si une tumeur est « HER2‑positive » à l’aide de deux outils de routine : une coloration au microscope qui montre la quantité de protéine HER2 à la surface cellulaire, et des tests ADN qui détectent des copies supplémentaires ou des mutations du gène HER2 (appelé ERBB2). Ces approches se concentrent sur la quantité d’HER2 non modifié présente, et non sur son état d’activation. Or, les médicaments ciblés appartiennent à différentes classes. Certains conjugués anticorps‑médicament requièrent principalement la présence d’HER2 comme point d’attache, tandis que les inhibiteurs de tyrosine kinase ne fonctionnent que si l’interrupteur HER2/EGFR est réellement enclenché. Autrement dit, l’abondance seule peut induire en erreur.
Une vue en plusieurs couches des tumeurs
Pour répondre à ce problème, l’équipe a profilé des tumeurs de 69 personnes atteintes de cancers avancés de divers types, notamment du cerveau, du poumon et du tube digestif. Pour chaque patient, ils ont analysé l’ADN et l’ARN par séquençage clinique de nouvelle génération et, crucialement, ont utilisé une technique très sensible appelée arrays protéiques en phase inverse sur cellules tumorales microdissectées au laser. Cela leur a permis de quantifier non seulement la protéine HER2 totale, mais aussi des modifications spécifiques d’activation — des marques de phosphorylation — sur HER2 et EGFR ainsi que sur des protéines clés en aval. Les patients ont été classés en groupes selon que leurs tumeurs présentaient des altérations du gène HER2, une surexpression de l’ARN, les deux ou aucune.
Quand gènes et signaux divergent
Les résultats ont révélé un décalage saisissant entre les altérations au niveau du gène et l’activité réelle de la voie. Beaucoup de patients porteurs de mutations HER2 ou EGFR ou d’excès de copies géniques présentaient peu ou pas de phosphorylation activatrice d’HER2. À l’inverse, certains patients sans anomalies détectables de l’ADN ou de l’ARN HER2 avaient HER2 et EGFR fortement activés, notamment en deux sites clés qui définissent un motif appelé signature HARPS. Les tumeurs présentant cette co‑activation montraient un engagement clair des voies en aval qui stimulent la croissance et la survie cellulaire. Par exemple, dans les cancers du cerveau, plus de la moitié des glioblastomes présentaient cette signature activée malgré l’absence d’altérations ADN classiques d’HER2, tandis que les méningiomes ne l’affichaient généralement pas.
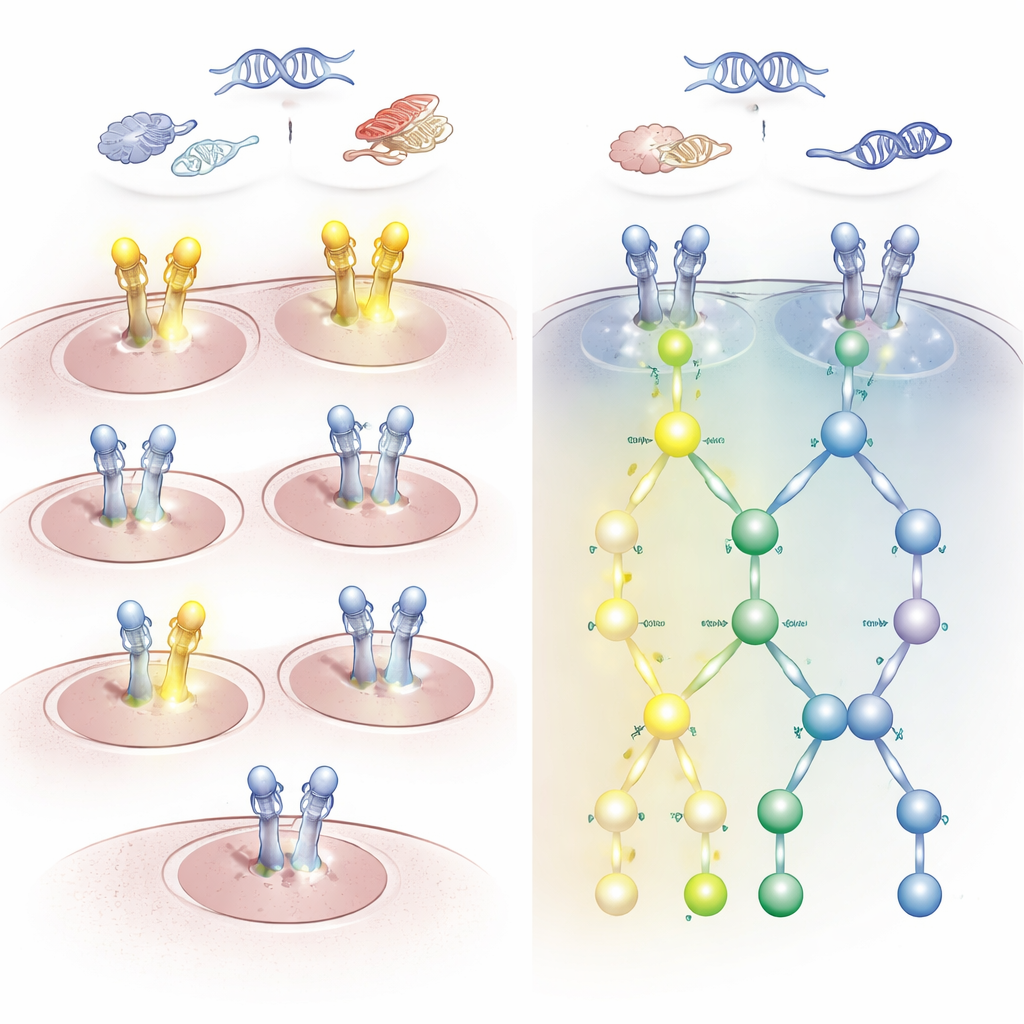
Implications pour le choix du bon médicament
Ces discordances ne sont pas que théoriques. Certains patients dont les tumeurs auraient été classées HER2‑négatives par les tests standards pourraient néanmoins répondre à des médicaments ciblant HER2 ou EGFR si leurs voies de signalisation sont activées. D’autres, fortement positifs aux tests de coloration ou d’ADN, peuvent en réalité présenter une signalisation HER2 silencieuse et être peu susceptibles de bénéficier de ces traitements. L’étude a également mis en évidence des cas où d’autres mutations oncogéniques, comme KRAS ou BRAF, coïncidaient avec une absence d’activation HER2/EGFR ; ces patients seraient probablement mieux traités par des thérapies ciblant ces autres drivers plutôt que par HER2.
Vers une oncologie de précision plus intelligente
Les auteurs concluent que, pour réellement personnaliser les thérapies dirigées contre HER2, il faut dépasser le simple séquençage de l’ADN et la mesure de l’abondance protéique. Des mesures directes de l’activité fonctionnelle des protéines — en particulier la phosphorylation de HER2 et d’EGFR — devraient être intégrées aux protocoles d’oncologie de précision. En ajoutant cette couche d’information, les cliniciens peuvent identifier avec plus d’exactitude qui est susceptible de bénéficier d’inhibiteurs de kinases, d’anticorps et de conjugués anticorps‑médicament ciblant la famille HER. En termes pratiques, il ne suffit pas de savoir que l’interrupteur est installé dans la tumeur ; il faut savoir s’il est effectivement allumé.
Citation: Hunt, A.L., Randall, J., Ogata, J.D. et al. Pan-cancer multi-omic ERBB2-HER2 characterization using next-generation sequencing and quantitative proteomics. npj Precis. Onc. 10, 153 (2026). https://doi.org/10.1038/s41698-026-01351-y
Mots-clés: HER2, EGFR, oncologie de précision, phosphoprotéomique, thérapie ciblée