Clear Sky Science · de
Pan-krebs Multi-omische ERBB2-HER2-Charakterisierung mittels Next-Generation-Sequencing und quantitativer Proteomik
Warum das für Krebspatienten wichtig ist
Krebsmedikamente, die gezielt ein Molekül namens HER2 ansprechen, haben die Behandlung vieler Menschen mit Brust- und anderen Krebsarten grundlegend verändert. Dennoch fällt es Ärztinnen und Ärzten weiterhin schwer, genau vorherzusagen, wer davon profitieren wird. Diese Studie zeigt, dass die üblichen genetischen Tests und Färbeverfahren Patienten übersehen können, deren Tumoren tatsächlich von HER2‑vermittelter Signalgebung abhängig sind — und zugleich fälschlich andere als potenzielle Kandidaten markieren, die wahrscheinlich nicht ansprechen. Indem die Forschenden direkt messen, wie HER2 und sein Partner EGFR innerhalb von Tumoren aktiviert sind, skizzieren sie einen präziseren Weg, Patientinnen und Patienten mit zielgerichteten Therapien zusammenzubringen.
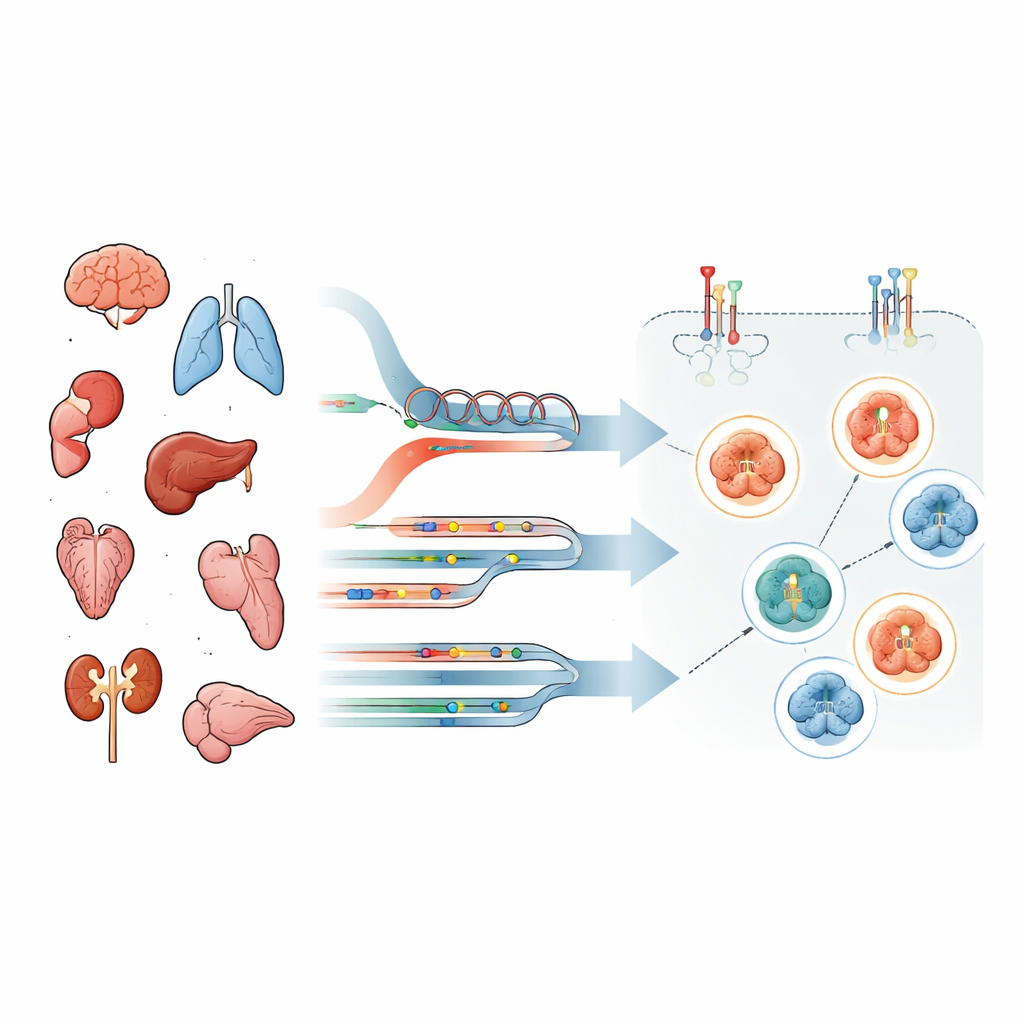
Über die Standardlabortests hinausblicken
Die meisten Krankenhäuser beurteilen, ob ein Tumor „HER2-positiv“ ist, mit zwei Routinetools: einer mikroskopischen Färbung, die zeigt, wie viel HER2-Protein an der Zelloberfläche sitzt, und DNA-Tests, die zusätzliche Kopien oder Mutationen des HER2-Gens (ERBB2 genannt) nachweisen. Diese Ansätze konzentrieren sich darauf, wie viel unverändertes HER2 vorhanden ist, nicht darauf, ob es tatsächlich Wachstumssignale aussendet. Zielgerichtete Medikamente fallen jedoch in unterschiedliche Klassen. Einige Antikörper-Wirkstoff-Konjugate benötigen HER2 hauptsächlich als Andockstelle, während Tyrosinkinaseinhibitoren nur wirken, wenn der HER2/EGFR-Signal-Schalter tatsächlich eingeschaltet ist. Das bedeutet, dass die bloße Menge irreführend sein kann.
Eine mehrschichtige Sicht auf Tumoren
Um dieses Problem anzugehen, analysierte das Team Tumoren von 69 Menschen mit fortgeschrittenen Krebserkrankungen verschiedener Typen, darunter Hirn-, Lungen- und Magen-Darm-Tumoren. Von jeder Patientin/jedem Patienten untersuchten sie DNA und RNA mittels klinischem Next-Generation-Sequencing und nutzten entscheidend eine sehr sensitive Technik namens Reverse-Phase-Protein-Arrays an laser-mikrodiskettierten Tumorzellen. Dadurch konnten sie nicht nur das gesamte HER2-Protein quantifizieren, sondern auch spezifische „An“-Modifikationen — Phosphorylierungsmarken — auf HER2 und EGFR sowie auf wichtigen Signalproteinen downstream. Die Patienten wurden in Gruppen eingeteilt, je nachdem, ob ihre Tumoren HER2-Genveränderungen, RNA-Überexpression, beides oder keines von beidem zeigten.
Wenn Gene und Signale nicht übereinstimmen
Die Ergebnisse zeigten eine auffällige Diskrepanz zwischen genetischen Veränderungen und tatsächlicher Pfadaktivität. Viele Patientinnen und Patienten mit HER2- oder EGFR-Mutationen oder zusätzlichen Genkopien wiesen wenig bis keine aktivierende Phosphorylierung an HER2 auf. Umgekehrt hatten einige Patientinnen und Patienten ohne nachweisbare HER2-Gen- oder RNA-Abnormalitäten stark aktiviertes HER2 und EGFR, insbesondere an zwei Schlüsselstellen, die ein Muster bilden, das als HARPS-Signatur bezeichnet wird. Tumoren mit dieser Koaktivierung zeigten eine klare Aktivierung der nachgelagerten Wege, die Zellwachstum und -überleben antreiben. Bei Hirntumoren beispielsweise zeigten mehr als die Hälfte der Glioblastome diese aktivierte Signatur, obwohl klassische HER2-DNA-Veränderungen fehlten, während Meningeome dies im Allgemeinen nicht taten.
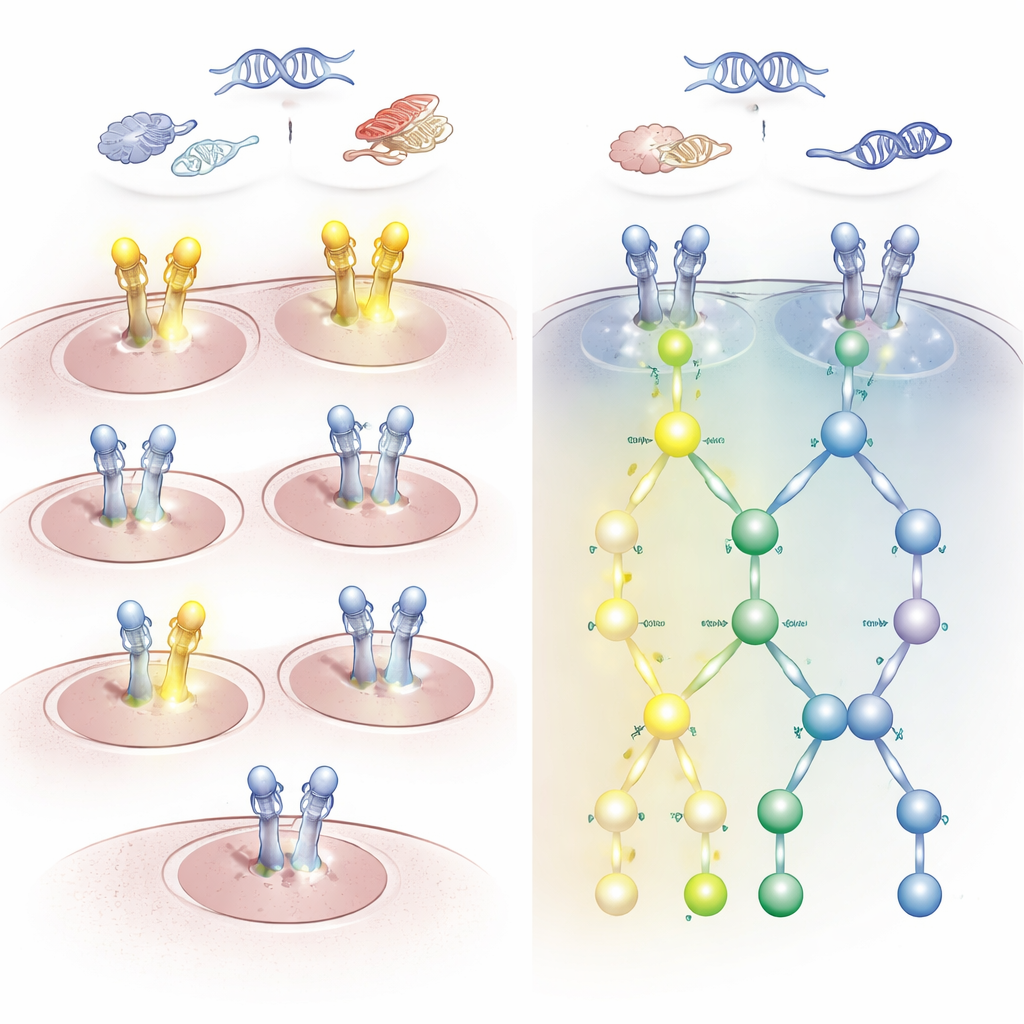
Folgen für die Wahl des richtigen Medikaments
Diese Diskrepanzen sind nicht nur akademisch. Einige Patientinnen und Patienten, deren Tumoren nach Standardtests als HER2-negativ eingestuft worden wären, könnten dennoch auf HER2- oder EGFR‑gerichtete Medikamente ansprechen, wenn ihre Signalwege aktiviert sind. Andere, die nach Färbung oder DNA-Tests stark positiv erscheinen, können tatsächlich ruhige HER2-Signalgebung haben und werden wahrscheinlich nicht von solchen Therapien profitieren. Die Studie hob auch Fälle hervor, in denen andere Treibermutationen, etwa in KRAS oder BRAF, mit einem Mangel an HER2/EGFR-Aktivierung einhergingen; diese Patientinnen und Patienten würden wahrscheinlich besser von Therapien profitieren, die auf diese alternativen Treiber abzielen, statt auf HER2.
Auf dem Weg zu klügerer Präzisionsonkologie
Die Autorinnen und Autoren kommen zu dem Schluss, dass Ärztinnen und Ärzte, um HER2‑gerichtete Therapien wirklich zu personalisieren, über DNA-Sequenzierung und einfache Proteinmengenmessungen hinausgehen müssen. Direkte Messungen funktioneller Proteinaktivität — insbesondere die Phosphorylierung von HER2 und EGFR — sollten in Präzisionsonkologie-Workflows integriert werden. Durch das Hinzufügen dieser Informationsschicht können Kliniker genauer identifizieren, wer wahrscheinlich von Kinaseinhibitoren, Antikörpern und Antikörper-Wirkstoff-Konjugaten profitiert, die die HER-Familie ansprechen. Einfach gesagt: Es reicht nicht zu wissen, dass der Schalter im Tumor eingebaut ist; wir müssen wissen, ob er tatsächlich eingeschaltet ist.
Zitation: Hunt, A.L., Randall, J., Ogata, J.D. et al. Pan-cancer multi-omic ERBB2-HER2 characterization using next-generation sequencing and quantitative proteomics. npj Precis. Onc. 10, 153 (2026). https://doi.org/10.1038/s41698-026-01351-y
Schlüsselwörter: HER2, EGFR, präzisionsonkologie, Phosphoproteomik, zielgerichtete Therapie