Clear Sky Science · ar
تصنيف واسع لسرطانات متعددة باستخدام بيانات أوميكس متعددة لـ ERBB2‑HER2 عبر التسلسل الجيني من الجيل التالي والبروتيوميات الكمية
لماذا يهم هذا لمرضى السرطان
الأدوية المضادة للسرطان التي تستهدف جزيئاً يسمى HER2 غيّرت علاج العديد من المصابين بسرطان الثدي وأنواع أخرى من السرطان. ومع ذلك، لا يزال الأطباء يواجهون صعوبة في التنبؤ بمن سيستفيد بدقة. تُظهر هذه الدراسة أن اختبارات الجينات والصبغات الشائعة قد تفوت مرضى تعتمد أورامهم فعلياً على إشارات مرتبطة بـ HER2 — وقد تشير خطأً إلى آخرين من غير المرجح أن يستجيبوا. من خلال قياس مدى تفعيل HER2 وشريكه EGFR داخل الأورام بشكل مباشر، يحدد الباحثون طريقة أدق لمطابقة المرضى مع العلاجات الموجهة.
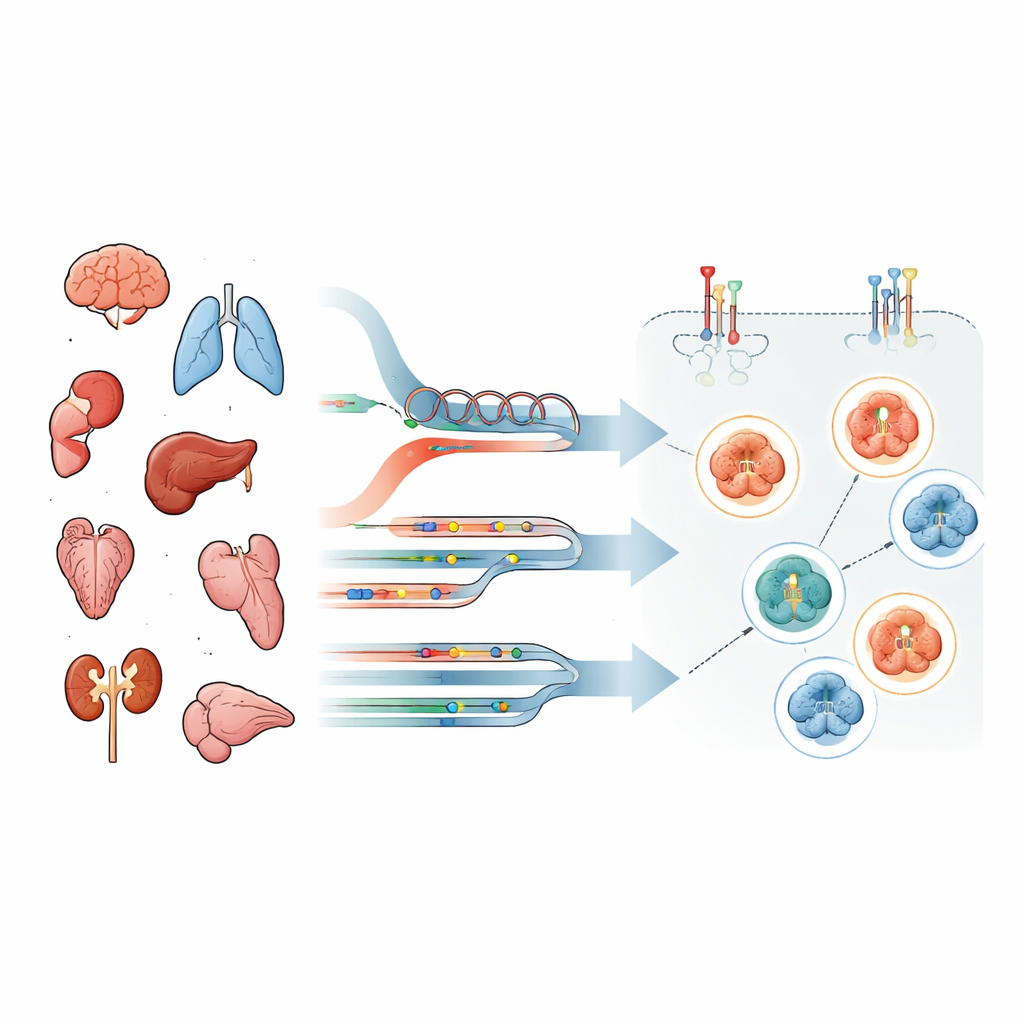
النظر إلى ما وراء الاختبارات المختبرية القياسية
تُقيّم معظم المستشفيات ما إذا كان الورم «إيجابياً لـ HER2» باستخدام أداتين روتينيتين: صبغة ميكروسكوبية تُظهر كمية بروتين HER2 على سطح الخلية، واختبارات DNA تكشف النسخ الإضافية أو الطفرات في جين HER2 (المسمى ERBB2). تركز هذه الأساليب على مقدار HER2 غير المعدّل الموجود، وليس على ما إذا كان يُصدر إشارات نمو فعالة. ومع ذلك، تنتمي الأدوية الموجهة إلى فئات مختلفة. بعض المقترانات من نوع جسم مضاد–دواء تحتاج في المقام الأول وجود HER2 كقاعدة ربط، بينما تعمل مثبطات كيناز التيروسين فقط إذا كان مفتاح إشارات HER2/EGFR مُفعلًا فعلاً. وهذا يعني أن الوفرة وحدها قد تكون مضللة.
رؤية متعددة الطبقات للأورام
لمعالجة هذه المشكلة، حلل الفريق أورام 69 مريضاً مصابين بسرطانات متقدمة من أنواع عديدة، بما في ذلك أورام الدماغ والرئة والجهاز الهضمي. من كل مريض، حلّلوا DNA وRNA باستخدام تسلسل الجيل التالي السريري و، والأهم، استخدموا تقنية شديدة الحساسية تسمى مصفوفات البروتين العكسية على خلايا ورمية مقتطعة بالليزر. سمح لهم ذلك بتكمية ليس فقط إجمالي بروتين HER2 ولكن أيضاً التعديلات المحددة «الفعّالة» — علامات الفسفرة — على HER2 وEGFR وعلى بروتينات إشارية رئيسية في المسار السفلي. تم تقسيم المرضى إلى مجموعات بناءً على ما إذا أظهرت أورامهم تغيّرات جينية في HER2، أو زيادة في التعبير RNA، أو كلاهما، أو لا شيء.
عندما تختلف الجينات عن الإشارات
أظهرت النتائج عدم تطابق لافت بين تغيّرات مستوى الجين والنشاط الفعلي للمسارات. أظهر العديد من المرضى الذين يحملون طفرات في HER2 أو EGFR أو نسخ جينية زائدة القليل أو لا شيء من فسفرة التفعيل على HER2. وعلى العكس من ذلك، كان لدى بعض المرضى الذين لم تُكتشف لديهم شذوذات في جين أو RNA HER2 تفعيل قوي لـ HER2 وEGFR، خاصة في موقعين رئيسيين يحددان نمطاً يُسمى توقيع HARPS. أظهرت الأورام ذات هذا التفعيل المشترك انخراطاً واضحاً للمسارات السفلية التي تحفز نمو الخلية وبقائها. في سرطانات الدماغ، على سبيل المثال، أظهر أكثر من نصف الأورام الدبقية هذا التوقيع المفعل على الرغم من افتقارها للتغيرات الجينية التقليدية في HER2، بينما لم تظهر الأورام السحائية ذلك عمومًا.
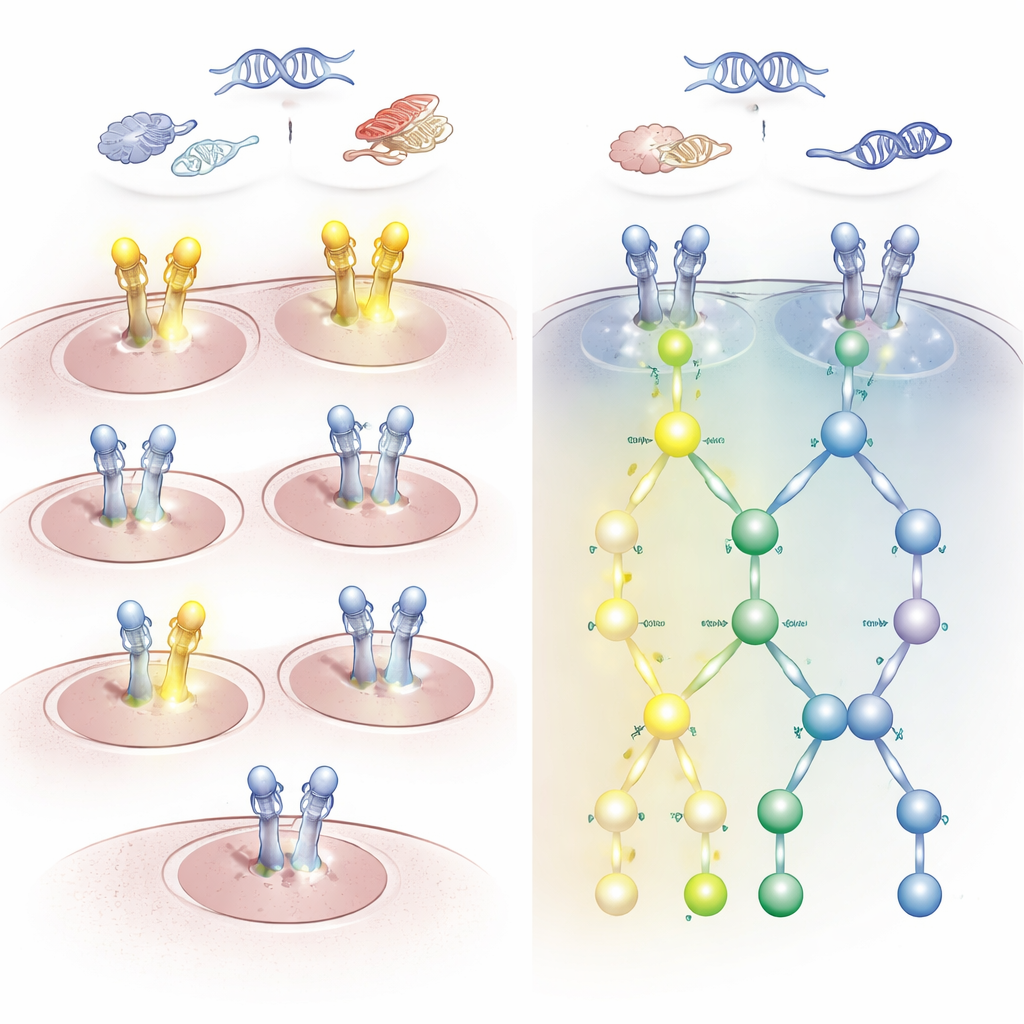
تداعيات لاختيار الدواء المناسب
ليست هذه التباينات أموراً نظرية فحسب. قد يستجيب بعض المرضى الذين كانت اختباراتهم الاعتيادية ستصنفهم على أنهم سلبيو HER2 لأدوية موجهة ضد HER2 أو EGFR إذا كانت مسارات الإشارة لديهم مُفعّلة. وأما الآخرون الذين يبدون إيجابيين بقوة حسب الصباغة أو اختبارات DNA فقد تكون إشارات HER2 لديهم خاملة بالفعل ومن غير المحتمل أن يستفيدوا من هذه العلاجات. كما سلطت الدراسة الضوء على حالات كانت فيها طفرات سائدة أخرى، مثل KRAS أو BRAF، متزامنة مع غياب تفعيل HER2/EGFR؛ من المرجح أن يكون هؤلاء المرضى أفضل خدمةً بعلاجات تستهدف هذه السواقة البديلة بدلاً من HER2.
نحو طب دقيق أذكى
يخلص المؤلفون إلى أنه لتخصيص العلاج الموجه لـ HER2 فعلياً، يجب على الأطباء تجاوز تسلسل DNA وبساطة قياس كمية البروتين. ينبغي دمج قياسات مباشرة لنشاط البروتين الوظيفي — خاصة فسفرة HER2 وEGFR — في سير عمل الأورام الدقيقة. بإضافة هذه الطبقة من المعلومات، يمكن للأطباء تحديد من المرجح أن يستفيد بدقة أكبر من مثبطات الكيناز، والأجسام المضادة، والمقترانات من نوع جسم مضاد–دواء التي تستهدف عائلة HER. بعبارات يومية، لا يكفي معرفة أن المفتاح مُركب داخل الورم؛ يجب أن نعرف ما إذا كان فعلاً مُشغلاً.
الاستشهاد: Hunt, A.L., Randall, J., Ogata, J.D. et al. Pan-cancer multi-omic ERBB2-HER2 characterization using next-generation sequencing and quantitative proteomics. npj Precis. Onc. 10, 153 (2026). https://doi.org/10.1038/s41698-026-01351-y
الكلمات المفتاحية: HER2, EGFR, الأورام الدقيقة الموجهة حسب الدقة, الفوسفوبروتيوميات, العلاج الموجه