Clear Sky Science · it
Caratterizzazione pan‑tumorale multi‑omica di ERBB2‑HER2 mediante sequenziamento di nuova generazione e proteomica quantitativa
Perché è importante per i pazienti oncologici
I farmaci oncologici che prendono di mira una molecola chiamata HER2 hanno trasformato il trattamento di molte persone con tumori al seno e altri tipi di cancro. Tuttavia i medici faticano ancora a prevedere con precisione chi ne trarrà beneficio. Questo studio mostra che i consueti test genetici e di colorazione possono non riconoscere pazienti i cui tumori dipendono davvero dalla segnalazione legata a HER2 — e possono al contrario segnalare erroneamente altri che difficilmente risponderanno. Misurando direttamente come HER2 e il suo partner EGFR sono attivati nei tumori, i ricercatori delineano un modo più preciso di associare i pazienti alle terapie mirate.
Guardare oltre i test di laboratorio standard
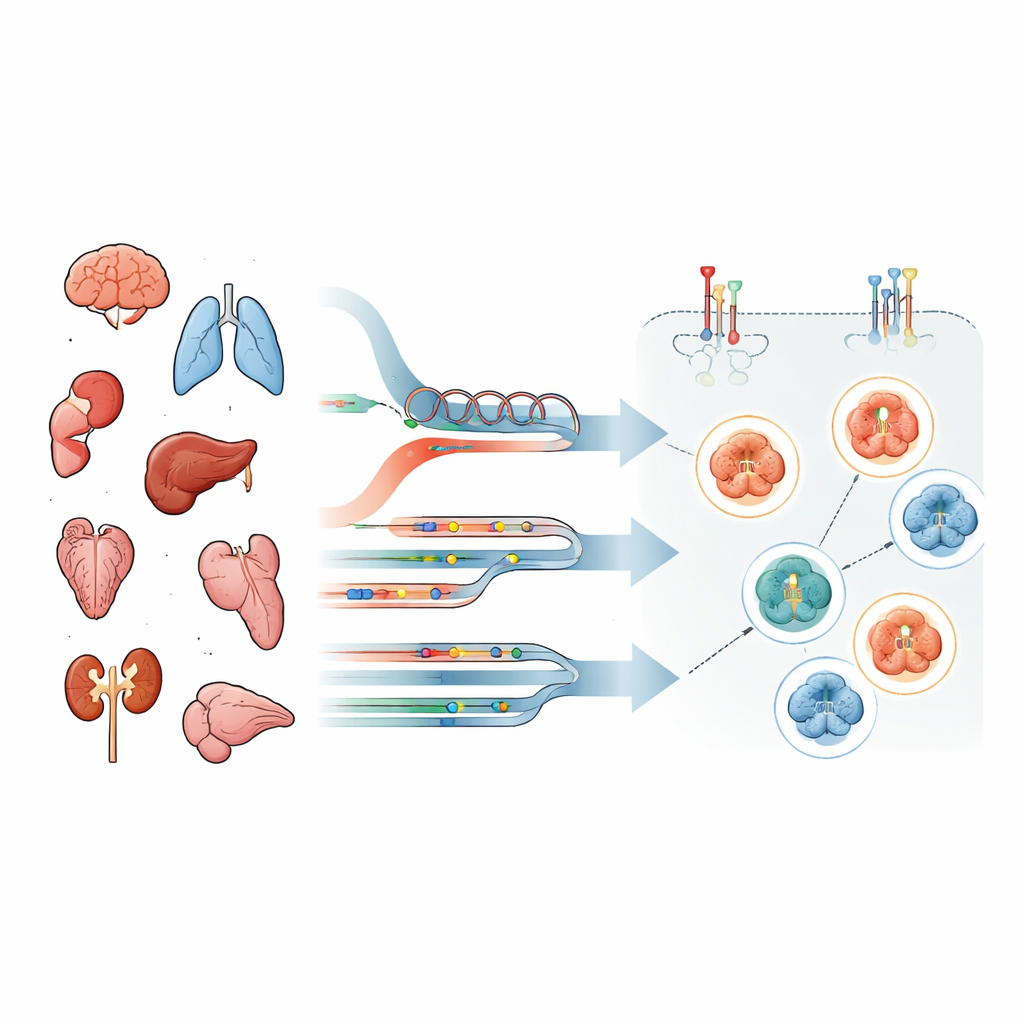
La maggior parte degli ospedali valuta se un tumore è “HER2‑positivo” utilizzando due strumenti di routine: una colorazione al microscopio che mostra quanto HER2 è presente sulla superficie cellulare e test del DNA che rilevano copie extra o mutazioni del gene HER2 (chiamato ERBB2). Questi approcci si concentrano su quanto HER2 non modificato è presente, non sul fatto che stia effettivamente inviando segnali di crescita. I farmaci mirati, però, appartengono a classi diverse. Alcuni anticorpi coniugati a farmaci richiedono soprattutto la presenza di HER2 come punto di ancoraggio, mentre gli inibitori delle tirosin chinasi funzionano solo se l’interruttore di segnalazione HER2/EGFR è effettivamente attivato. Ciò significa che la sola abbondanza può essere fuorviante.
Una vista multilivello dei tumori
Per affrontare questo problema, il gruppo ha profilato i tumori di 69 persone con tumori avanzati di vari tipi, inclusi tumori cerebrali, polmonari e gastrointestinali. Da ciascun paziente hanno analizzato DNA e RNA con sequenziamento clinico di nuova generazione e, cosa cruciale, hanno usato una tecnica altamente sensibile chiamata reverse‑phase protein arrays su cellule tumorali microdissezionate con laser. Questo ha permesso di quantificare non solo la proteina HER2 totale ma anche specifiche modifiche “attivanti” — marcature di fosforilazione — su HER2 e EGFR e su proteine chiave della segnalazione a valle. I pazienti sono stati raggruppati in base al fatto che i loro tumori mostrassero alterazioni del gene HER2, sovraespressione di RNA, entrambe o nessuna delle due.
Quando geni e segnali non coincidono
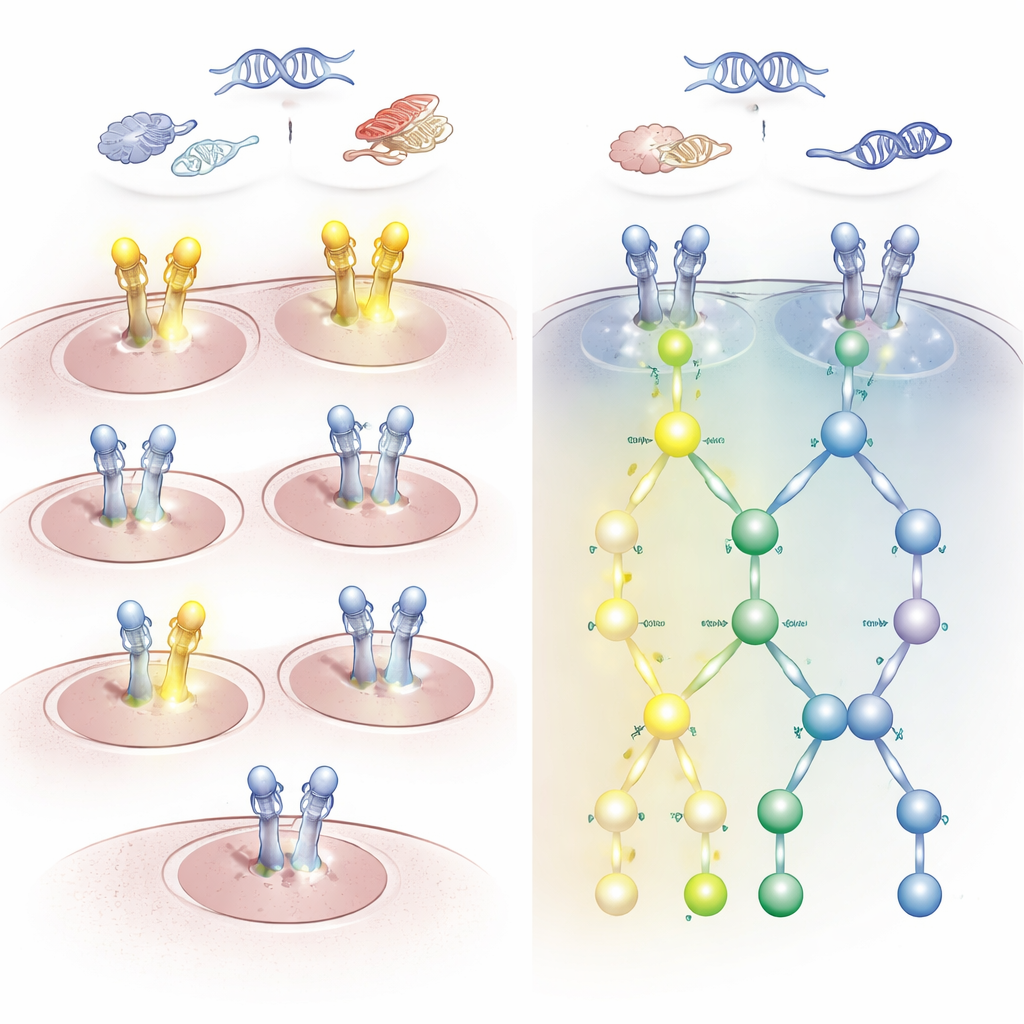
I risultati hanno rivelato una marcata discrepanza tra le alterazioni a livello genico e l’effettiva attività della via di segnalazione. Molti pazienti con mutazioni o copie extra di HER2 o EGFR mostravano poca o nessuna fosforilazione attivante su HER2. Al contrario, alcuni pazienti senza anomalie rilevabili a livello di gene o RNA HER2 avevano HER2 e EGFR fortemente attivati, specialmente in due siti chiave che definiscono un pattern chiamato firma HARPS. I tumori con questa co‑attivazione mostravano un chiaro coinvolgimento delle vie a valle che guidano la crescita e la sopravvivenza cellulare. Nei tumori cerebrali, per esempio, oltre la metà dei glioblastomi presentava questa firma attivata pur non avendo le classiche alterazioni del DNA di HER2, mentre i meningiomi generalmente non la mostravano.
Implicazioni nella scelta della terapia giusta
Queste discrepanze non sono solo accademiche. Alcuni pazienti i cui tumori sarebbero stati etichettati come HER2‑negativi dai test standard potrebbero comunque rispondere a farmaci mirati contro HER2 o EGFR se le loro vie di segnalazione sono attivate. Altri che appaiono fortemente positivi alla colorazione o ai test del DNA possono, in realtà, avere una segnalazione HER2 silente e quindi non trarre beneficio da tali trattamenti. Lo studio ha inoltre evidenziato casi in cui altre mutazioni driver, come in KRAS o BRAF, coincidevano con l’assenza di attivazione HER2/EGFR; questi pazienti probabilmente trarrebbero maggiore vantaggio da terapie rivolte a quei driver alternativi piuttosto che a HER2.
Verso un’oncologia di precisione più intelligente
Gli autori concludono che per personalizzare veramente la terapia diretta contro HER2, i medici devono andare oltre il sequenziamento del DNA e la semplice abbondanza proteica. Le misurazioni dirette dell’attività funzionale delle proteine — in particolare la fosforilazione di HER2 e EGFR — dovrebbero essere integrate nei flussi di lavoro dell’oncologia di precisione. Aggiungendo questo livello di informazione, i clinici possono identificare con maggiore accuratezza chi è probabile che benefici di inibitori delle chinasi, anticorpi e anticorpi‑coniugati a farmaci che prendono di mira la famiglia HER. In termini pratici, non basta sapere che l’interruttore è installato nel tumore; dobbiamo sapere se è effettivamente acceso.
Citazione: Hunt, A.L., Randall, J., Ogata, J.D. et al. Pan-cancer multi-omic ERBB2-HER2 characterization using next-generation sequencing and quantitative proteomics. npj Precis. Onc. 10, 153 (2026). https://doi.org/10.1038/s41698-026-01351-y
Parole chiave: HER2, EGFR, oncologia di precisione, fosfoproteomica, terapia mirata