Clear Sky Science · zh
GPR124 调节玻璃体血管消退并与内皮-间质转变相关
为何微小的眼内血管必须消失
出生前,眼球内部布满了一张临时的血管网,为正在生长的晶状体及周围组织提供养分。为了日后获得清晰视力,这一支架必须按时消失,并由永久的视网膜循环取代。当这一清理过程失败时,儿童可能出现严重的眼疾,包括视网膜脱离和失明。本研究提出了一个基础但关键的问题:哪些分子信号告诉这些临时血管何时以及如何消失?
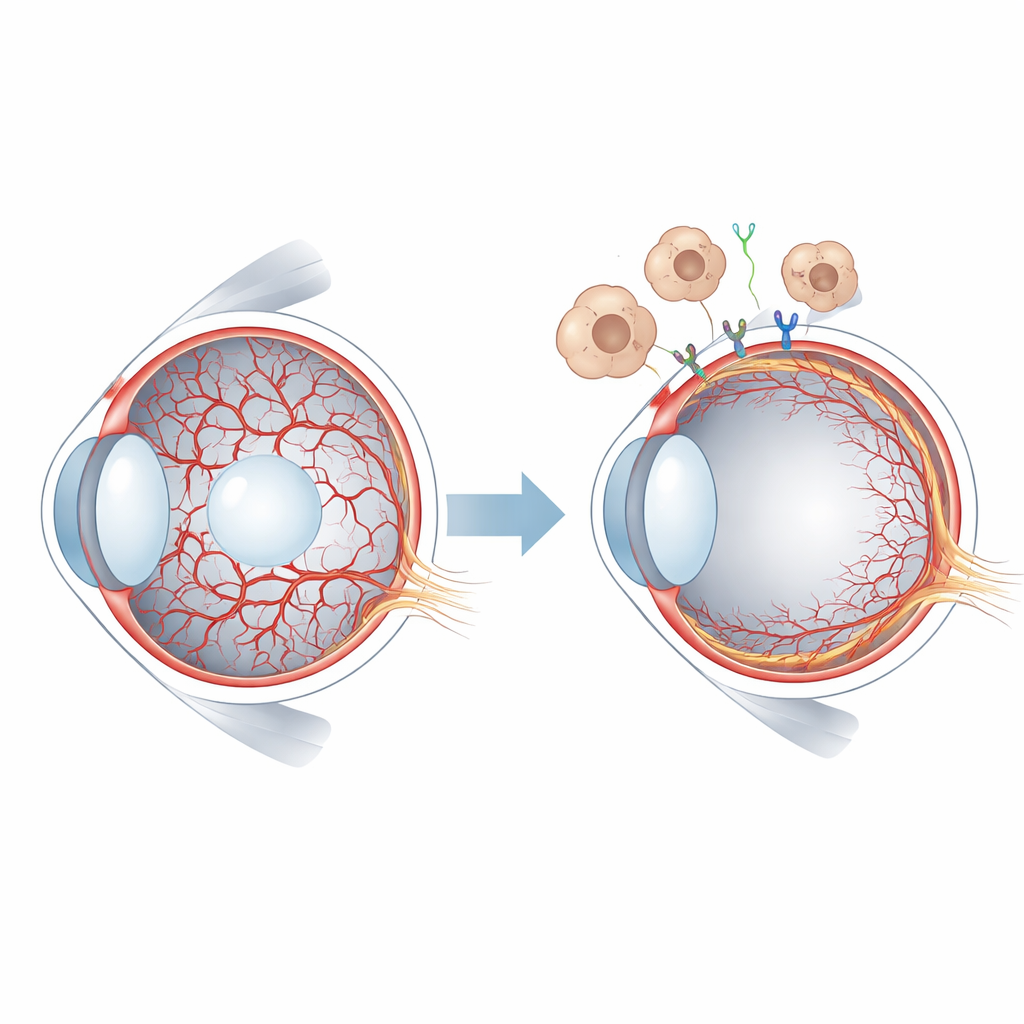
幼年眼中的短暂供血
在哺乳动物中,早期眼组织由玻璃体血管供养,这是一张细腻的网络,跨越眼球的凝胶状中心并包绕晶状体。随着视网膜开始建立自身的血供,玻璃体系统必须退化并清除。在人类这一过程在出生前完成,而在小鼠中则发生于出生后,这为实验研究提供了便利窗口。当玻璃体血管持续存在时(称为持续性增生性原发性玻璃体病),视力可能严重受损。研究者已知一类称为 WNT 的信号,尤其是由巨噬细胞释放的 WNT7B 蛋白,有助于触发玻璃体血管的消退。但作用于血管细胞的具体受体及下游事件尚不清楚。
锁定关键的分子把关者
研究小组把注意力集中在 GPR124 上,这是一种类受体蛋白,已知在发育中的大脑中作为 WNT7A 和 WNT7B 的辅受体,促进血管生长和血脑屏障形成。他们构建了能在出生后短期内特异性在内皮细胞——即血管内壁细胞——中删除 GPR124 的小鼠模型。当从玻璃体内皮细胞中去除 GPR124 时,中央眼血管的消退比正常同窝幼鼠明显变慢。玻璃体网络在更长时间内保持更致密,尽管同样的信号似乎并非构建眼内表面永久视网膜血管所必需。这种区室特异性的效应表明,GPR124 对拆解临时玻璃体循环至关重要,但在构建永久视网膜网络方面大体可有可无。
信号如何重塑并移除血管
为了解 GPR124 如何影响细胞行为,研究者测量了玻璃体血管中 WNT 靶基因的活性。他们发现,丧失 GPR124 导致 LEF1 及其他经典 WNT 响应蛋白的核内水平显著降低,表明 WNT/β-连环蛋白通路被抑制。然而 GPR124 并不控制所有形式的细胞死亡。沿着原本完整的血管出现的孤立凋亡内皮细胞数量在有无 GPR124 的情况下相似。相反,GPR124 对于协调性的“节段性”消退是必需的,在这种消退中,一段血管上的一串相邻内皮细胞同时死亡,导致管腔塌陷。这一模式表明 GPR124 有助于将分散的信号转换为协同的重塑事件,从而高效地修剪不需要的血管段。
处于两种身份之间的细胞
进一步深入研究时,团队使用单细胞 RNA 测序对玻璃体网络的单个细胞进行谱系分析。他们发现,具有完整 GPR124 的内皮细胞显示出与部分内皮-间质转变相一致的基因表达模式,这是一种状态,细胞开始丧失部分典型内皮特征,同时获得与更具移动性和基质产能相关的特征。经典内皮标志物如 VE-cadherin 和 血管性梗阻因子(von Willebrand factor)水平降低,而诸如 ZEB1 的间质标志物增加。显微镜学在蛋白水平上证实了这些变化。与此同时,若干促进细胞死亡的基因在 GPR124 阳性细胞中更为活跃,与另一条主要发育通路——转化生长因子 β(TGF-β)相关的基因也发生了改变。相邻的支持细胞称为周细胞表现出继发性应激反应,但仔细的成像显示内皮细胞先于周细胞死亡,随后周细胞丧失,最终留下空的“幽灵”基底膜丝带。
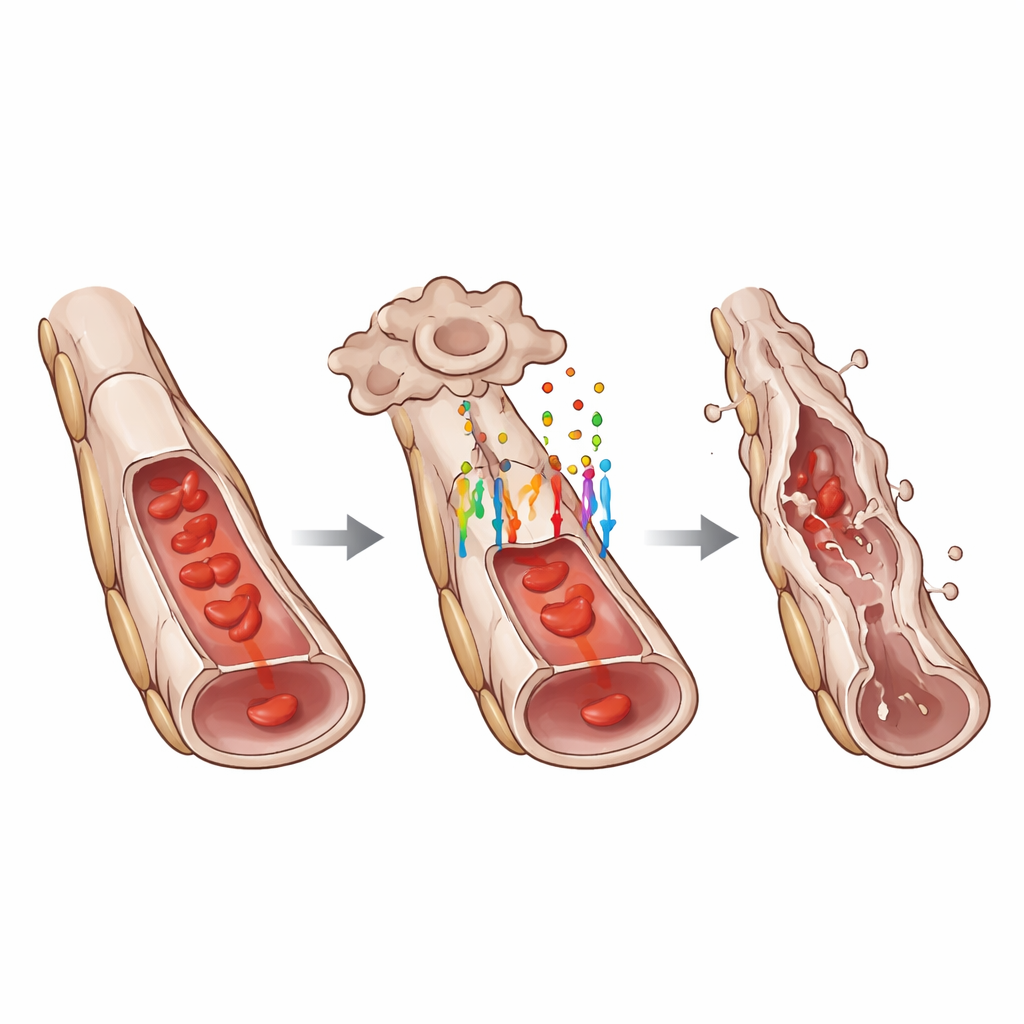
这对眼部健康及更广泛意义的影响
综上所述,这些发现将 GPR124 定位为玻璃体血管消退的核心协调者。通过促进 WNT7 驱动的信号,GPR124 将内皮细胞推向一种过渡状态,松解其连接,促使其进入凋亡准备,并帮助指挥逐步塌陷和清理废弃血管,同时大体保持视网膜血管的生长完整。理解这一精细调控的程序有助于揭示发育中眼睛如何自我重塑,并指出潜在的分子靶点,用于治疗那些临时血管不愿消退的疾病。类似的 GPR124 依赖性转变可能也影响其他器官的血管修剪,提示其在正常发育以及因血管异常持久或瘢痕形成相关的疾病中具有更广泛的相关性。
引用: Hannig, L., Heiden, R., Ergün, S. et al. GPR124 regulates hyaloid blood vessel regression and is associated with endothelial-mesenchymal transition. Sci Rep 16, 13765 (2026). https://doi.org/10.1038/s41598-026-50835-1
关键词: 眼睛发育, 血管消退, Wnt 信号, GPR124, 内皮转变