Clear Sky Science · it
GPR124 regola la regressione dei vasi ipaloidei ed è associato alla transizione endotelio-mesenchimale
Perché i minuscoli vasi oculari devono scomparire
Prima della nascita, l'interno dell'occhio è attraversato da una rete temporanea di vasi sanguigni che nutrono il cristallino in crescita e i tessuti circostanti. Per una visione nitida in seguito, questa impalcatura deve scomparire al momento giusto e essere sostituita dalla circolazione retinica permanente. Quando questa pulizia fallisce, i bambini possono sviluppare gravi problemi oculari, inclusi distacco della retina e cecità. Questo studio pone una domanda fondamentale ma cruciale: quali segnali molecolari dicono a questi vasi temporanei quando e come scomparire?
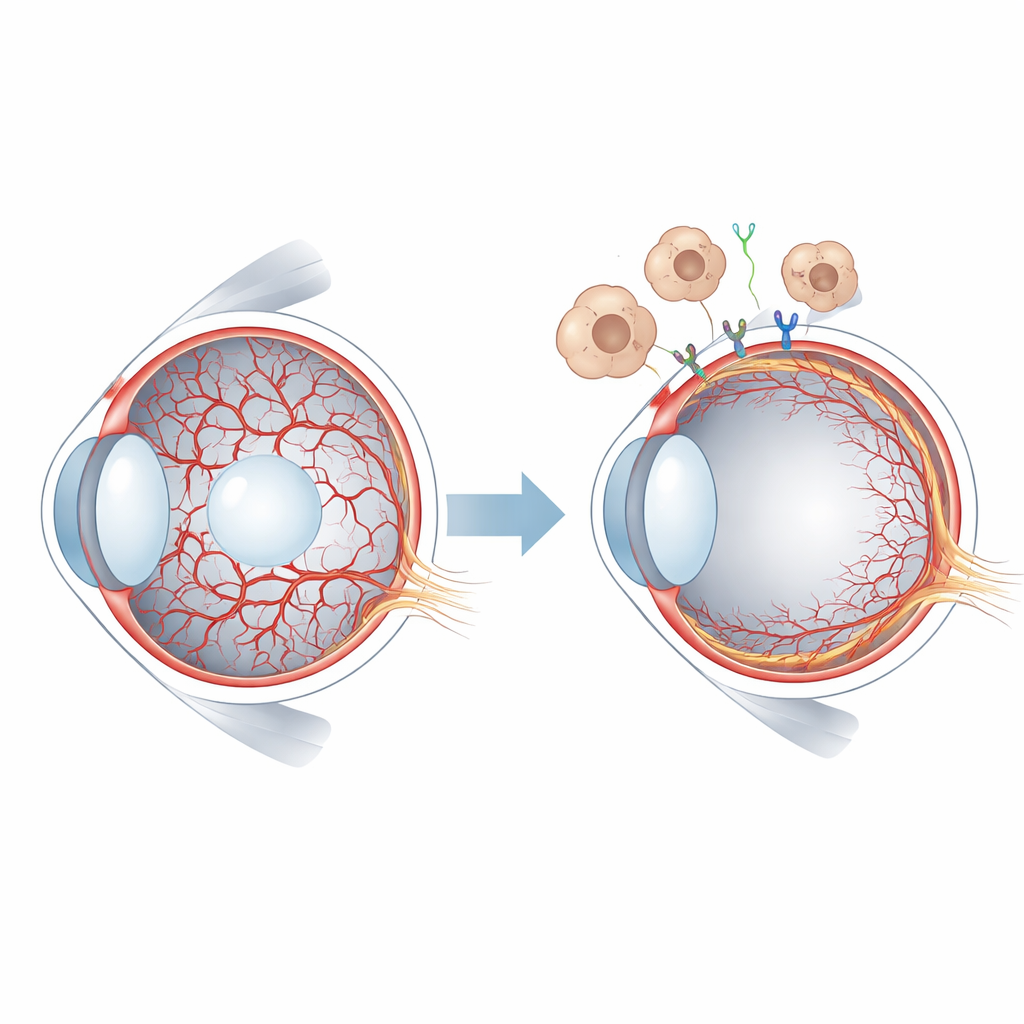
Un apporto ematico a breve vita nell'occhio giovane
Nei mammiferi, i tessuti oculari precoci sono nutriti dai vasi ipaloidei, una rete delicata che attraversa il centro gelatinoso dell'occhio e avvolge il cristallino. Man mano che la retina comincia a costruire il proprio apporto ematico, il sistema ipaloideo deve regredire e venire eliminato. Nell'uomo questo avviene prima della nascita, mentre nei topi si svolge dopo la nascita, offrendo una finestra conveniente per lo studio sperimentale. Quando i vasi ipaloidei persistono, come nella condizione chiamata vitreo primario iperplastico persistente, la vista può essere gravemente compromessa. I ricercatori sapevano già che una famiglia di segnali chiamata WNT, e in particolare la proteina WNT7B rilasciata da cellule immunitarie chiamate macrofagi, aiuta a innescare la regressione dei vasi ipaloidei. Ma i recettori specifici sulle cellule vascolari e gli eventi a valle non erano ben noti.
Individuare un importante guardiano molecolare
Il gruppo si è concentrato su GPR124, una proteina simile a un recettore nota per funzionare come co-recettore per WNT7A e WNT7B nel cervello in sviluppo, dove promuove la crescita dei vasi e la formazione della barriera emato-encefalica. Hanno ingegnerizzato topi in cui GPR124 poteva essere eliminato specificamente nelle cellule endoteliali — le cellule che rivestono i vasi sanguigni — poco dopo la nascita. Quando GPR124 è stato rimosso dalle cellule endoteliali ipaloidee, i vasi centrali dell'occhio hanno regredito molto più lentamente rispetto ai fratelli di cucciolata normali. La rete ipaloidea è rimasta più densa più a lungo, anche se lo stesso segnale sembrava non necessario per la costruzione dei vasi retinici lungo la superficie interna dell'occhio. Questo effetto specifico per compartimento mostra che GPR124 è cruciale per smantellare la circolazione ipaloidea temporanea ma in gran parte non essenziale per costruire la rete retinica permanente.
Come il segnale rimodella ed elimina i vasi
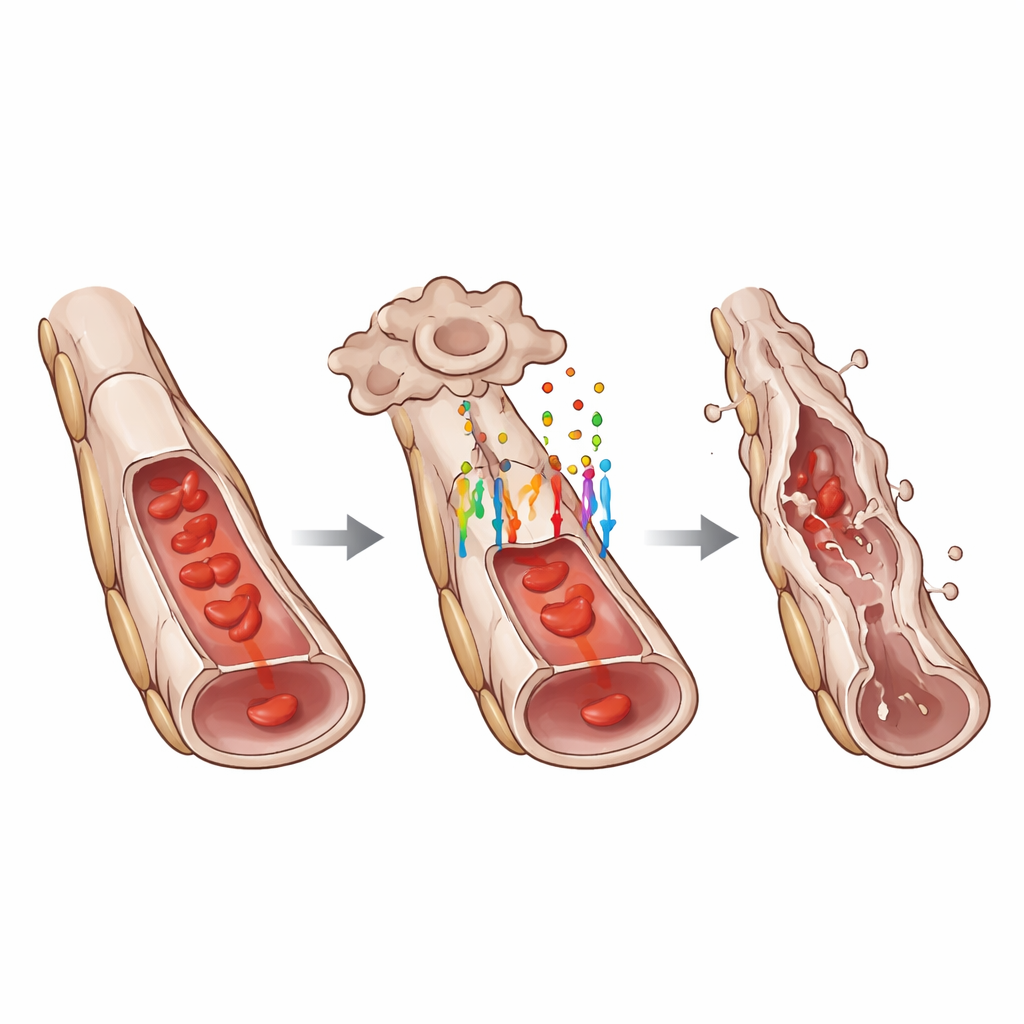
Per capire come GPR124 influenza il comportamento cellulare, i ricercatori hanno misurato l'attività dei geni bersaglio WNT nei vasi ipaloidei. Hanno scoperto che la perdita di GPR124 riduceva marcatamente i livelli nucleari di LEF1 e di altre proteine classiche responsabili della risposta WNT, indicando un’attenuazione della via WNT/β-catenina. Tuttavia GPR124 non controllava tutte le forme di morte cellulare. Il numero di cellule endoteliali isolate in fase di morte lungo vasi altrimenti intatti era simile con o senza GPR124. Al contrario, GPR124 era necessario per la regressione «segmentale» coordinata, in cui stringhe di cellule endoteliali vicine lungo un segmento di vaso morivano insieme, causando il collasso del tubulo. Questo schema suggerisce che GPR124 aiuti a convertire segnali sparsi in un evento di rimodellamento concertato che pota efficacemente i tratti vascolari indesiderati.
Cellule in transizione tra due identità
Approfondendo, il team ha usato il sequenziamento dell'RNA a singola cellula per profilare cellule individuali dalla rete ipaloidea. Hanno scoperto che le cellule endoteliali con GPR124 intatto mostravano un profilo di espressione genica coerente con una transizione parziale da endoteliale a mesenchimale, uno stato in cui cominciano a perdere alcuni tratti caratteristici endoteliali mentre acquisiscono caratteristiche associate a cellule più mobili e produttrici di matrice. Marker endoteliali classici come VE-caderina e il fattore di von Willebrand risultavano ridotti, mentre marker mesenchimali come ZEB1 aumentavano. La microscopia ha confermato questi cambiamenti a livello proteico. Allo stesso tempo, diversi geni che promuovono la morte cellulare erano più attivi nelle cellule GPR124-positive, e geni collegati al fattore di crescita trasformante beta, un’altra importante via dello sviluppo, risultavano anch'essi alterati. Le cellule di supporto vicine, chiamate periciti, mostravano risposte di stress secondarie, ma immagini accurate indicavano che le cellule endoteliali morivano per prime, seguite più tardi dalla perdita dei periciti e, infine, da fili vuoti «fantasma» della membrana basale.
Cosa significa per la salute oculare e oltre
Nel complesso, i risultati pongono GPR124 come un coordinatore centrale della regressione dei vasi ipaloidei. Abilitando la segnalazione guidata da WNT7, GPR124 spinge le cellule endoteliali in uno stato di transizione, allenta le loro giunzioni, le prepara all'apoptosi e aiuta a orchestrare il collasso e la rimozione graduale dei vasi obsoleti, pur lasciando in gran parte intatto la crescita dei vasi retinici. Comprendere questo programma finemente regolato offre intuizioni su come l'occhio in sviluppo si rimodella e individua potenziali bersagli molecolari per trattare disturbi in cui i vasi temporanei si rifiutano di scomparire. Transizioni dipendenti da GPR124 simili potrebbero modellare la potatura dei vasi anche in altri organi, suggerendo rilevanza più ampia per lo sviluppo normale e per malattie caratterizzate da persistenza dei vasi o cicatrizzazione anomala.
Citazione: Hannig, L., Heiden, R., Ergün, S. et al. GPR124 regulates hyaloid blood vessel regression and is associated with endothelial-mesenchymal transition. Sci Rep 16, 13765 (2026). https://doi.org/10.1038/s41598-026-50835-1
Parole chiave: sviluppo oculare, regressione dei vasi sanguigni, segnalazione Wnt, GPR124, transizione endoteliale