Clear Sky Science · fr
GPR124 régule la régression des vaisseaux hyaloïdes et est associé à la transition endothélio-mésenchymateuse
Pourquoi de minuscules vaisseaux oculaires doivent disparaître
Avant la naissance, l’intérieur de l’œil est parcouru par un réseau temporaire de vaisseaux sanguins qui nourrissent le cristallin en croissance et les tissus environnants. Pour une vision nette plus tard dans la vie, cette charpente doit disparaître au bon moment et être remplacée par la circulation rétinienne permanente. Lorsque ce nettoyage échoue, les enfants peuvent développer de graves problèmes oculaires, y compris un décollement de la rétine et la cécité. Cette étude pose une question fondamentale mais cruciale : quels signaux moléculaires indiquent à ces vaisseaux temporaires quand et comment disparaître ?
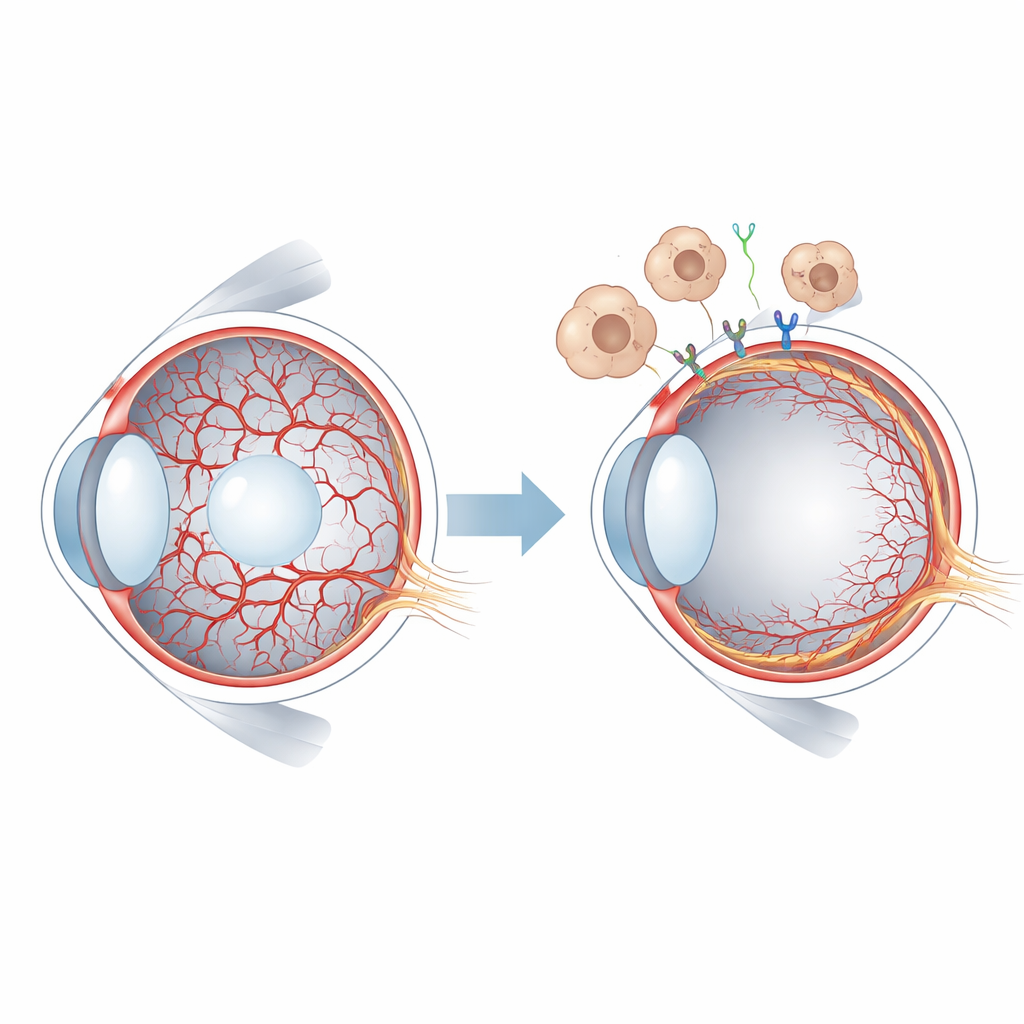
Un apport sanguin de courte durée dans l’œil en développement
Chez les mammifères, les premiers tissus oculaires sont nourris par les vaisseaux hyaloïdes, un réseau délicat qui s’étend au centre gélatineux de l’œil et entoure le cristallin. À mesure que la rétine commence à établir sa propre vascularisation, le système hyaloïde doit régresser et se résorber. Chez l’humain, cela se produit avant la naissance, tandis que chez la souris cela se déroule après la naissance, offrant une fenêtre commode pour l’étude expérimentale. Lorsque les vaisseaux hyaloïdes persistent, comme dans une affection appelée vitré primaire hyperplasique persistant, la vision peut être gravement compromise. Les chercheurs savaient déjà qu’une famille de signaux appelée WNT, et en particulier la protéine WNT7B libérée par des cellules immunitaires appelées macrophages, aide à déclencher la régression des vaisseaux hyaloïdes. Mais les récepteurs spécifiques sur les cellules vasculaires et les événements en aval n’étaient pas bien compris.
Identifier un régulateur moléculaire clé
L’équipe s’est concentrée sur GPR124, une protéine de type récepteur connue pour agir comme corécepteur de WNT7A et WNT7B dans le cerveau en développement, où elle favorise la croissance vasculaire et la formation de la barrière hémato-encéphalique. Ils ont généré des souris dans lesquelles GPR124 pouvait être supprimé spécifiquement dans les cellules endothéliales — les cellules qui tapissent les vaisseaux sanguins — peu après la naissance. Lorsque GPR124 a été retiré des cellules endothéliales hyaloïdes, les vaisseaux centraux de l’œil ont régressé beaucoup plus lentement que chez les congénères normaux. Le réseau hyaloïde est resté plus dense plus longtemps, même si le même signal semblait inutile pour la formation des vaisseaux rétiniens le long de la surface interne de l’œil. Cet effet spécifique à une zone montre que GPR124 est crucial pour démanteler la circulation hyaloïde temporaire mais largement dispensable pour construire le réseau rétinien permanent.
Comment le signal remodèle et élimine les vaisseaux
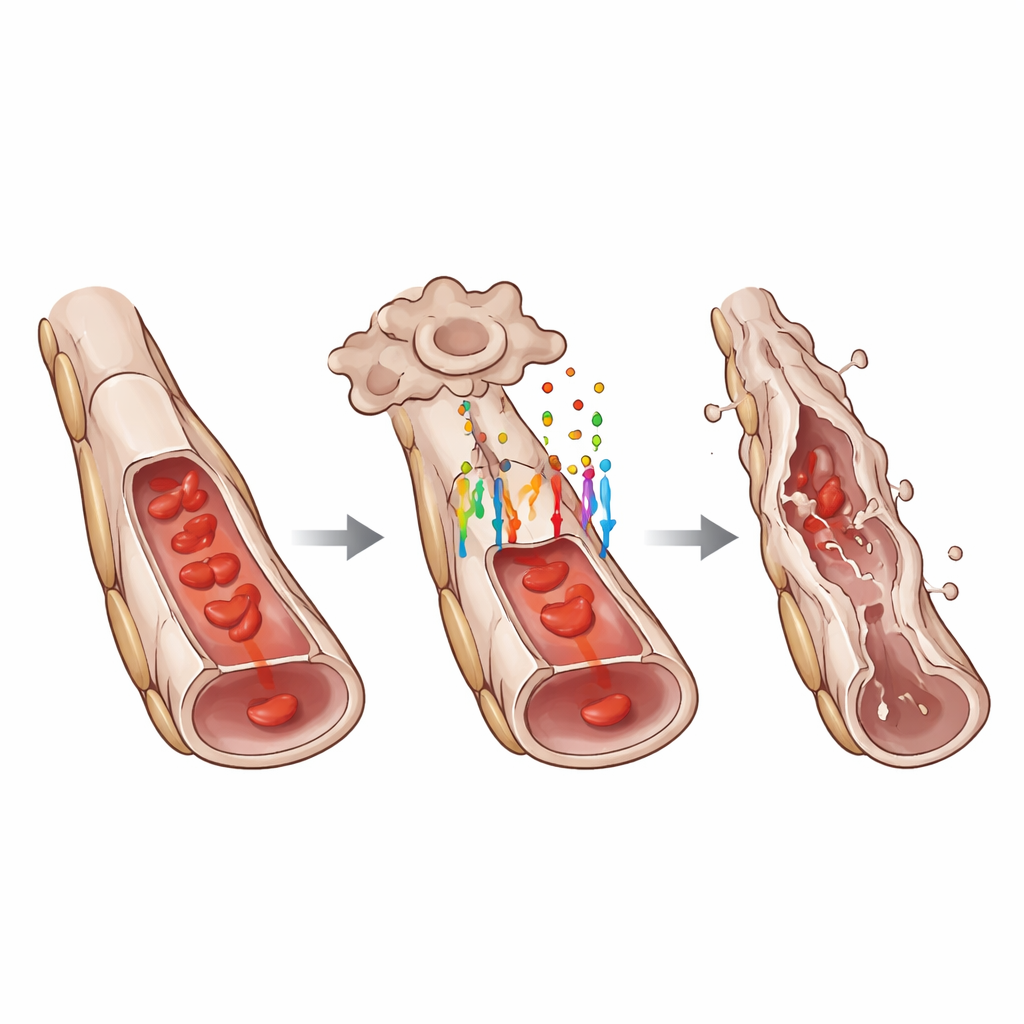
Pour comprendre comment GPR124 influence le comportement cellulaire, les chercheurs ont mesuré l’activité des gènes cibles de WNT dans les vaisseaux hyaloïdes. Ils ont constaté que la perte de GPR124 réduisait nettement les niveaux nucléaires de LEF1 et d’autres protéines classiquement réactives à WNT, indiquant un affaiblissement de la voie WNT/β-caténine. Pourtant GPR124 ne contrôlait pas toutes les formes de mort cellulaire. Le nombre de cellules endothéliales isolées mourantes le long de vaisseaux par ailleurs intacts était similaire avec ou sans GPR124. Au contraire, GPR124 était nécessaire pour une régression « segmentaire » coordonnée, où des rangs de cellules endothéliales voisines le long d’un segment vasculaire mouraient ensemble, provoquant l’effondrement du tube. Ce schéma suggère que GPR124 aide à convertir des signaux dispersés en un événement de remodelage concerté qui émonde efficacement les segments vasculaires indésirables.
Des cellules en transition entre deux identités
Pour approfondir, l’équipe a utilisé le séquençage ARN unicellulaire pour profiler les cellules individuelles du réseau hyaloïde. Ils ont découvert que les cellules endothéliales avec GPR124 intacte présentaient un profil d’expression génique compatible avec une transition partielle endothéliale-vers-mésenchymateuse, un état dans lequel elles commencent à perdre certains traits caractéristiques des endothéliums tout en acquérant des attributs associés à des cellules plus mobiles et productrices de matrice. Les marqueurs endothéliaux classiques tels que la VE-cadhérine et le facteur von Willebrand étaient réduits, tandis que des marqueurs mésenchymateux comme ZEB1 augmentaient. La microscopie a confirmé ces changements au niveau des protéines. Parallèlement, plusieurs gènes favorisant la mort cellulaire étaient plus actifs dans les cellules GPR124-positives, et des gènes liés au facteur de croissance transformant bêta, une autre voie majeure du développement, étaient également altérés. Les cellules de soutien voisines appelées péricytes montraient des réponses de stress secondaires, mais une imagerie attentive a indiqué que les cellules endothéliales mouraient d’abord, suivies plus tard par la perte des péricytes et, finalement, des « fantômes » de membrane basale vides.
Ce que cela signifie pour la santé oculaire et au-delà
Pris ensemble, ces résultats positionnent GPR124 comme un coordinateur central de la régression des vaisseaux hyaloïdes. En permettant la signalisation pilotée par WNT7, GPR124 pousse les cellules endothéliales vers un état de transition, relâche leurs jonctions, les prépare à l’apoptose et aide à orchestrer l’effondrement et le nettoyage progressifs des vaisseaux obsolètes, tout en préservant largement la croissance des vaisseaux rétiniens. Comprendre ce programme finement réglé éclaire la manière dont l’œil en développement se remodèle et met en évidence des cibles moléculaires potentielles pour traiter des troubles où les vaisseaux temporaires refusent de disparaître. Des transitions dépendantes de GPR124 similaires pourraient modeler l’élagage vasculaire dans d’autres organes, suggérant une portée plus vaste pour le développement normal et pour des maladies marquées par une persistance vasculaire anormale ou une cicatrisation.
Citation: Hannig, L., Heiden, R., Ergün, S. et al. GPR124 regulates hyaloid blood vessel regression and is associated with endothelial-mesenchymal transition. Sci Rep 16, 13765 (2026). https://doi.org/10.1038/s41598-026-50835-1
Mots-clés: développement de l’œil, régression des vaisseaux sanguins, signalisation Wnt, GPR124, transition endothéliale