Clear Sky Science · ru
GPR124 регулирует регрессию гиалоидных сосудов и связан с эндотелиально-мезенхимальным переходом
Почему мелкие сосуды глаза должны исчезать
До рождения внутренность глаза пронизана временной сетью кровеносных сосудов, которая питает растущую линзу и окружающие ткани. Для острого зрения позже в жизни этот каркас должен исчезнуть вовремя и быть заменён постоянным сетчатым кровообращением сетчатки. Когда этот «уборочный» процесс срывается, у детей могут развиваться серьёзные проблемы со зрением, включая отслойку сетчатки и слепоту. В этом исследовании ставится простой, но важный вопрос: какие молекулярные сигналы сообщают временным сосудам, когда и как им исчезнуть?
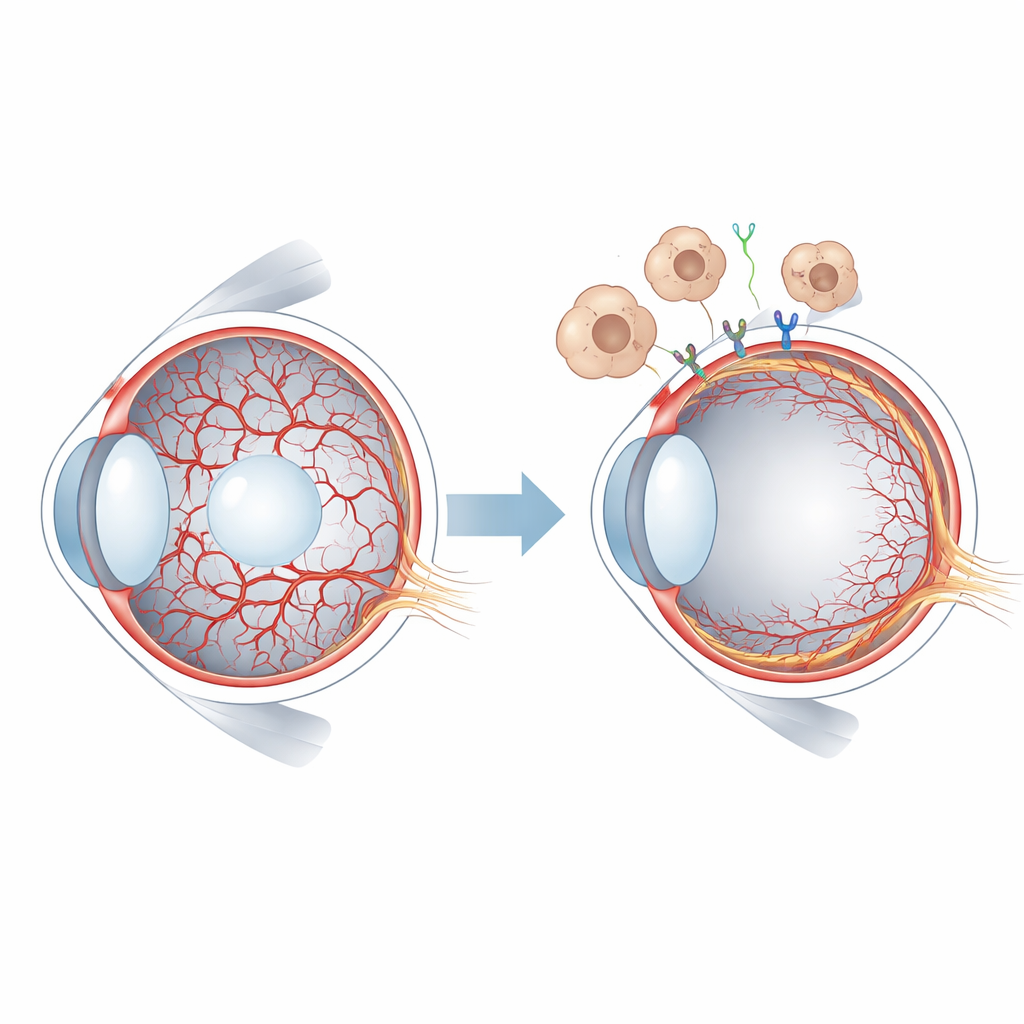
Кратковременное кровоснабжение в молодом глазу
У млекопитающих ранние ткани глаза питаются гиалоидными сосудами — тонкой сетью, простирающейся через желеобразное центральное пространство глаза и охватывающей хрусталик. По мере того как сетчатка начинает строить собственное кровоснабжение, гиалоидная система должна регрессировать и освобождать пространство. У людей это происходит до рождения, а у мышей — после, что даёт удобное окно для экспериментального изучения. Если гиалоидные сосуды сохраняются, как при состоянии, называемом персистирующей гиперпластической первичной стекловидной оболочкой, зрение может серьёзно нарушиться. Ранее исследователи уже знали, что семейство сигналов WNT, и в частности белок WNT7B, выделяемый макрофагами, помогает запускать регрессию гиалоидных сосудов. Но какие рецепторы на клетках сосудов воспринимают эти сигналы и какие события запускаются далее, было мало изучено.
Выявление ключевого молекулярного «шлюза»
Команда сосредоточилась на GPR124 — рецептороподобном белке, известном как со-рецептор для WNT7A и WNT7B в развивающемся мозге, где он способствует росту сосудов и формированию гематоэнцефалического барьера. Учёные создали мышей, в которых GPR124 можно было удалить специфически в эндотелиальных клетках — клетках, выстилающих сосуды — вскоре после рождения. При удалении GPR124 из гиалоидного эндотелия центральные сосуды глаза регрессировали значительно медленнее, чем у нормальных собратьев. Гиалоидная сеть оставалась более плотной дольше, хотя тот же сигнал, по-видимому, не был необходим для формирования сосудов сетчатки вдоль внутренней поверхности глаза. Этот зависящий от компартмента эффект показывает, что GPR124 критически важен для демонтажа временного гиалоидного кровообращения, но в значительной степени не обязателен для построения постоянной сетчаточной сети.
Как сигнал перестраивает и удаляет сосуды
Чтобы понять, как GPR124 влияет на поведение клеток, исследователи измеряли активность генов‑мишеней WNT в гиалоидных сосудах. Они обнаружили, что потеря GPR124 заметно снижала уровень ядерного LEF1 и других классических WNT‑отвечающих белков, указывая на ослабление пути WNT/β‑катенин. Вместе с тем GPR124 не управлял всеми формами гибели клеток. Число одиночных умирающих эндотелиальных клеток вдоль в остальном целых сосудов было похоже при наличии или отсутствии GPR124. Вместо этого GPR124 оказался необходим для согласованной «сегментарной» регрессии, когда цепочки соседних эндотелиальных клеток вдоль участка сосуда массово погибают вместе, вызывая коллапс трубки. Такая картина указывает на то, что GPR124 помогает преобразовать разрозненные сигналы в координированное ремоделирование, эффективно обрезающее нежелательные участки сосудов.
Клетки в переходном состоянии между двумя идентичностями
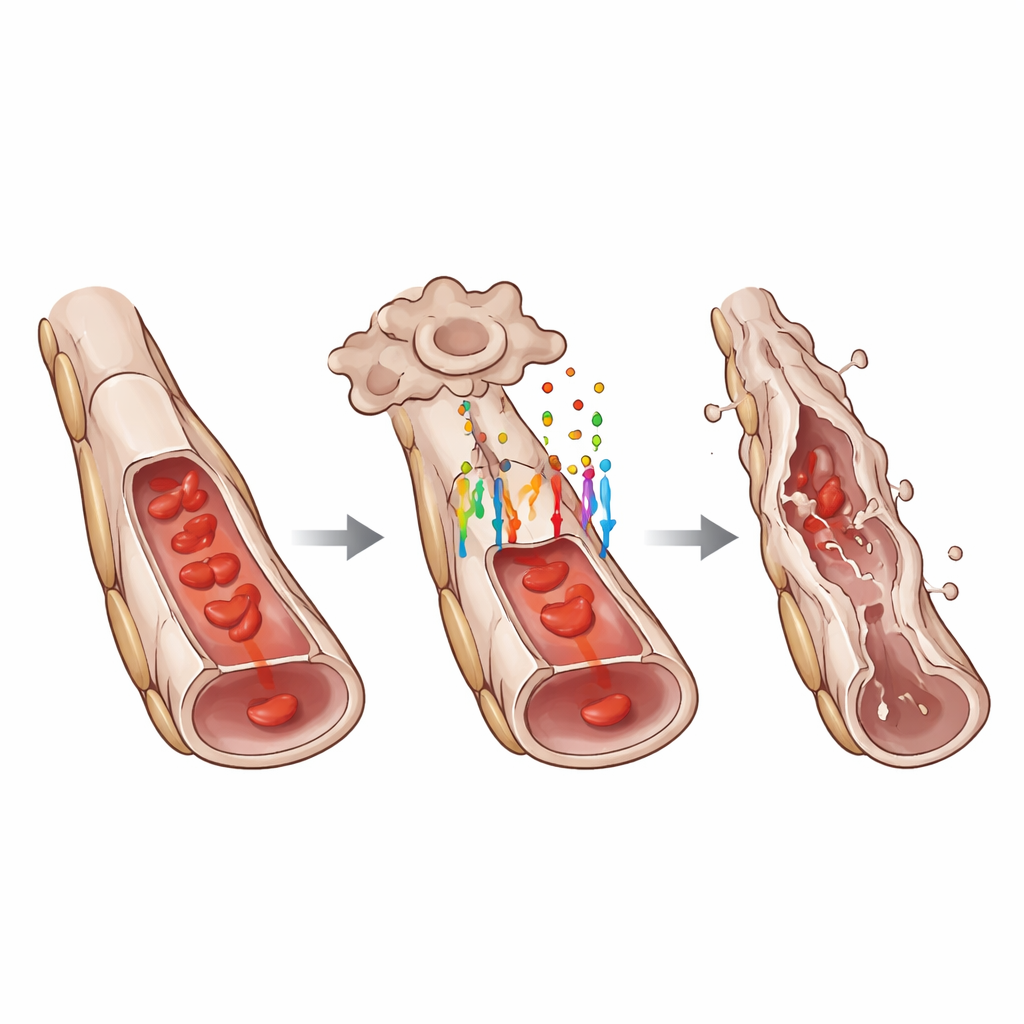
Углубляясь, команда использовала секвенирование РНК одиночных клеток, чтобы профилировать отдельные клетки из гиалоидной сети. Они обнаружили, что эндотелиальные клетки с интактным GPR124 демонстрировали профиль экспрессии генов, соответствующий частичному эндотелиально‑мезенхимальному переходу — состоянию, при котором клетки начинают терять некоторые характерные эндотелиальные признаки и приобретать свойства более подвижных, матриксообразующих клеток. Классические эндотелиальные маркёры, такие как VE‑кадгерин и фактор фон Виллебранда, были снижены, тогда как мезенхимальные маркёры, например ZEB1, повышены. Микроскопия подтвердила эти изменения на белковом уровне. Одновременно несколько генов, способствующих гибели клеток, были более активны в GPR124‑положительных клетках, а гены, связанные с трансформирующим фактором роста бета (TGF‑β), также претерпели изменения. Сопредельные поддерживающие клетки — перициты — демонстрировали вторичные реакции стресса, но тщательное визуализирование показало, что эндотелиальные клетки умирают первыми, затем теряются перициты и в конце остаются пустые «призрачные» нитки базальной мембраны.
Что это значит для здоровья глаза и не только
В сумме результаты ставят GPR124 в центр координации регрессии гиалоидных сосудов. Обеспечивая WNT7‑опосредованный сигнал, GPR124 переводит эндотелиальные клетки в переходное состояние, ослабляет их контакты, подготавливает к апоптозу и помогает организовать поэтапный коллапс и очистку устаревших сосудов, при этом рост сосудов сетчатки остаётся в основном нетронутым. Понимание этой тонко настроенной программы проливает свет на то, как развивающийся глаз перестраивает сам себя, и выделяет потенциальные молекулярные мишени для лечения расстройств, при которых временные сосуды отказываются исчезать. Похожие GPR124‑зависимые переходы могут формировать облегченную «обрезку» сосудов в других органах, что указывает на более широкую значимость для нормального развития и для заболеваний, сопровождающихся патологическим сохранением сосудов или образованием рубцовой ткани.
Цитирование: Hannig, L., Heiden, R., Ergün, S. et al. GPR124 regulates hyaloid blood vessel regression and is associated with endothelial-mesenchymal transition. Sci Rep 16, 13765 (2026). https://doi.org/10.1038/s41598-026-50835-1
Ключевые слова: развитие глаза, регрессия кровеносных сосудов, Wnt‑сигналинг, GPR124, эндотелиальный переход