Clear Sky Science · pl
GPR124 reguluje regresję naczyń krwionośnych ciała szklistkowego i wiąże się z przejściem śródbłonkowo-mezenchymalnym
Dlaczego maleńkie naczynia oka muszą zniknąć
Przed narodzinami wnętrze oka jest oplecione tymczasową siecią naczyń krwionośnych, które odżywiają rosnącą soczewkę i otaczające tkanki. Dla ostrego widzenia w późniejszym życiu ta rusztowanie musi zniknąć we właściwym czasie i zostać zastąpione przez stałe krążenie siatkówkowe. Gdy to sprzątanie się nie udaje, u dzieci mogą wystąpić poważne problemy okulistyczne, w tym odwarstwienie siatkówki i ślepota. W tym badaniu zadano podstawowe, lecz kluczowe pytanie: jakie sygnały molekularne informują te tymczasowe naczynia, kiedy i w jaki sposób mają zniknąć?
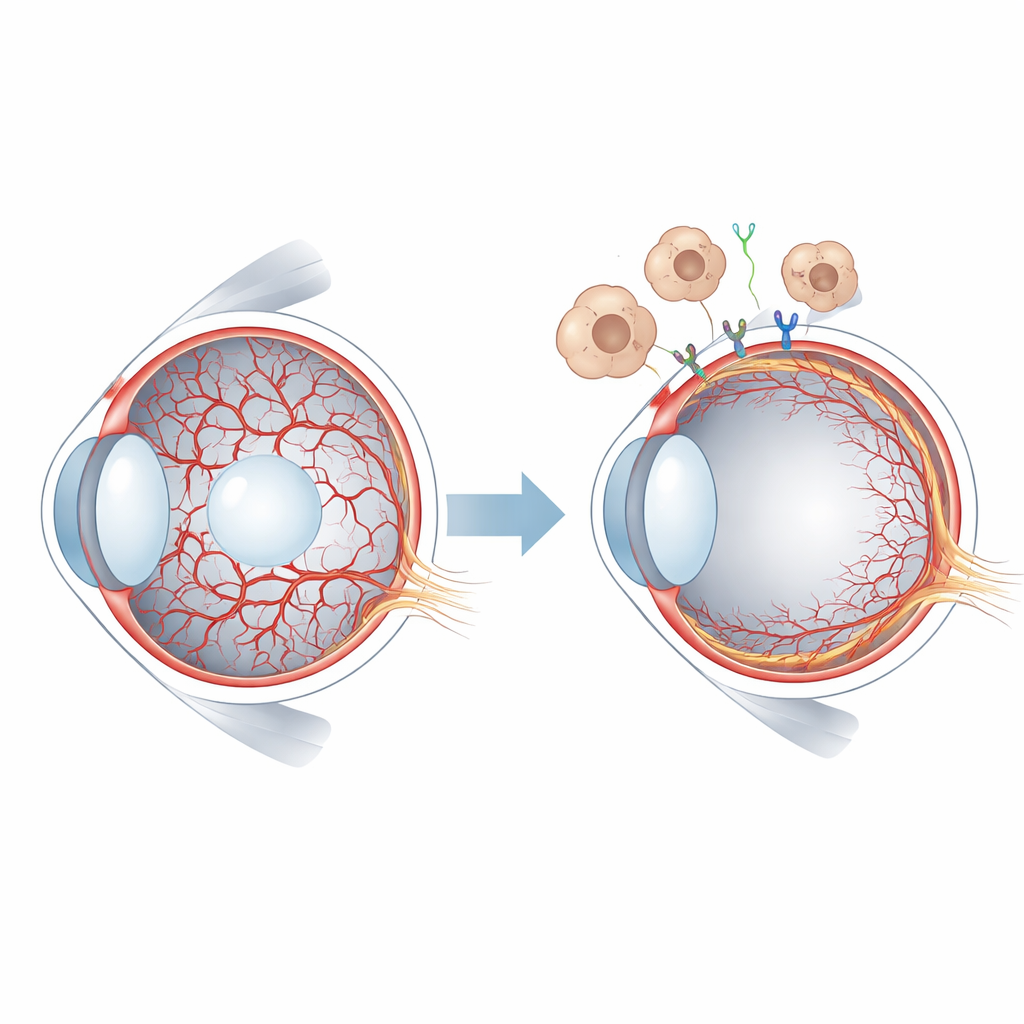
Krótko żywiące naczynia w młodym oku
U ssaków wczesne tkanki oka są odżywiane przez naczynia ciała szklistkowego (hyaloid), delikatną sieć rozciągającą się przez żelopodobne centrum oka i obejmującą soczewkę. W miarę jak siatkówka zaczyna tworzyć własne unaczynienie, system hyaloid musi się cofnąć i zostać usunięty. U ludzi dzieje się to przed urodzeniem, natomiast u myszy odbywa się po porodzie, co daje wygodne okno do badań eksperymentalnych. Gdy naczynia hyaloid utrzymują się, jak w stanie zwanym uporczywą hiperplastyczną wtórną ciałem szklistym (persistent hyperplastic primary vitreous), widzenie może być poważnie zaburzone. Naukowcy wiedzieli już, że rodzina sygnałów zwana WNT, a w szczególności białko WNT7B uwalniane przez komórki odpornościowe zwane makrofagami, pomaga inicjować regresję naczyń hyaloid. Jednak konkretne receptory na komórkach naczyń oraz dalsze wydarzenia wewnątrzkomórkowe nie były dobrze poznane.
Wyznaczenie kluczowego molekularnego strażnika
Zespół skupił się na GPR124, białku przypominającym receptor, znanym jako koreceptor dla WNT7A i WNT7B w rozwijającym się mózgu, gdzie sprzyja wzrostowi naczyń i tworzeniu bariery krew–mózg. Stworzyli myszy, w których GPR124 można było usunąć specyficznie w komórkach śródbłonka — komórkach wyścielających naczynia krwionośne — krótko po urodzeniu. Kiedy GPR124 został usunięty z komórek śródbłonka hyaloid, centralne naczynia oka cofały się znacznie wolniej niż u normalnych miotów. Sieć hyaloid pozostawała gęstsza przez dłuższy czas, mimo że ten sam sygnał wydawał się zbędny do budowy naczyń siatkówki wzdłuż wewnętrznej powierzchni oka. Ten efekt specyficzny dla przedziału pokazuje, że GPR124 jest kluczowy dla demontażu tymczasowego krążenia hyaloid, ale w dużej mierze niezbędny przy tworzeniu stałej sieci siatkówkowej.
Jak sygnał przebudowuje i usuwa naczynia
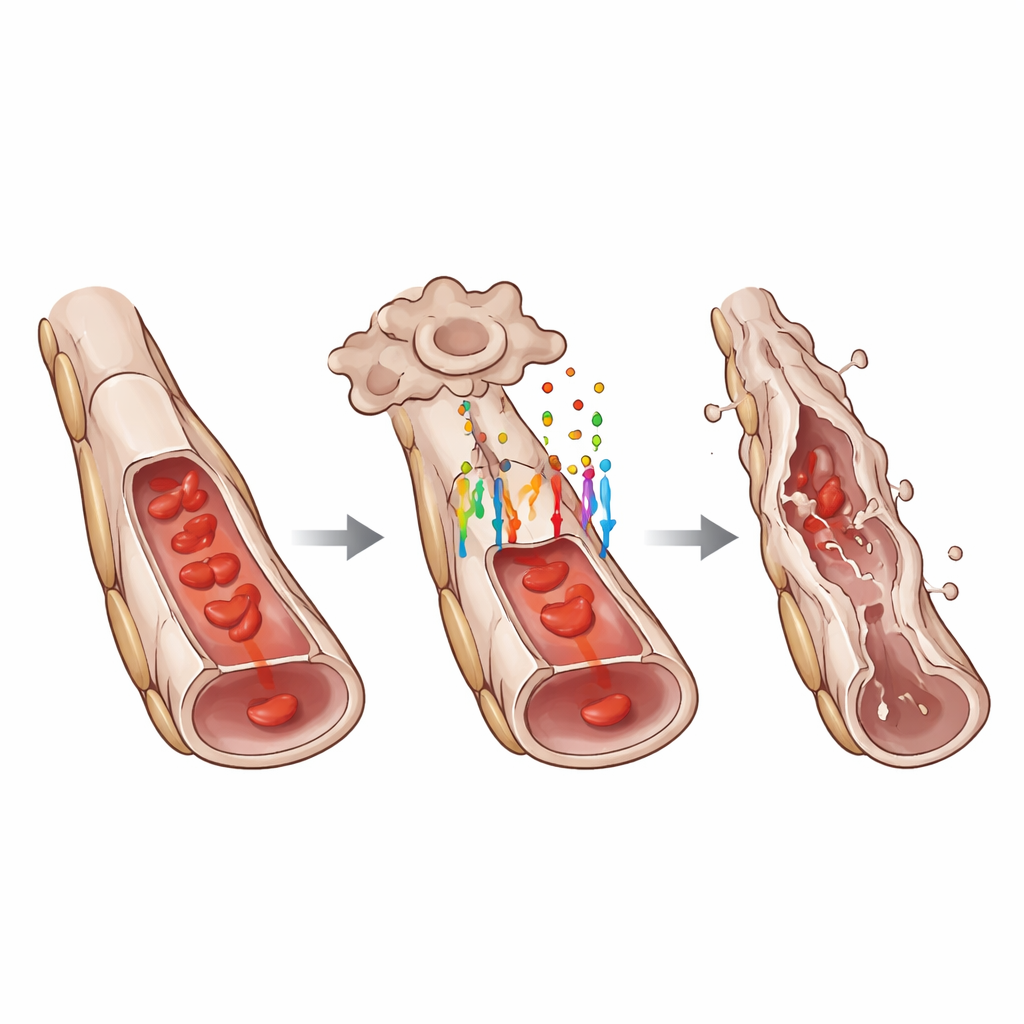
Aby zrozumieć, jak GPR124 wpływa na zachowanie komórek, badacze zmierzyli aktywność genów docelowych WNT w naczyniach hyaloid. Stwierdzili, że utrata GPR124 wyraźnie zmniejszała poziomy jądrowe LEF1 i innych klasycznych białek reagujących na WNT, co wskazuje na stłumienie ścieżki WNT/β-katenina. Jednak GPR124 nie kontrolował wszystkich form śmierci komórkowej. Liczba pojedynczych umierających komórek śródbłonka wzdłuż inaczej nienaruszonych naczyń była podobna z GPR124 i bez niego. Zamiast tego GPR124 był wymagany do skoordynowanej „segmentalnej” regresji, w której ciągi sąsiednich komórek śródbłonka wzdłuż odcinka naczynia umierają razem, powodując zapadnięcie się rurki. Ten wzorzec sugeruje, że GPR124 pomaga przekształcić rozproszone sygnały w zorganizowane zdarzenie przebudowy, które efektywnie usuwa niepożądane odcinki naczyń.
Komórki w przejściu między dwiema tożsamościami
Pogłębiając badanie, zespół użył sekwencjonowania RNA pojedynczych komórek, by scharakteryzować poszczególne komórki z sieci hyaloid. Odkryli, że komórki śródbłonka z zachowanym GPR124 wykazywały wzór ekspresji genów zgodny z częściowym przejściem śródbłonkowo-mezenchymalnym — stanem, w którym zaczynają tracić niektóre cechy charakterystyczne dla śródbłonka, jednocześnie nabywając cechy komórek bardziej ruchomych i produkujących macierz. Klasyczne markery śródbłonka, takie jak VE-kadheryna i czynnik von Willebranda, były zmniejszone, natomiast markery mezenchymalne, jak ZEB1, wzrastały. Mikroskopia potwierdziła te zmiany na poziomie białek. Równocześnie kilka genów promujących śmierć komórkową było bardziej aktywnych w komórkach pozytywnych na GPR124, a geny związane z transformującym czynnikiem wzrostu beta (TGF-β), inną kluczową ścieżką rozwojową, także ulegały zmianom. Sąsiednie komórki podporowe zwane perycytami wykazywały wtórne reakcje stresowe, lecz staranne obrazowanie wskazało, że najpierw umierały komórki śródbłonka, a później następowała utrata perycytów i ostatecznie puste „dusze” włókien błony podstawnej.
Co to znaczy dla zdrowia oka i nie tylko
W sumie wyniki lokują GPR124 jako centralnego koordynatora regresji naczyń hyaloid. Dzięki umożliwieniu sygnalizacji napędzanej przez WNT7, GPR124 popycha komórki śródbłonka w stan przejściowy, rozluźnia ich połączenia, przygotowuje je do apoptozy i pomaga orkiestracyjnie przeprowadzić stopniowe zapadanie się i sprzątanie przestarzałych naczyń, pozostawiając przy tym wzrost naczyń siatkówkowych w dużej mierze nienaruszony. Zrozumienie tego precyzyjnie wyregulowanego programu daje wgląd w to, jak rozwijające się oko przebudowuje się samo i wskazuje potencjalne cele molekularne do leczenia zaburzeń, w których tymczasowe naczynia odmawiają ustąpienia. Podobne przejścia zależne od GPR124 mogą kształtować przycinanie naczyń w innych narządach, sugerując szersze znaczenie dla normalnego rozwoju oraz chorób charakteryzujących się nieprawidłową utrzymaniem naczyń lub bliznowaceniem.
Cytowanie: Hannig, L., Heiden, R., Ergün, S. et al. GPR124 regulates hyaloid blood vessel regression and is associated with endothelial-mesenchymal transition. Sci Rep 16, 13765 (2026). https://doi.org/10.1038/s41598-026-50835-1
Słowa kluczowe: rozwój oka, regresja naczyń krwionośnych, sygnalizacja Wnt, GPR124, przejście śródbłonkowe