Clear Sky Science · es
GPR124 regula la regresión de los vasos sanguíneos hialoideos y se asocia con la transición endotelio-mesenquimal
Por qué deben desaparecer los diminutos vasos del ojo
Antes del nacimiento, el interior del ojo está atravesado por una red temporal de vasos sanguíneos que nutre al cristalino en crecimiento y a los tejidos circundantes. Para obtener una visión nítida más adelante en la vida, este andamiaje debe desaparecer en el momento oportuno y ser reemplazado por la circulación retiniana permanente. Cuando esta limpieza falla, los niños pueden desarrollar problemas oculares graves, incluyendo desprendimiento de retina y ceguera. Este estudio plantea una pregunta básica pero crucial: ¿qué señales moleculares indican a esos vasos temporales cuándo y cómo deben desaparecer?
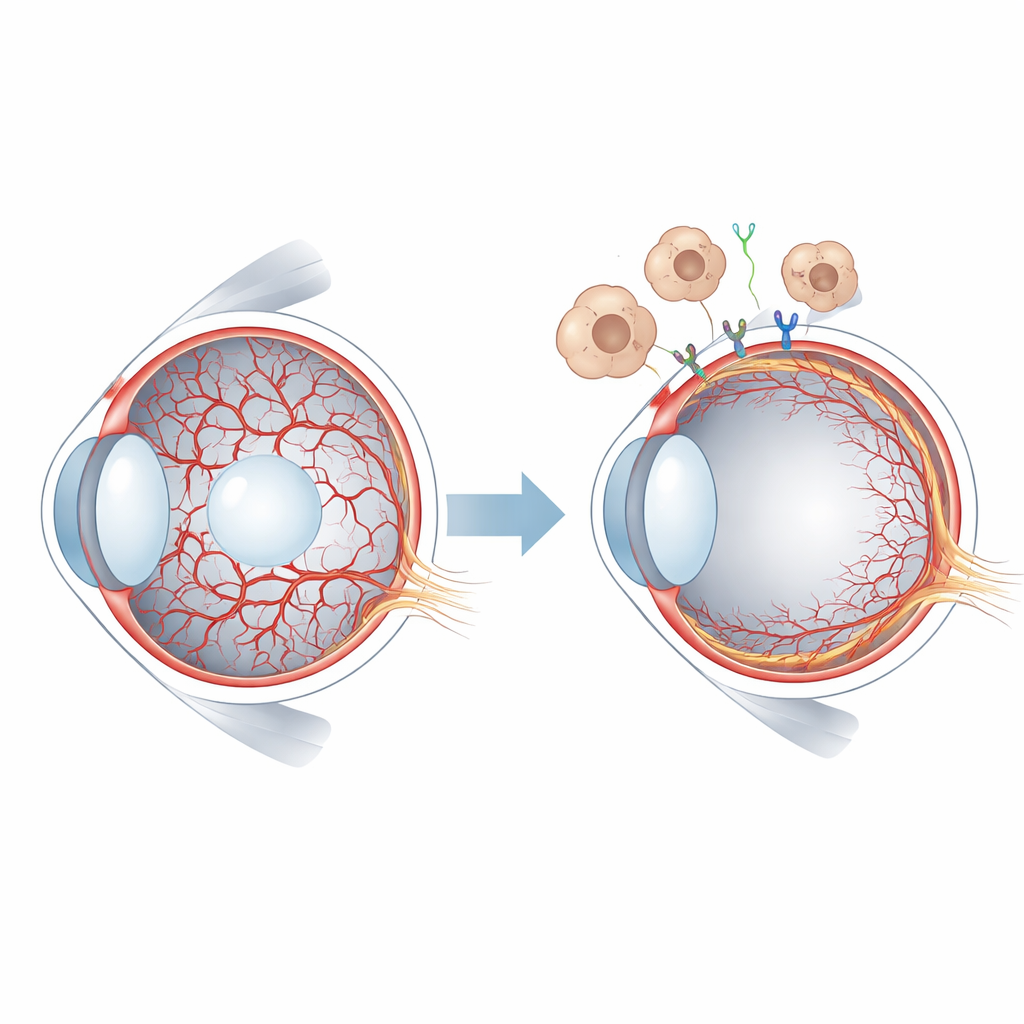
Un suministro sanguíneo efímero en el ojo joven
En los mamíferos, los tejidos oculares tempranos son nutridos por los vasos hialoideos, una red delicada que atraviesa el centro gelatinoso del ojo y rodea el cristalino. A medida que la retina comienza a formar su propia circulación, el sistema hialoideo debe regresionar y despejarse. En humanos esto ocurre antes del nacimiento, mientras que en ratones se desarrolla después del nacimiento, lo que ofrece una ventana conveniente para el estudio experimental. Cuando los vasos hialoideos persisten, como en una condición llamada vítreo primario hiperplásico persistente, la visión puede verse gravemente comprometida. Los investigadores ya sabían que una familia de señales llamada WNT, y en particular la proteína WNT7B liberada por células inmunitarias llamadas macrófagos, ayuda a desencadenar la regresión de los vasos hialoideos. Pero los receptores específicos en las células vasculares y los eventos a valle no se comprendían bien.
Señalando a un guardián molecular clave
El equipo se centró en GPR124, una proteína tipo receptor conocida por actuar como co-receptor de WNT7A y WNT7B en el cerebro en desarrollo, donde promueve el crecimiento vascular y la formación de la barrera hematoencefálica. Diseñaron ratones en los que GPR124 podía eliminarse específicamente en células endoteliales—las células que recubren los vasos—poco después del nacimiento. Cuando se eliminó GPR124 de las células endoteliales hialoideas, los vasos centrales del ojo regresionaron mucho más lentamente que en las crías normales. La red hialoidea permaneció más densa durante más tiempo, aunque la misma señal pareció innecesaria para formar los vasos retinianos a lo largo de la superficie interna del ojo. Este efecto específico de compartimento muestra que GPR124 es crítico para desmantelar la circulación hialoidea temporal pero, en gran medida, prescindible para la construcción de la red retiniana permanente.
Cómo la señal remodela y elimina los vasos
Para entender cómo GPR124 influye en el comportamiento celular, los investigadores midieron la actividad de genes diana de WNT en los vasos hialoideos. Encontraron que la pérdida de GPR124 redujo notablemente los niveles nucleares de LEF1 y de otras proteínas clásicamente respon-sivas a WNT, lo que indica una vía WNT/β-catenina atenuada. Sin embargo, GPR124 no controlaba todas las formas de muerte celular. El número de células endoteliales aisladas muriendo a lo largo de vasos por lo demás intactos fue similar con o sin GPR124. En cambio, GPR124 era necesario para la regresión coordinada “segmentaria”, en la que hileras de células endoteliales vecinas a lo largo de un segmento vascular morían juntas, provocando el colapso del tubo. Este patrón sugiere que GPR124 ayuda a convertir señales dispersas en un evento de remodelado concertado que poda de manera eficaz secciones vasculares no deseadas.
Células en transición entre dos identidades
Profundizando más, el equipo usó secuenciación de ARN a célula única para perfilar células individuales de la red hialoidea. Descubrieron que las células endoteliales con GPR124 intacto mostraban un patrón de expresión génica consistente con una transición parcial endotelio‑a‑mesenquimal, un estado en el que empiezan a perder algunas características endoteliales distintivas mientras adquieren rasgos asociados con células más móviles y productoras de matriz. Marcadores endoteliales clásicos como VE‑cadherina y el factor von Willebrand se redujeron, mientras que marcadores mesenquimales como ZEB1 aumentaron. La microscopía confirmó estos cambios a nivel proteico. Al mismo tiempo, varios genes que promueven la muerte celular estaban más activos en las células positivas para GPR124, y genes vinculados al factor de crecimiento transformante beta, otra vía mayor del desarrollo, también se alteraron. Las células de soporte vecinas llamadas pericitos mostraron respuestas secundarias de estrés, pero imágenes detalladas indicaron que las células endoteliales morían primero, seguidas más tarde por la pérdida de pericitos y, finalmente, por hilos vacíos o “fantasma” de membrana basal.
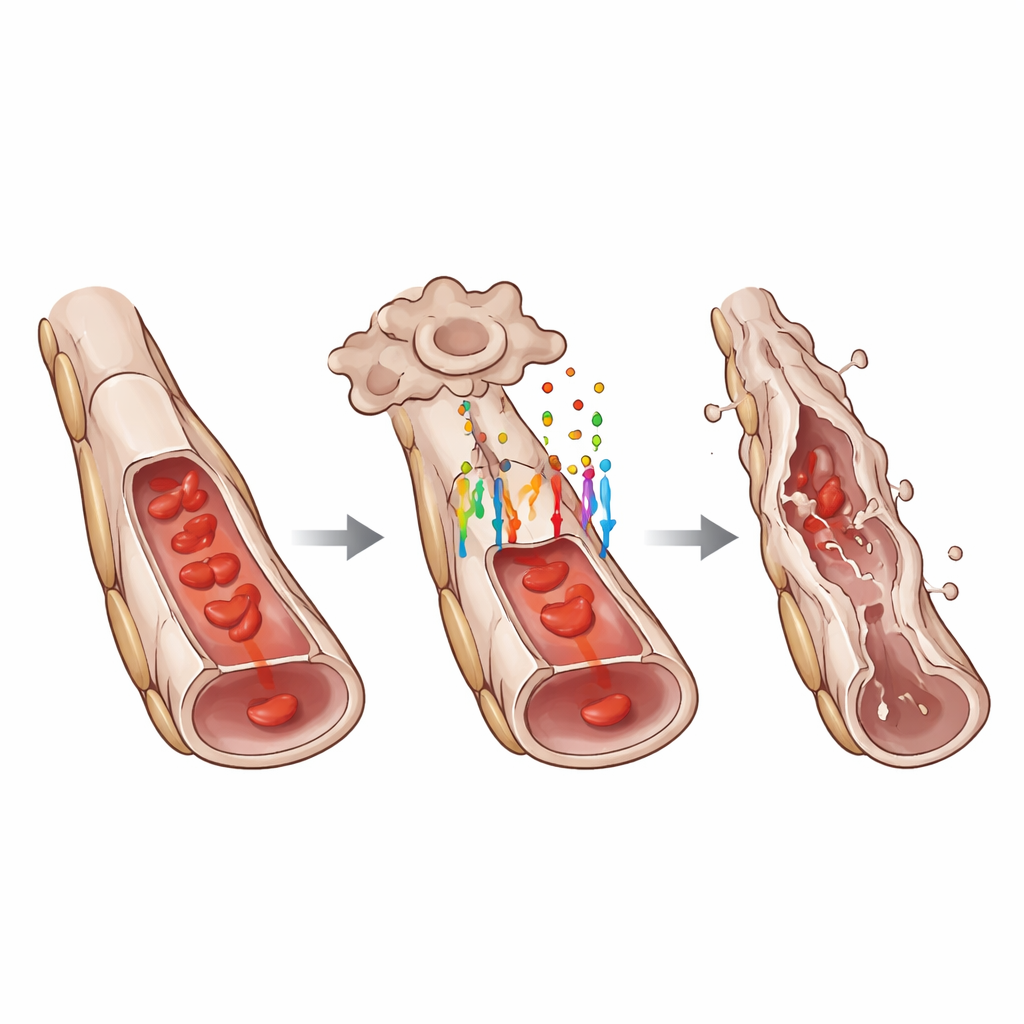
Qué significa esto para la salud ocular y más allá
En conjunto, los hallazgos sitúan a GPR124 como un coordinador central de la regresión de los vasos hialoideos. Al posibilitar la señalización impulsada por WNT7, GPR124 empuja a las células endoteliales hacia un estado transicional, afloja sus uniones, las prepara para la apoptosis y ayuda a orquestar el colapso y la limpieza escalonada de vasos obsoletos, todo ello sin afectar en gran medida el crecimiento de los vasos retinianos. Comprender este programa finamente afinado ofrece perspectivas sobre cómo el ojo en desarrollo se remodela a sí mismo y resalta posibles dianas moleculares para tratar trastornos en los que los vasos temporales se niegan a desaparecer. Transiciones dependientes de GPR124 similares podrían moldear la poda vascular en otros órganos, lo que sugiere una relevancia más amplia para el desarrollo normal y para enfermedades caracterizadas por persistencia vascular anómala o cicatrización.
Cita: Hannig, L., Heiden, R., Ergün, S. et al. GPR124 regulates hyaloid blood vessel regression and is associated with endothelial-mesenchymal transition. Sci Rep 16, 13765 (2026). https://doi.org/10.1038/s41598-026-50835-1
Palabras clave: desarrollo ocular, regresión de vasos sanguíneos, señalización Wnt, GPR124, transición endotelial