Clear Sky Science · pt
GPR124 regula a regressão dos vasos sanguíneos hialoides e está associado à transição endotelial-mesenquimal
Por que pequenos vasos oculares precisam desaparecer
Antes do nascimento, o interior do olho é atravessado por uma teia temporária de vasos sanguíneos que nutrem o cristalino em crescimento e os tecidos circundantes. Para que a visão fique nítida mais adiante na vida, essa estrutura de suporte deve desaparecer no momento certo e ser substituída pela circulação permanente da retina. Quando essa limpeza falha, crianças podem desenvolver problemas oculares graves, incluindo descolamento de retina e cegueira. Este estudo faz uma pergunta básica, porém crucial: quais sinais moleculares dizem a esses vasos temporários quando e como desaparecer?
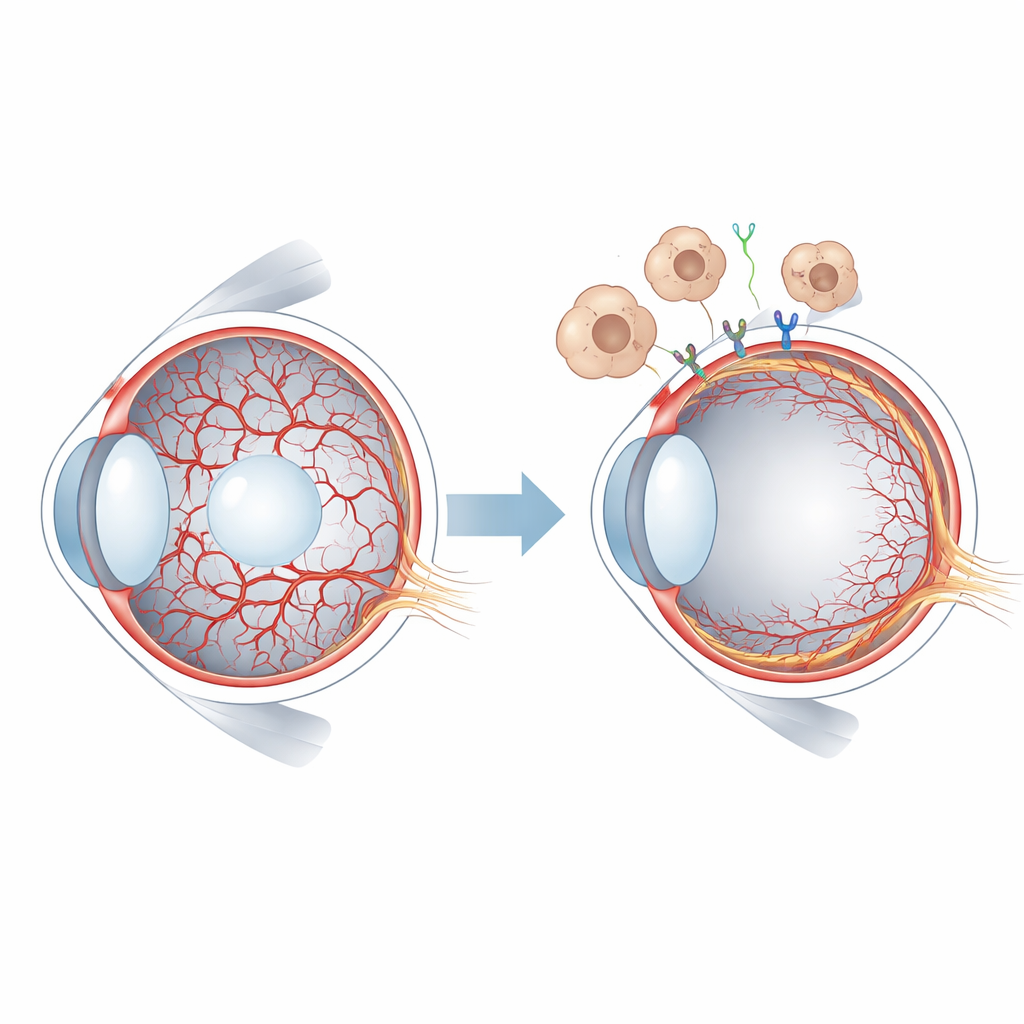
Um suprimento sanguíneo de curta duração no olho jovem
Em mamíferos, os tecidos oculares iniciais são nutridos pelos vasos hialoides, uma rede delicada que atravessa o centro gelatinoso do olho e envolve o cristalino. À medida que a retina começa a formar sua própria circulação, o sistema hialoide precisa regredir e ser eliminado. No ser humano isso ocorre antes do nascimento, enquanto em camundongos se desenrola após o nascimento, oferecendo uma janela conveniente para estudo experimental. Quando os vasos hialoides persistem, como na condição chamada vítreo primário hiperplásico persistente, a visão pode ser severamente comprometida. Pesquisadores já sabiam que uma família de sinais chamada WNT, e em particular a proteína WNT7B liberada por células imunes chamadas macrófagos, ajuda a desencadear a regressão dos vasos hialoides. Mas os receptores específicos nas células vasculares e os eventos a jusante não eram bem compreendidos.
Localizando um importante guardião molecular
A equipe concentrou-se em GPR124, uma proteína com aparência de receptor conhecida por atuar como co-receptor para WNT7A e WNT7B no cérebro em desenvolvimento, onde promove o crescimento vascular e a formação da barreira hematoencefálica. Eles criaram camundongos nos quais GPR124 podia ser deletado especificamente em células endoteliais — as células que revestem os vasos sanguíneos — logo após o nascimento. Quando GPR124 foi removido das células endoteliais hialoides, os vasos centrais do olho regrediram muito mais lentamente do que em irmãos normais. A rede hialoide permaneceu mais densa por mais tempo, embora o mesmo sinal parecesse desnecessário para construir os vasos retinais ao longo da superfície interna do olho. Esse efeito específico por compartimento mostra que GPR124 é crítico para desmontar a circulação hialoide temporária, mas em grande parte dispensável para a construção da rede retiniana permanente.
Como o sinal remodela e remove vasos
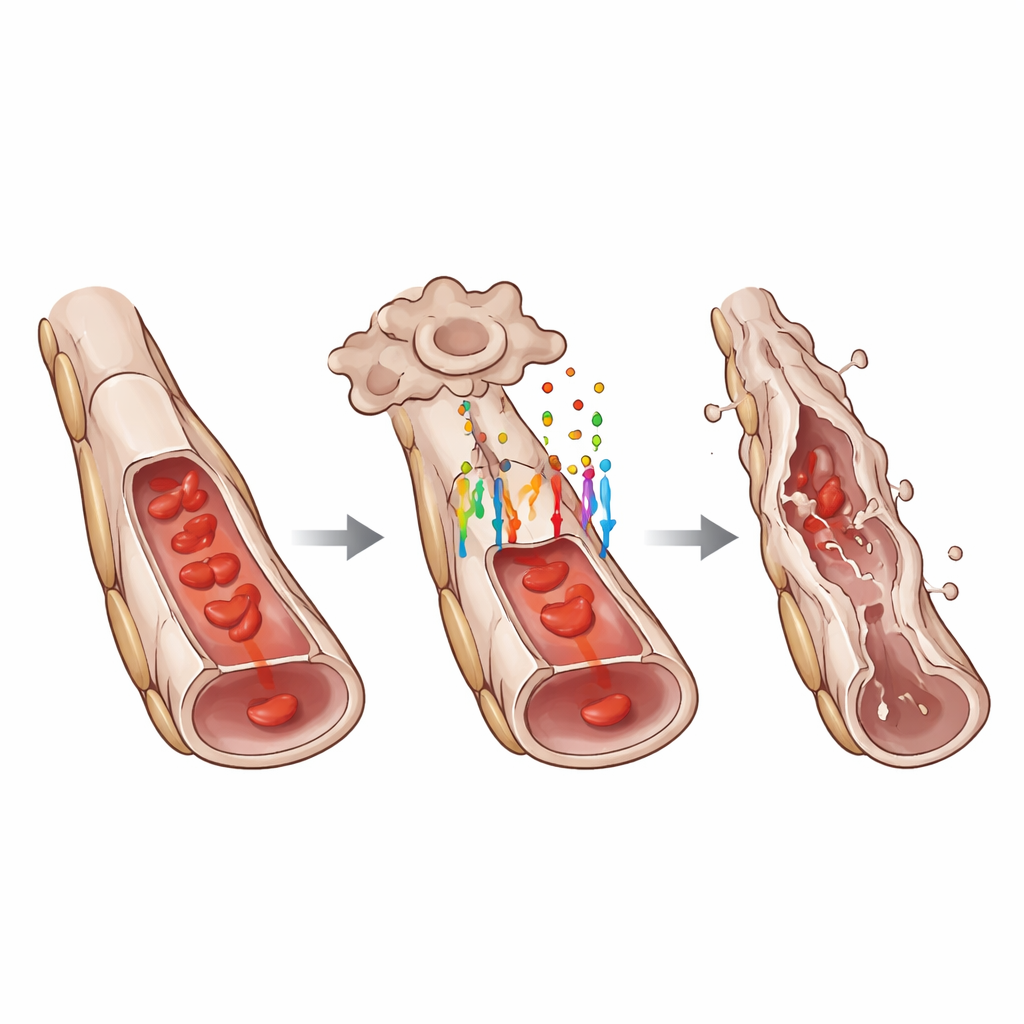
Para entender como GPR124 influencia o comportamento celular, os pesquisadores mediram a atividade de genes-alvo da via WNT nos vasos hialoides. Eles descobriram que a perda de GPR124 reduziu marcadamente os níveis nucleares de LEF1 e outras proteínas clássicas responsivas à WNT, indicando uma via WNT/β-catenina atenuada. Ainda assim, GPR124 não controlou todas as formas de morte celular. O número de células endoteliais moribundas isoladas ao longo de vasos aparentemente intactos foi semelhante com ou sem GPR124. Em vez disso, GPR124 foi necessário para a regressão “segmentar” coordenada, em que sequências de células endoteliais vizinhas ao longo de um segmento vascular morrem em conjunto, fazendo com que o tubo colapse. Esse padrão sugere que GPR124 ajuda a converter sinais dispersos em um evento de remodelagem concertado que poda de forma eficiente seções vasculares indesejadas.
Células em transição entre duas identidades
Aprofundando, a equipe usou sequenciamento de RNA de célula única para perfilar células individuais da rede hialoide. Eles descobriram que células endoteliais com GPR124 intacto exibiam um padrão de expressão gênica consistente com uma transição parcial de endotélio para mesênquima, um estado no qual começam a perder algumas características endoteliais marcantes enquanto ganham traços associados a células mais móveis e produtoras de matriz. Marcadores endoteliais clássicos, como VE-caderina e fator von Willebrand, foram reduzidos, enquanto marcadores mesenquimais como ZEB1 aumentaram. A microscopia confirmou essas mudanças ao nível proteico. Ao mesmo tempo, vários genes promotores da morte celular estavam mais ativos em células positivas para GPR124, e genes ligados ao transformador de crescimento beta (TGF-β), outra via importante no desenvolvimento, também foram alterados. Células de suporte vizinhas chamadas pericitos mostraram respostas secundárias de estresse, mas imagens cuidadosas indicaram que as células endoteliais morriam primeiro, seguidas mais tarde pela perda de pericitos e, finalmente, por fios vazios — “fantasmas” — de membrana basal.
O que isso significa para a saúde ocular e além
No conjunto, os achados posicionam GPR124 como um coordenador central da regressão dos vasos hialoides. Ao permitir a sinalização dirigida por WNT7, GPR124 empurra as células endoteliais para um estado transitório, afrouxa suas junções, as prepara para apoptose e ajuda a orquestrar o colapso e a limpeza em etapas dos vasos obsoletos, enquanto deixa o crescimento dos vasos da retina em grande parte intacto. Compreender esse programa finamente ajustado oferece insights sobre como o olho em desenvolvimento se remodela e destaca potenciais alvos moleculares para tratar distúrbios em que vasos temporários se recusam a desaparecer. Transições dependentes de GPR124 semelhantes podem moldar a poda vascular em outros órgãos, sugerindo relevância mais ampla para o desenvolvimento normal e para doenças marcadas por persistência anormal de vasos ou cicatrização.
Citação: Hannig, L., Heiden, R., Ergün, S. et al. GPR124 regulates hyaloid blood vessel regression and is associated with endothelial-mesenchymal transition. Sci Rep 16, 13765 (2026). https://doi.org/10.1038/s41598-026-50835-1
Palavras-chave: desenvolvimento ocular, regressão de vasos sanguíneos, sinalização Wnt, GPR124, transição endotelial