Clear Sky Science · ar
GPR124 ينظّم تراجع الأوعية الدموية الهيالوية ويرتبط بالتحول البطاني-الmezنخي
لماذا يجب أن تختفي الأوعية الصغيرة في العين
قبل الولادة، يكون داخل العين محاطًا بشبكة مؤقتة من الأوعية الدموية تغذي العدسة والنسيج المحيط بها أثناء نموهما. من أجل رؤية حادة لاحقًا، لا بد لهذه البنية الداعمة أن تختفي في الوقت المناسب وتستبدل بالدورة الدموية الشبكية الدائمة. عندما يفشل هذا التنظيف، قد يصاب الأطفال بمشكلات بصرية خطيرة، بما في ذلك انفصال الشبكية والعمى. تطرح هذه الدراسة سؤالًا أساسيًا لكنه حاسم: ما الإشارات الجزيئية التي تخبر هذه الأوعية المؤقتة متى وكيف تختفي؟
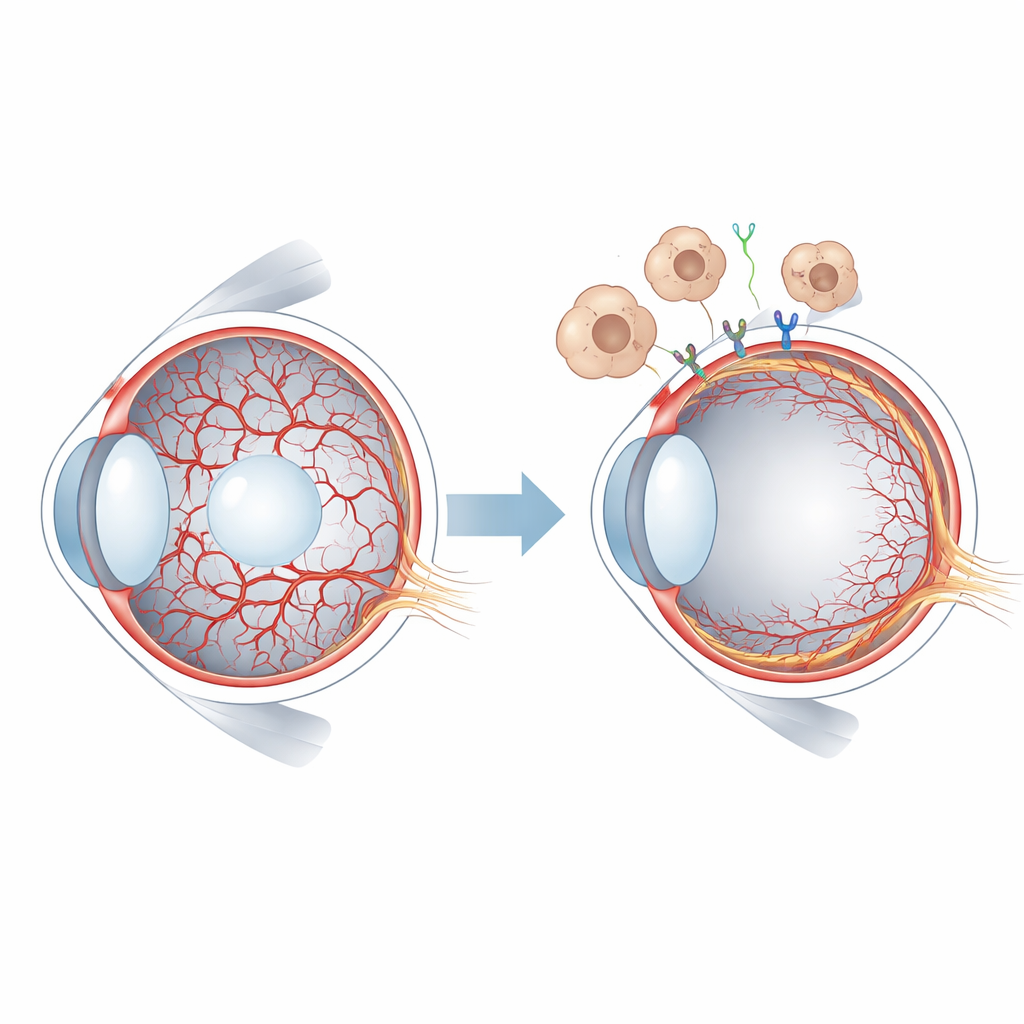
إمداد دموي قصير العمر في عين الصغير
في الثدييات، يغذي الأنسجة العينية المبكرة أوعية الهيالوس، وهي شبكة دقيقة تمتد عبر مركز العين الهلامي وتلتف حول العدسة. عندما تبدأ الشبكية في بناء إمدادها الدموي الخاص، يجب أن تتراجع منظومة الهيالوس وتنكشف. عند البشر يحدث ذلك قبل الولادة، بينما في الفئران يتكشف بعد الولادة، ما يوفر نافذة مناسبة للدراسة التجريبية. عندما تستمر أوعية الهيالوس، كما في حالة تسمى الزجاجي الأولي المفرط الخلقي المستمر، قد تتدهور الرؤية بشدة. كان الباحثون يعلمون سابقًا أن عائلة إشارات تسمى WNT، وبشكل خاص البروتين WNT7B الذي تفرزه الخلايا المناعية المسماة البلعميات، تساعد في تحفيز تراجع أوعية الهيالوس. لكن المستقبلات المحددة على خلايا الأوعية الدموية والأحداث التالية لم تكن مفهومة جيدًا.
تحديد بواب جزيئي رئيسي
ركز الفريق على GPR124، بروتين شبيه بالمستقبل معروف بعمله كمتعاون مستقبل لـ WNT7A وWNT7B في الدماغ النامي، حيث يعزّز نمو الأوعية وتكوين الحاجز الدماغي-الدموي. صنعوا فئرانًا معدّلة يمكن حذف GPR124 فيها تحديدًا من الخلايا البطانية—الخلايا التي تبطّن الأوعية الدموية—بعد الولادة بفترة قصيرة. عندما أزيل GPR124 من خلايا البطين الهيالوية، تراجع أوعية مركز العين أبطأ بكثير مقارنةً بنفس العمر الطبيعي. بقيت شبكة الهيالوس أكثر كثافة لفترة أطول، رغم أن نفس الإشارة بدت غير ضرورية لبناء أوعية الشبكية على السطح الداخلي للعين. هذا التأثير الخاص بالحجرة يبيّن أن GPR124 حاسم لتفكيك الدورة الهيالوية المؤقتة لكنه إلى حد كبير غير ضروري لبناء الشبكة الشبكية الدائمة.
كيف تشكّل الإشارة الأوعية وتزيلها
لفهم كيف يؤثر GPR124 في سلوك الخلايا، قاس الباحثون نشاط جينات الهدف التابعة لـ WNT في أوعية الهيالوس. وجدوا أن فقدان GPR124 قلّل بشكل ملحوظ مستويات LEF1 النووية وبروتينات مستجيبة تقليدية لـ WNT الأخرى، مما يشير إلى كبت مسار WNT/β-catenin. ومع ذلك لم يتحكم GPR124 في كل أشكال موت الخلايا. كان عدد الخلايا البطانية الميتة المعزولة على طول أوعية تبدو سليمة مماثلاً مع أو بدون GPR124. بدلًا من ذلك، كان GPR124 مطلوبًا للتراجع «القِطّاعي» المنسق، حيث تموت سلاسل من الخلايا البطانية المجاورة على طول مقطع الوعاء معًا، ما يؤدي إلى انهيار الأنبوب. يشير هذا النمط إلى أن GPR124 يساعد في تحويل إشارات مشتتة إلى حدث إعادة تشكيل منسق يقصّ بكفاءة أجزاء الأوعية غير المرغوب فيها.
خلايا في مرحلة انتقالية بين هويتين
للتعمق أكثر، استخدم الفريق تسلسل RNA أحادي الخلية لتوصيف خلايا فردية من شبكة الهيالوس. اكتشفوا أن الخلايا البطانية التي تحمل GPR124 أظهرت نمطًا تعبيريًا جينيًا يتوافق مع تحول جزئي من بطاني إلى ميزنخي، حالة تبدأ فيها بفقدان بعض الملامح البطانية المميزة بينما تكتسب سمات مرتبطة بخلايا أكثر حركة ومنتجة للمصفوفة. كانت علامات بطانية كلاسيكية مثل VE-cadherin وعامل فون ويليبراند منخفضة، بينما ارتفعت علامات ميزنخية مثل ZEB1. أكدت المجهرية هذه التغيرات على مستوى البروتين. في الوقت نفسه، كانت عدة جينات معززة لموت الخلايا أكثر نشاطًا في الخلايا الإيجابية لـ GPR124، وتغيرت أيضًا جينات مرتبطة بعامل النمو المحول بيتا، وهو مسار تطويري رئيسي آخر. أظهرت الخلايا الداعمة المجاورة المسماة البرسيِّنا استجابات ثانوية للضغط، لكن التصوير الدقيق أشار إلى أن الخلايا البطانية ماتت أولًا، تلتها لاحقًا خسارة البرسيِّنا وفي النهاية خيوط فارغة «شبحية» من غشاء القاعدة.
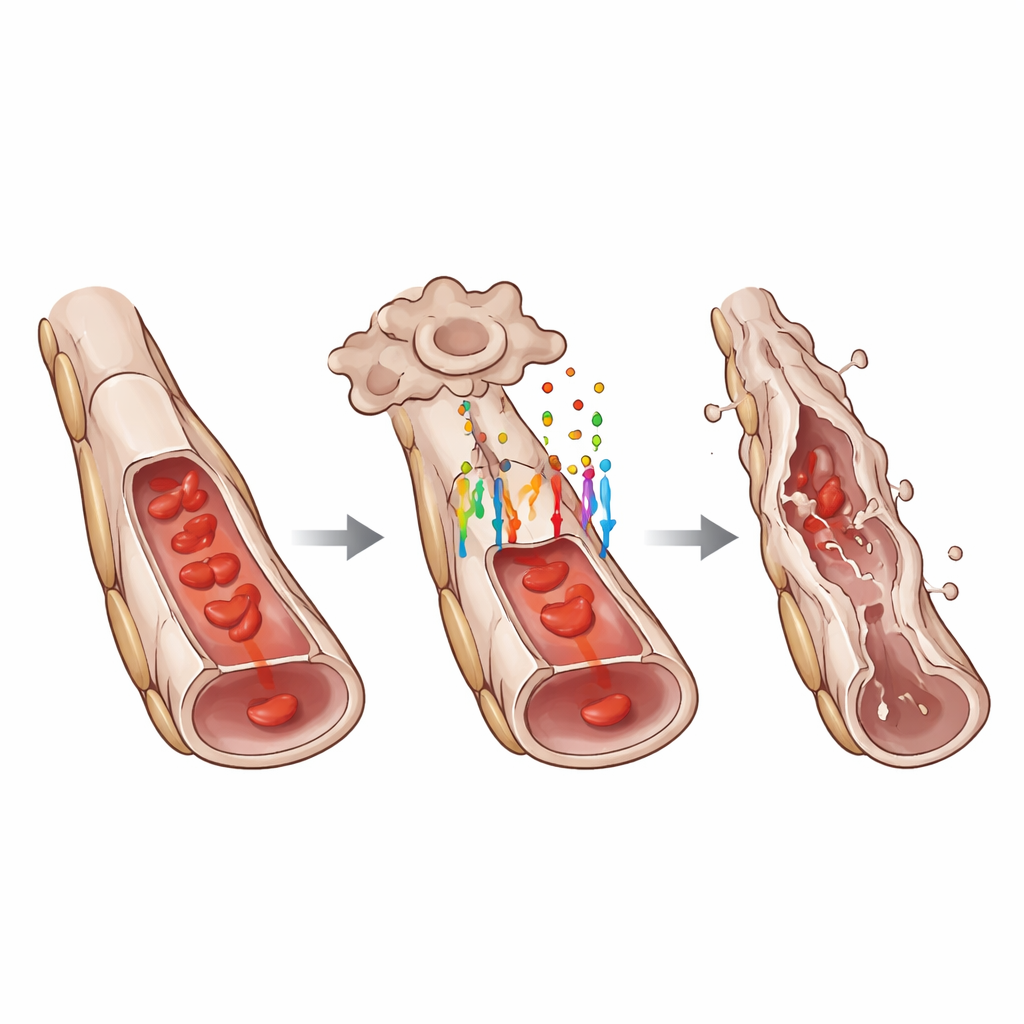
ما دلالته لصحة العين وما بعدها
تضع النتائج مجتمعة GPR124 كمنسق مركزي لتراجع أوعية الهيالوس. من خلال تمكين الإشارات المدفوعة بـ WNT7، يدفع GPR124 الخلايا البطانية إلى حالة انتقالية، يرخّي وصلاتها، يهيئها للموت المبرمج، ويساعد في تنظيم انهيار وتنظيف منظم لقطع الأوعية البالية، كل ذلك مع إبقاء نمو أوعية الشبكية سليمًا إلى حد كبير. يوفر فهم هذا البرنامج الدقيق رؤى حول كيفية إعادة تشكيل العين النامية لنفسها ويبرز أهدافًا جزيئية محتملة لعلاج اضطرابات تبقى فيها الأوعية المؤقتة عالقة. قد تشكل تحولات معتمدة على GPR124 عمليات تقليم الأوعية في أعضاء أخرى أيضًا، مما يشير إلى صلة أوسع بالتطوّر الطبيعي ولأمراض تتصف ببقاء غير طبيعي للأوعية أو التندب.
الاستشهاد: Hannig, L., Heiden, R., Ergün, S. et al. GPR124 regulates hyaloid blood vessel regression and is associated with endothelial-mesenchymal transition. Sci Rep 16, 13765 (2026). https://doi.org/10.1038/s41598-026-50835-1
الكلمات المفتاحية: تطوّر العين, تراجع الأوعية الدموية, إشارة Wnt, GPR124, التحول البطاني