Clear Sky Science · sv
GPR124 reglerar regression av hyaloida blodkärl och är associerat med endotelial-mesenkymal övergång
Varför små kärl i ögat måste försvinna
Före födseln är ögats insida genomsyrad av ett temporärt nätverk av blodkärl som förser den växande linsen och omkringliggande vävnad med näring. För att få skarp syn senare i livet måste denna stomme försvinna i rätt tid och ersättas av den permanenta retinala cirkulationen. När denna städning misslyckas kan barn utveckla allvarliga ögonproblem, inklusive näthinneavlossning och blindhet. Denna studie ställer en grundläggande men avgörande fråga: vilka molekylära signaler talar om för dessa tillfälliga kärl när och hur de ska försvinna?
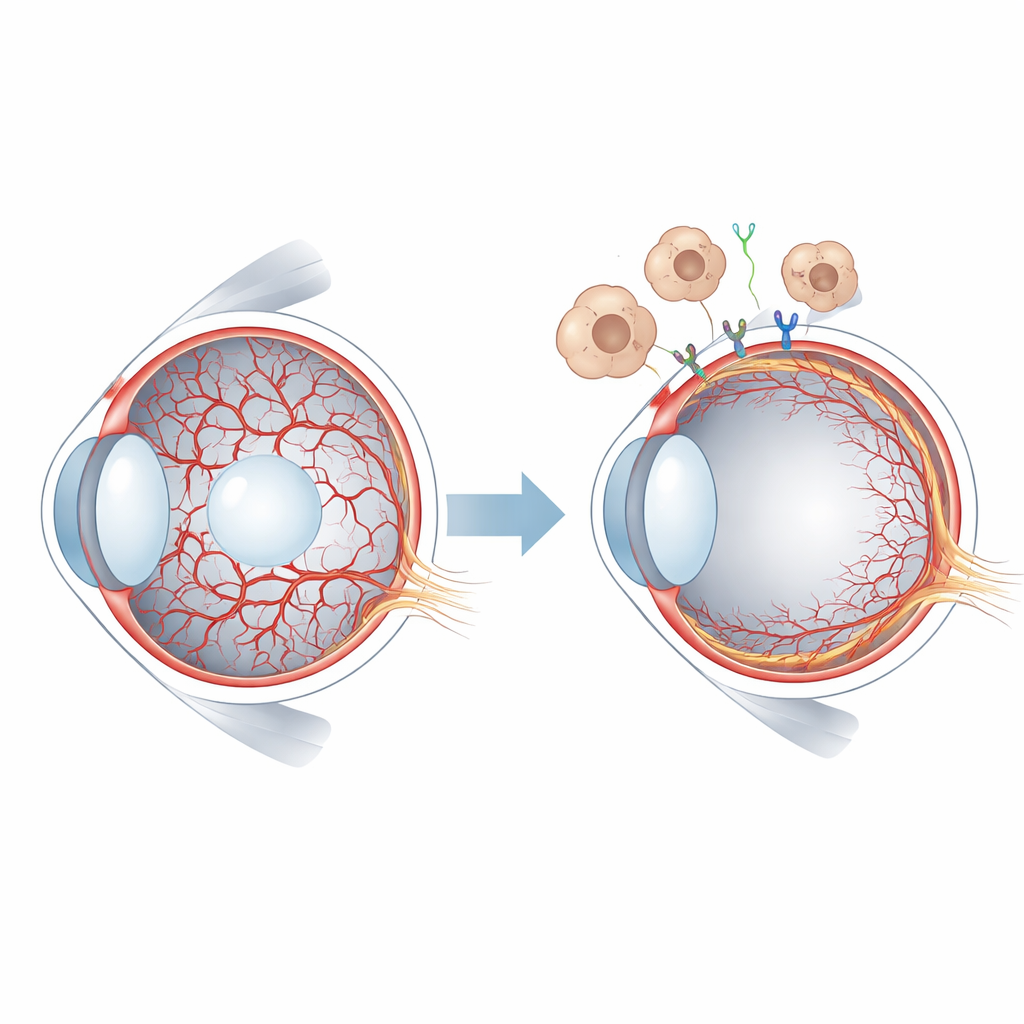
En kortlivad blodförsörjning i det unga ögat
Hos däggdjur försörjs tidig ögonvävnad av de hyaloida kärlen, ett ömtåligt nätverk som sträcker sig genom ögats geléartade mitt och omsluter linsen. När näthinnan börjar bygga sin egen blodförsörjning måste det hyaloida systemet regressera och rensas bort. Hos människor sker detta före födseln, medan det hos möss äger rum efter födseln, vilket ger ett praktiskt fönster för experimentell studie. När hyaloida kärl kvarstår, som i tillståndet persistent hyperplastisk primär glaskropp, kan synen vara allvarligt påverkad. Forskare visste redan att en signalsläkt kallad WNT, särskilt proteinet WNT7B som frisätts av immunceller kallade makrofager, hjälper till att initiera regressionen av hyaloida kärl. Men de specifika receptorerna på blodkärlscellerna och de efterföljande händelserna var inte väl förstådda.
Identifiering av en viktig molekylär grindvakt
Forskargruppen fokuserade på GPR124, ett receptorliknande protein som är känt för att fungera som en co-receptor för WNT7A och WNT7B i den utvecklande hjärnan, där det främjar blodkärlstillväxt och bildandet av blod-hjärnbarriären. De konstruerade möss där GPR124 specifikt kunde tas bort i endotelceller—de celler som bekläder blodkärlen—kort efter födseln. När GPR124 togs bort från hyaloida endotelceller regresserade de centrala ögonkärlen mycket långsammare än hos normala syskon. Det hyaloida nätverket förblev tätare längre, även om samma signal verkade onödig för att bygga de retinala kärlen längs ögats inneryta. Denna compartmentspecifika effekt visar att GPR124 är avgörande för att demontera den temporära hyaloida cirkulationen men i stor utsträckning överflödig för konstruktionen av det permanenta retinala nätverket.
Hur signalen omformar och avlägsnar kärl
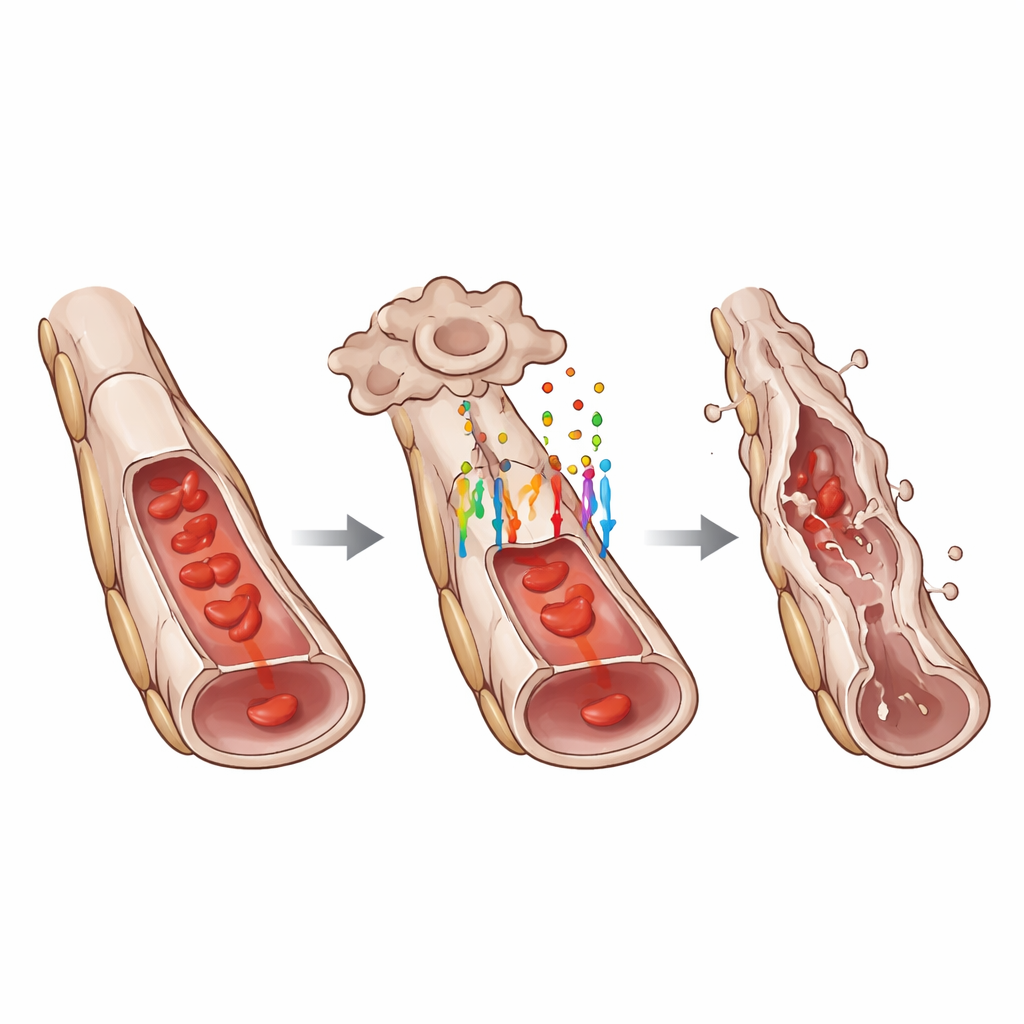
För att förstå hur GPR124 påverkar cellbeteende mätte forskarna aktiviteten hos WNT-målgener i hyaloida kärl. De fann att förlust av GPR124 markant minskade nukleära nivåer av LEF1 och andra klassiska WNT-responsiva proteiner, vilket indikerar en dämpad WNT/β-katenin-väg. Ändå kontrollerade GPR124 inte alla former av celldöd. Antalet isolerade döende endotelceller längs i övrigt intakta kärl var liknande med eller utan GPR124. Istället krävdes GPR124 för koordinerad "segmentell" regression, där rader av närliggande endotelceller längs ett kärlsegment dog samtidigt, vilket orsakade att röret kollapsade. Detta mönster tyder på att GPR124 hjälper till att omvandla utspridda signaler till ett samordnat ombyggnadsevenemang som effektivt gallrar bort oönskade kärlavsnitt.
Celler i övergång mellan två identiteter
För att gå djupare användes enkelcells-RNA-sekvensering för att profilera individuella celler från det hyaloida nätverket. De upptäckte att endotelceller med intakt GPR124 visade ett genuttrycksmönster som stämmer överens med en partiell endotelial-till-mesenkymal övergång, ett tillstånd där de börjar förlora vissa karakteristiska endoteliala egenskaper samtidigt som de får drag som är förknippade med mer rörliga, matrixproducerande celler. Klassiska endotelmarkörer som VE-kadherin och von Willebrand-faktor var reducerade, medan mesenkymala markörer såsom ZEB1 ökade. Mikroskopi bekräftade dessa förändringar på proteinnivå. Samtidigt var flera gener som främjar celldöd mer aktiva i GPR124-positiva celler, och gener kopplade till transformings tillväxtfaktor beta, en annan viktig utvecklingsväg, var också förändrade. Närliggande stödjeceller kallade pericyter visade sekundära stressreaktioner, men noggrann bildanalys indikerade att endotelcellerna dog först, följt senare av förlust av pericyter och slutligen tomma "spöktrådar" av basalmembran.
Vad detta betyder för ögonhälsa och vidare
Sammantaget placerar fynden GPR124 som en central koordinator av regressionen av hyaloida kärl. Genom att möjliggöra WNT7-driven signalering skjuter GPR124 endotelceller in i ett övergångstillstånd, luckrar upp deras förbindelser, förbereder dem för apoptos och hjälper till att orkestrera det stegvisa kollapset och städningen av föråldrade kärl, samtidigt som den retinala kärltillväxten i stort sett lämnas intakt. Att förstå detta finstämda program ger insikt i hur det utvecklande ögat omformar sig självt och lyfter fram potentiella molekylära måltavlor för behandling av sjukdomar där temporära kärl vägrar att försvinna. Liknande GPR124-beroende övergångar kan forma beskärning av blodkärl i andra organ, vilket antyder bredare relevans för normal utveckling och för sjukdomar präglade av onormal kvarvaro av kärl eller ärrbildning.
Citering: Hannig, L., Heiden, R., Ergün, S. et al. GPR124 regulates hyaloid blood vessel regression and is associated with endothelial-mesenchymal transition. Sci Rep 16, 13765 (2026). https://doi.org/10.1038/s41598-026-50835-1
Nyckelord: ögonutveckling, regression av blodkärl, Wnt-signalering, GPR124, endotelial övergång