Clear Sky Science · de
GPR124 reguliert den Rückbau hyaloider Blutgefäße und steht im Zusammenhang mit dem endothelial-mesenchymalen Übergang
Warum winzige Gefäße im Auge verschwinden müssen
Vor der Geburt durchzieht ein temporäres Geflecht von Blutgefäßen das Innere des Auges und versorgt die wachsende Linse und das umgebende Gewebe. Für später scharfes Sehen muss dieses Gerüst pünktlich verschwinden und durch die permanente Netzhautdurchblutung ersetzt werden. Scheitert diese „Aufräumarbeit“, können Kinder schwere Augenprobleme entwickeln, einschließlich Netzhautablösung und Erblindung. Die vorliegende Studie stellt eine grundlegende, aber entscheidende Frage: Welche molekularen Signale sagen diesen temporären Gefäßen, wann und wie sie verschwinden sollen?
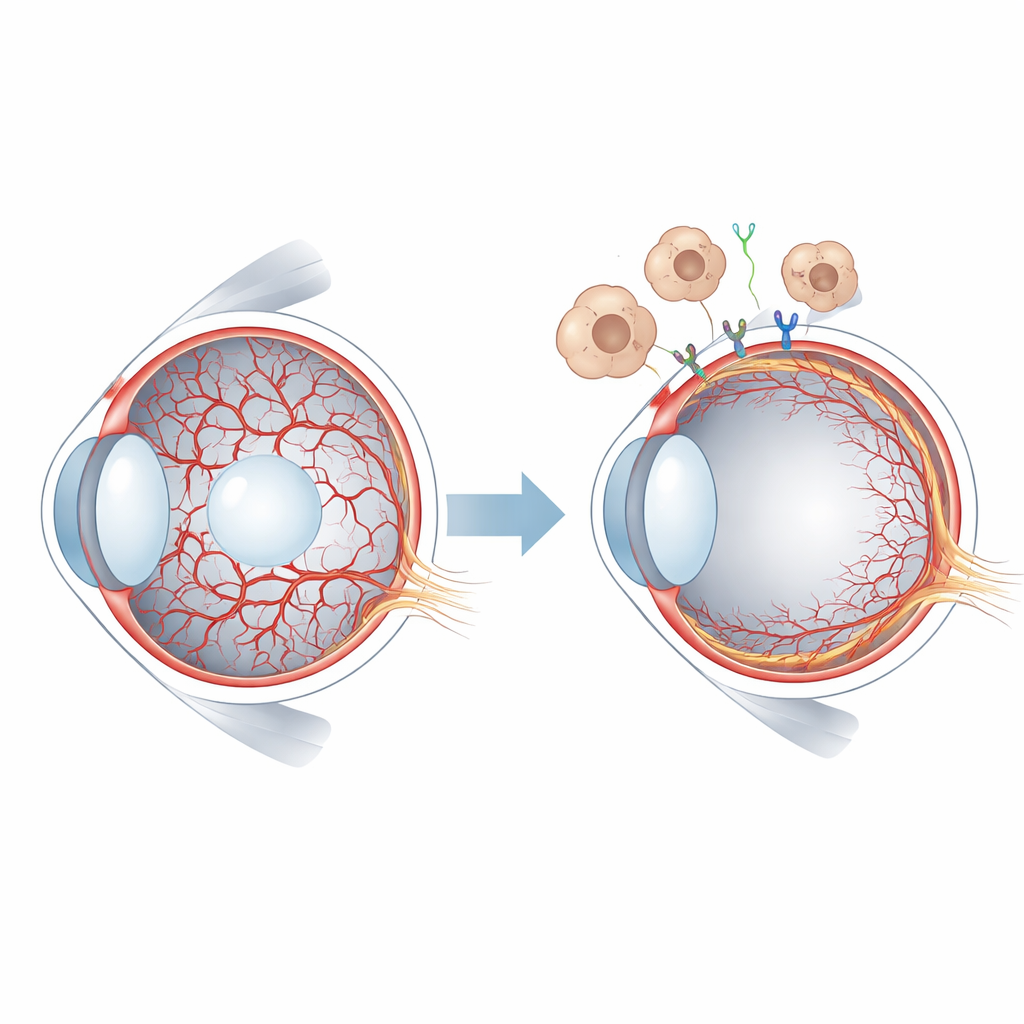
Eine kurzlebige Blutversorgung im jungen Auge
Bei Säugetieren wird das frühe Augenlager von den hyaloiden Gefäßen versorgt, einem feinen Netzwerk, das das gelartige Augeninnere überspannt und die Linse umschließt. Sobald die Netzhaut beginnt, ihre eigene Blutversorgung aufzubauen, muss das hyaloide System zurückgebildet und entfernt werden. Beim Menschen geschieht dies vor der Geburt, bei Mäusen nach der Geburt, was ein günstiges Zeitfenster für experimentelle Untersuchungen bietet. Bleiben die hyaloiden Gefäße bestehen, etwa bei der Erkrankung „persistent hyperplastic primary vitreous“, kann das Sehvermögen stark beeinträchtigt sein. Forscher wussten bereits, dass eine Signalfamilie namens WNT, insbesondere das von Makrophagen freigesetzte Protein WNT7B, die Rückbildung hyaloider Gefäße fördert. Welche Rezeptoren auf Gefäßzellen diese Signale empfangen und welche nachgeschalteten Ereignisse folgen, war jedoch wenig geklärt.
Aufspüren eines wichtigen molekularen Torwächters
Das Team konzentrierte sich auf GPR124, ein rezeptorähnliches Protein, das als Co-Rezeptor für WNT7A und WNT7B im sich entwickelnden Gehirn bekannt ist und dort Gefäßwachstum sowie die Blut-Hirn-Schranke fördert. Die Forscher erzeugten Mäuse, bei denen GPR124 gezielt kurz nach der Geburt in Endothelzellen—den Zellen, die die Gefäße auskleiden—deletiert werden konnte. Wurde GPR124 in hyaloiden Endothelzellen entfernt, regressten die zentralen Augengefäße deutlich langsamer als bei normalen Wurfgeschwistern. Das hyaloide Netzwerk blieb länger dichter, obwohl dasselbe Signal für den Aufbau der retinalen Gefäße an der inneren Augenseite offenbar nicht erforderlich war. Dieser kompartimentspezifische Effekt zeigt, dass GPR124 entscheidend für den Abbau der temporären hyaloiden Zirkulation ist, für den Aufbau des permanenten retinalen Netzwerks dagegen weitgehend entbehrlich.
Wie das Signal Gefäße umformt und entfernt
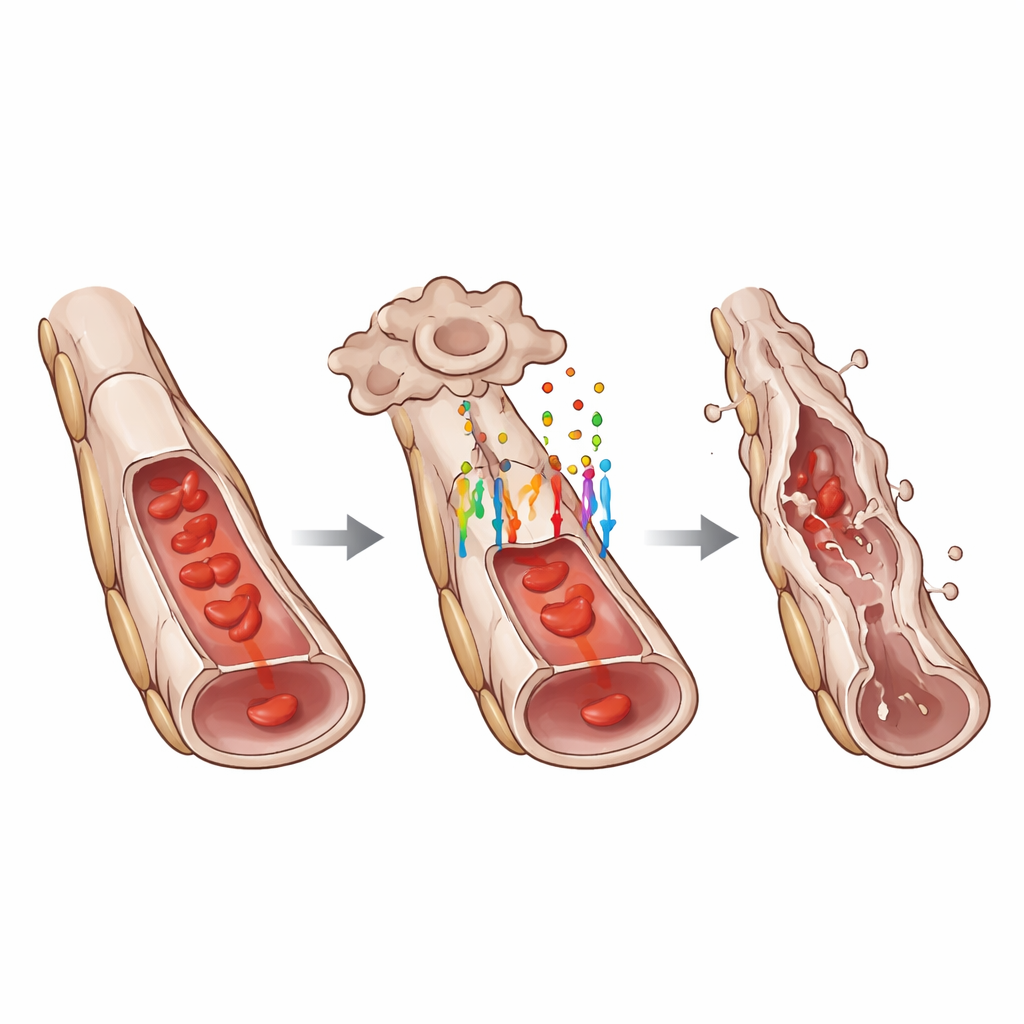
Um zu verstehen, wie GPR124 das Zellverhalten beeinflusst, maßen die Forscher die Aktivität von WNT-Zielgenen in hyaloiden Gefäßen. Sie fanden, dass der Verlust von GPR124 die nukleären Spiegel von LEF1 und anderen klassischen WNT-reaktiven Proteinen deutlich verringerte, was auf eine abgeschwächte WNT/β-Catenin-Signalkaskade hinweist. GPR124 steuerte jedoch nicht alle Formen des Zelltods. Die Zahl einzelner sterbender Endothelzellen entlang ansonsten intakter Gefäße war mit und ohne GPR124 ähnlich. Stattdessen war GPR124 erforderlich für koordinierte „segmentale“ Regressionen, bei denen Stränge benachbarter Endothelzellen entlang eines Gefäßsegments gemeinsam zugrunde gingen, sodass das Rohr kollabierte. Dieses Muster legt nahe, dass GPR124 dabei hilft, verstreute Signale in ein konzertiertes Remodelling-Ereignis zu überführen, das unerwünschte Gefäßabschnitte effizient ausdünnt.
Zellen im Übergang zwischen zwei Identitäten
Tiefergehende Analysen mittels Einzelzell-RNA-Sequenzierung lieferten Expressionsprofile individueller Zellen aus dem hyaloiden Netzwerk. Die Forscher entdeckten, dass Endothelzellen mit intaktem GPR124 ein Genexpressionsmuster zeigten, das mit einer partiellen endothelial-to-mesenchymal-Transition übereinstimmt—einem Zustand, in dem sie beginnen, einige typische endotheliale Merkmale zu verlieren und gleichzeitig Eigenschaften zu gewinnen, die mit mobileren, matrixproduzierenden Zellen assoziiert sind. Klassische endotheliale Marker wie VE-Cadherin und von-Willebrand-Faktor waren reduziert, während mesenchymale Marker wie ZEB1 zunahmen. Mikroskopische Untersuchungen bestätigten diese Veränderungen auf Proteinebene. Zugleich waren mehrere Gene, die den Zelltod fördern, in GPR124-positiven Zellen stärker aktiv, und Gene, die mit dem Transforming-Growth-Factor-Beta-Signalweg verknüpft sind—einem weiteren wichtigen Entwicklungsweg—wurden ebenfalls verändert. Nachbarzellen, sogenannte Perizyten, zeigten sekundäre Stressantworten, doch sorgfältige Bildgebung deutete darauf hin, dass Endothelzellen zuerst starben, gefolgt von Perizytenverlust und schließlich leeren „Geister“-Strängen der Basalmembran.
Was das für die Augengesundheit und darüber hinaus bedeutet
In der Summe positionieren die Ergebnisse GPR124 als zentralen Koordinator der Rückbildung hyaloider Gefäße. Indem GPR124 WNT7-vermittelte Signalgebung ermöglicht, treibt es Endothelzellen in einen Übergangszustand, lockert ihre Verbindungen, setzt sie für Apoptose in Bereitschaft und hilft, den schrittweisen Kollaps und die Bereinigung obsoleter Gefäße zu orchestrieren—während das Wachstum retinaler Gefäße weitgehend unangetastet bleibt. Das Verständnis dieses fein abgestimmten Programms liefert Einblicke, wie sich das sich entwickelnde Auge umgestaltet, und weist auf potenzielle molekulare Ziele zur Behandlung von Erkrankungen hin, bei denen temporäre Gefäße nicht verschwinden wollen. Ähnliche GPR124-abhängige Übergänge könnten auch die Gefäßkürzung in anderen Organen prägen und damit eine breitere Relevanz für normale Entwicklung sowie für Krankheiten mit anhaltender Gefäßpersistenz oder Vernarbung nahelegen.
Zitation: Hannig, L., Heiden, R., Ergün, S. et al. GPR124 regulates hyaloid blood vessel regression and is associated with endothelial-mesenchymal transition. Sci Rep 16, 13765 (2026). https://doi.org/10.1038/s41598-026-50835-1
Schlüsselwörter: Augenentwicklung, Rückbildung von Blutgefäßen, Wnt-Signalgebung, GPR124, endotheliale Transition