Clear Sky Science · nl
GPR124 reguleert regressie van hyaloïde bloedvaten en is geassocieerd met endotheel-mesenchymale transitie
Waarom kleine vaten in het oog moeten verdwijnen
Voor de geboorte is de binnenkant van het oog dooraderd met een tijdelijk web van bloedvaten dat de groeiende lens en het omliggende weefsel van voedingsstoffen voorziet. Voor scherp zicht later in het leven moet dit skelet op tijd verdwijnen en plaatsmaken voor de blijvende retina-circulatie. Als deze opruiming mislukt, kunnen kinderen ernstige oogaandoeningen ontwikkelen, waaronder netvliesloslating en blindheid. Deze studie stelt een fundamentele maar cruciale vraag: welke moleculaire signalen vertellen deze tijdelijke vaten wanneer en hoe ze moeten verdwijnen?
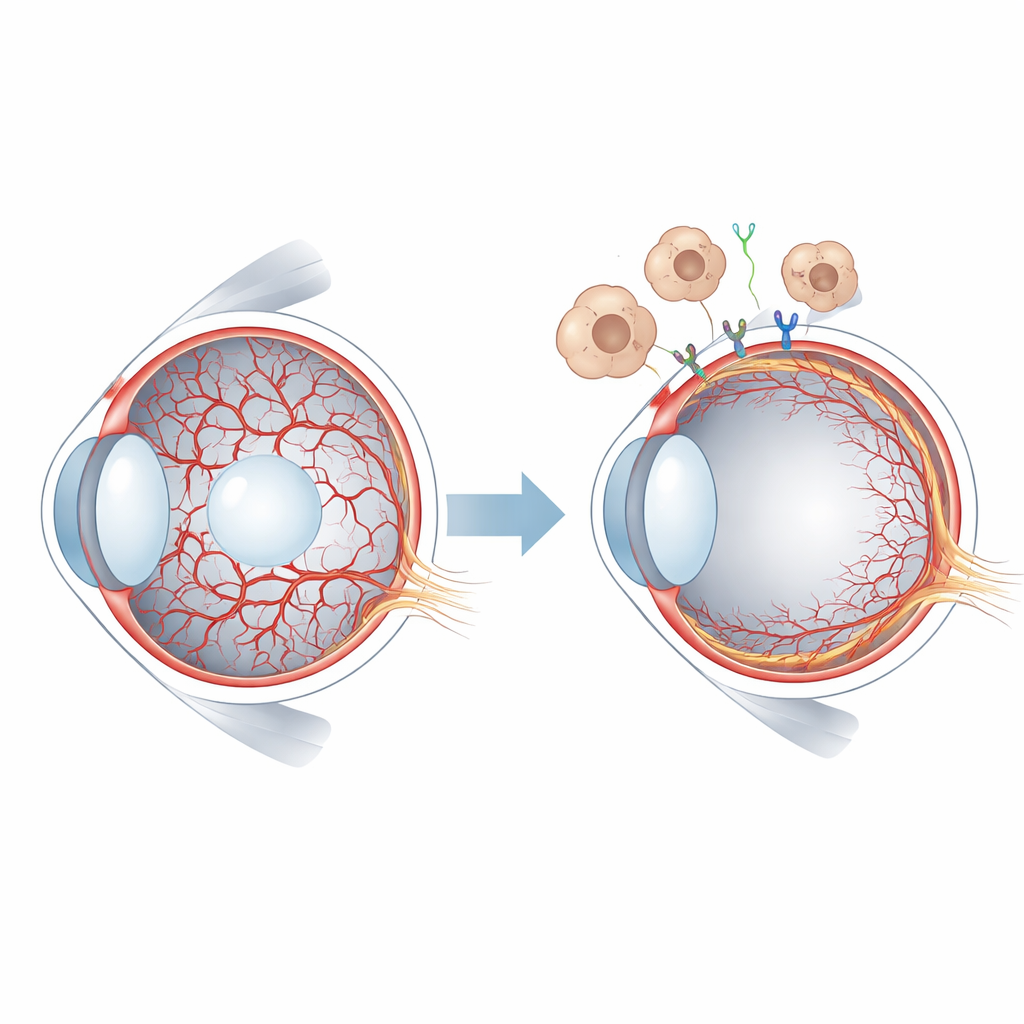
Een kortstondige bloedvoorziening in het jonge oog
Bij zoogdieren wordt het vroege oogweefsel gevoed door de hyaloïde vaten, een delicaat netwerk dat door het gelachtige midden van het oog loopt en zich om de lens heen wikkelt. Terwijl het netvlies zijn eigen bloedvoorziening begint op te bouwen, moeten de hyaloïde vaten terugtrekken en verdwijnen. Bij mensen gebeurt dit vóór de geboorte, terwijl het bij muizen na de geboorte plaatsvindt, wat een handig venster voor experimenteel onderzoek biedt. Wanneer hyaloïde vaten aanhouden, zoals bij een aandoening genaamd persistent hyperplastic primary vitreous, kan het gezichtsvermogen ernstig worden aangetast. Onderzoekers wisten al dat een familie van signalen, WNT genoemd, en in het bijzonder het eiwit WNT7B dat door immuuncellen genaamd macrofagen wordt afgegeven, helpt de regressie van hyaloïde vaten te starten. Maar de specifieke receptoren op bloedvatcellen en de downstream gebeurtenissen waren niet goed begrepen.
Het aanwijzen van een belangrijke moleculaire poortwachter
Het team richtte zich op GPR124, een receptorachtig eiwit dat bekendstaat als co-receptor voor WNT7A en WNT7B in de zich ontwikkelende hersenen, waar het de groei van bloedvaten en de vorming van de bloed-hersenbarrière bevordert. Ze maakten muizen waarbij GPR124 specifiek in endotheelcellen — de cellen die bloedvaten bekleden — kort na de geboorte kon worden uitgeschakeld. Wanneer GPR124 uit hyaloïde endotheelcellen werd verwijderd, regresseerden de centrale oogvaten veel langzamer dan bij normale nestgenoten. Het hyaloïde netwerk bleef langer dichter, ook al leek hetzelfde signaal niet nodig voor het opbouwen van de retinale vaten langs het inwendige oppervlak van het oog. Dit compartimentspecifieke effect toont aan dat GPR124 cruciaal is voor het ontmantelen van de tijdelijke hyaloïde circulatie, maar grotendeels overbodig voor de aanleg van het permanente retinale netwerk.
Hoe het signaal vaten hervormt en verwijdert
Om te begrijpen hoe GPR124 het celgedrag beïnvloedt, maten de onderzoekers de activiteit van WNT-doelgenen in hyaloïde vaten. Ze ontdekten dat verlies van GPR124 de nucleaire niveaus van LEF1 en andere klassieke WNT-responsieve eiwitten duidelijk verminderde, wat wijst op een afgezwakte WNT/β-catenine-route. Toch reguleerde GPR124 niet alle vormen van celdood. Het aantal geïsoleerd stervende endotheelcellen langs anders intacte vaten was vergelijkbaar met of zonder GPR124. In plaats daarvan was GPR124 vereist voor gecoördineerde “segmentale” regressie, waarbij rijen aangrenzende endotheelcellen langs een vatsegment gezamenlijk afsterven, waardoor de buis instort. Dit patroon suggereert dat GPR124 helpt verspreide signalen om te zetten in een gezamenlijk remodeleringsgebeuren dat efficiënt ongewenste vaatsecties snoeit.
Cellen in transitie tussen twee identiteiten
Dieper gravend gebruikten de onderzoekers single-cell RNA-sequencing om individuele cellen uit het hyaloïde netwerk te profileren. Ze ontdekten dat endotheelcellen met intacte GPR124 een genexpressiepatroon vertoonden dat consistent is met een gedeeltelijke endotheel-naar-mesenchymale transitie, een toestand waarin ze beginnen enkele kenmerkende endotheel-eigenschappen te verliezen terwijl ze kenmerken verwerven die passen bij meer mobiele, matrixproducerende cellen. Klassieke endotheelmarkers zoals VE-cadherine en von Willebrand-factor waren verminderd, terwijl mesenchymale markers zoals ZEB1 toenamen. Microscopia bevestigde deze veranderingen op eiwitniveau. Tegelijkertijd waren meerdere genen die celsterfte bevorderen actiever in GPR124-positieve cellen, en genen gekoppeld aan transforming growth factor beta, een andere belangrijke ontwikkelingsroute, waren ook veranderd. Burensteunende cellen genaamd pericyten vertoonden secundaire stressreacties, maar zorgvuldige beeldvorming toonde aan dat endotheelcellen eerst afstierven, gevolgd door later verlies van pericyten en uiteindelijk lege “spook”-strengen van basaalmembraan.
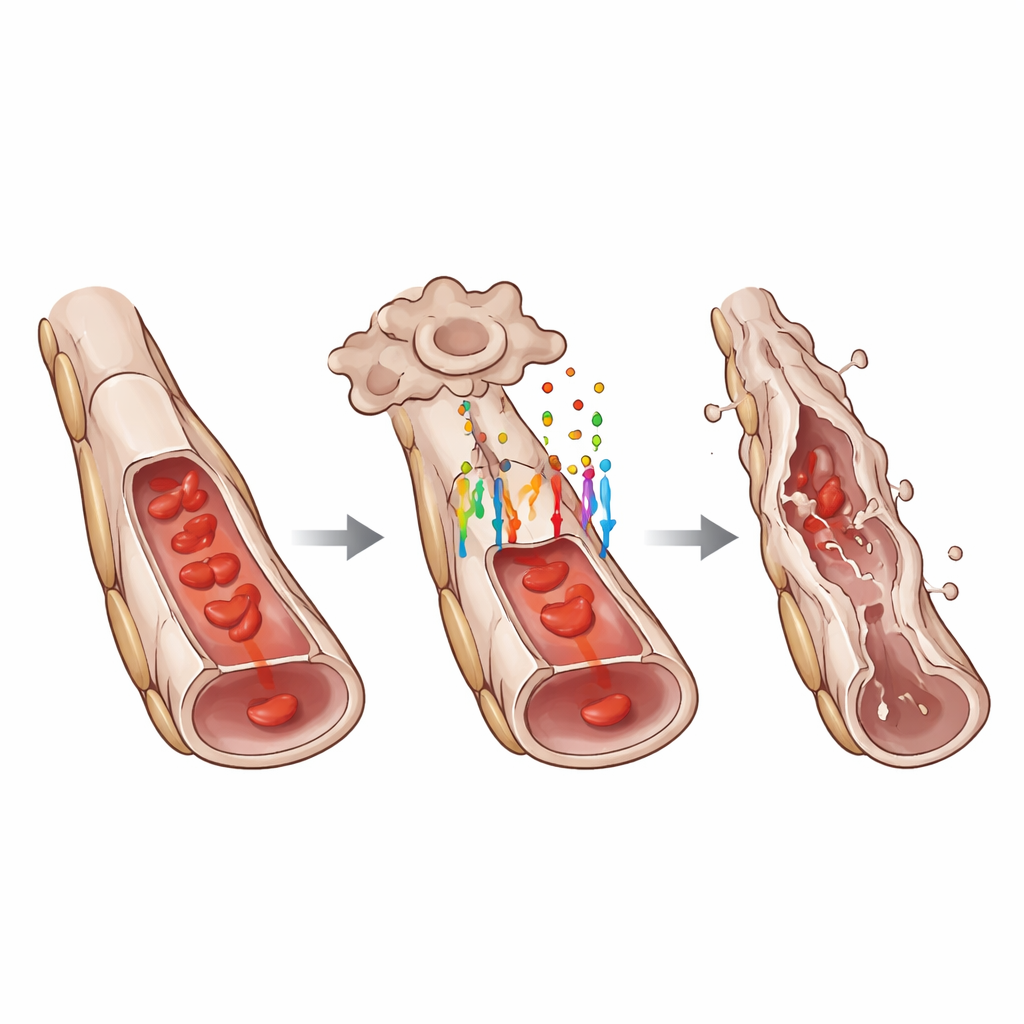
Wat dit betekent voor ooggezondheid en daarbuiten
Alles bij elkaar plaatsen de bevindingen GPR124 als een centrale coördinator van hyaloïde vaatregressie. Door WNT7-gestuurde signalering mogelijk te maken, duwt GPR124 endotheelcellen in een overgangstoestand, versoepelt hun verbindingen, maakt ze gevoelig voor apoptose en helpt het stapsgewijze instorten en opruimen van verouderde vaten te orkestreren, terwijl de groei van retinale vaten grotendeels intact blijft. Inzicht in dit fijn afgestelde programma werpt licht op hoe het zich ontwikkelende oog zichzelf herstructureert en benadrukt potentiële moleculaire doelwitten voor de behandeling van aandoeningen waarbij tijdelijke vaten weigeren te verdwijnen. Vergelijkbare GPR124-afhankelijke transities kunnen de snoei van bloedvaten in andere organen vormgeven, wat wijst op bredere relevantie voor normale ontwikkeling en voor ziekten die worden gekenmerkt door abnormale vatpersistentie of littekenvorming.
Bronvermelding: Hannig, L., Heiden, R., Ergün, S. et al. GPR124 regulates hyaloid blood vessel regression and is associated with endothelial-mesenchymal transition. Sci Rep 16, 13765 (2026). https://doi.org/10.1038/s41598-026-50835-1
Trefwoorden: oogontwikkeling, regressie van bloedvaten, Wnt-signaal, GPR124, endotheeltransitie