Clear Sky Science · zh
在牙龈卟啉单胞菌中鉴定出类LolB蛋白,揭示选择性的LolA–LolB配对
为什么这种口腔细菌重要
大多数人知道牙龈卟啉单胞菌(Porphyromonas gingivalis)会导致牙龈疾病,但这种微生物也与阿尔茨海默症和风湿性关节炎等疾病有关。为生存,它依赖一种精密的运输系统,将称为脂蛋白的特定蛋白质运送到其外表面。这些脂蛋白帮助细菌构建保护性外壳并与宿主发生相互作用。理解这一转运系统的工作原理不仅有助于阐明细菌的基础生物学,也可以揭示新的抗生素弱点,从而在尽量不伤害有益微生物的前提下开发治疗策略。
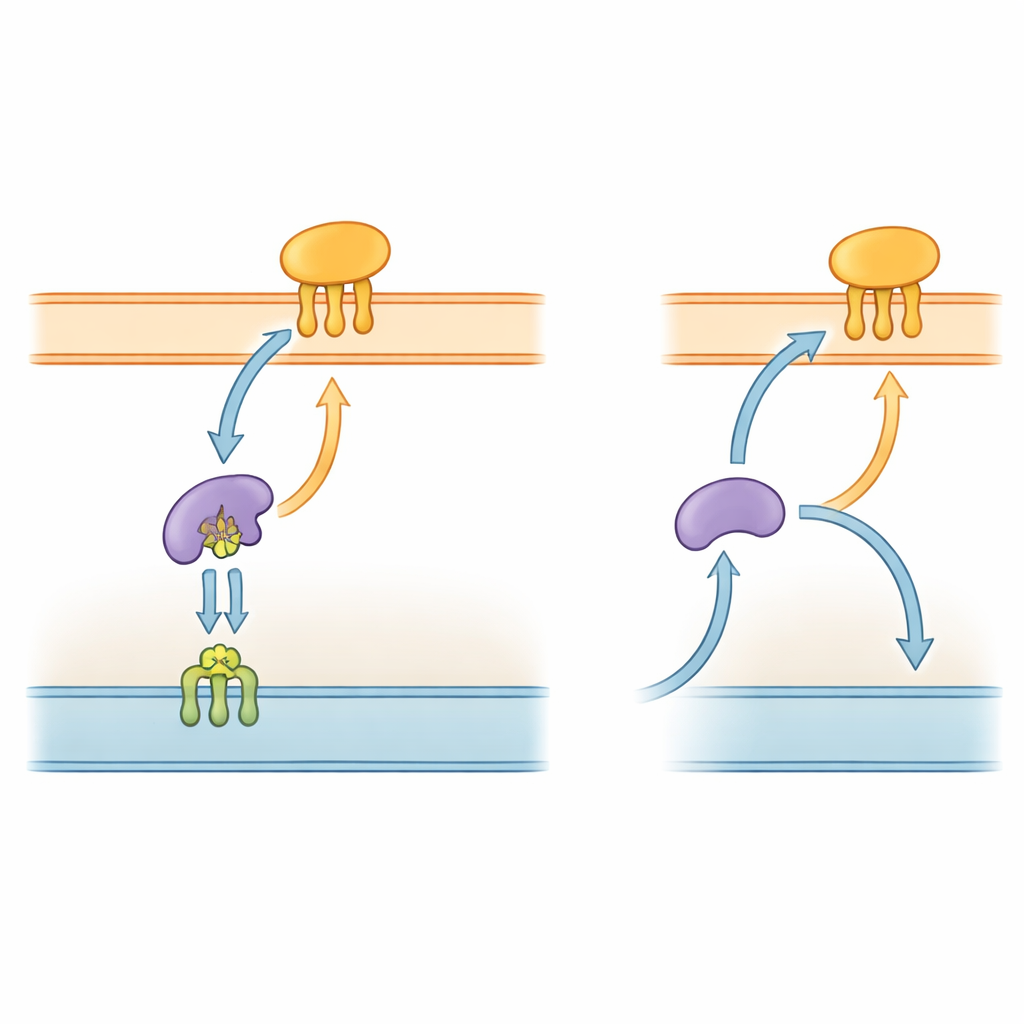
细菌的蛋白质高速公路
革兰氏阴性细菌,包括P. gingivalis,被一个由两层膜和中间水相间隔的复杂包膜包裹。它们的许多关键工具是脂蛋白——通过短的类脂链锚定在膜上的蛋白。在研究透彻的物种如大肠杆菌中,一个由五部分组成的“Lol”系统把这些脂蛋白从内膜搬运,穿过周质间隙,并插入外膜。系统中的一个组分LolA在周质中充当穿梭,而位于外膜的LolB接收货物并将其插入表层。由于这一递送途径对于构建外膜至关重要,Lol系统的部分组分已被作为新型抗生素的研究靶点。
看似缺失的那一块其实并未缺失
多年来,研究者认为P. gingivalis及其在拟杆菌门(Bacteroidota)的一些近亲完全缺失LolB。这引发了一个难题:这些细菌如何将脂蛋白插入外膜?利用现代结构预测工具(如AlphaFold)与后续实验,作者在P. gingivalis中鉴定出一个长期寻觅的候选蛋白,由基因pgn0994编码。他们表明该蛋白(命名为LolB-PG)在折叠方式上几乎与其他细菌已知的LolB蛋白相同,尽管其氨基酸序列差异较大。其三维结构显示出一片弯曲的片层形成深槽,这种形状非常适合托举脂蛋白的脂基尾。
量身定制的分子伙伴关系
团队进一步研究了LolB-PG如何与其可能的搭档LolA相互作用,后者负责在周质中运送脂蛋白。精确的生物物理测量表明,LolB-PG对P. gingivalis的主要LolA蛋白具有强烈且特异的结合力,亲和力与大肠杆菌等其他细菌中经典的LolA–LolB配对相当。相比之下,LolB-PG几乎不与P. gingivalis的第二个LolA样蛋白LolA3或其他物种的LolA发生相互作用。结构建模解释了其原因:LolB-PG与主要LolA以“口对口”方式对接,使两者的槽对齐,脂基尾可以从一个槽滑入另一个槽,而LolA3则呈现不匹配的表面。这些结果表明存在选择性的配对——每个蛋白有专门的角色,而非一套通用的相互作用。
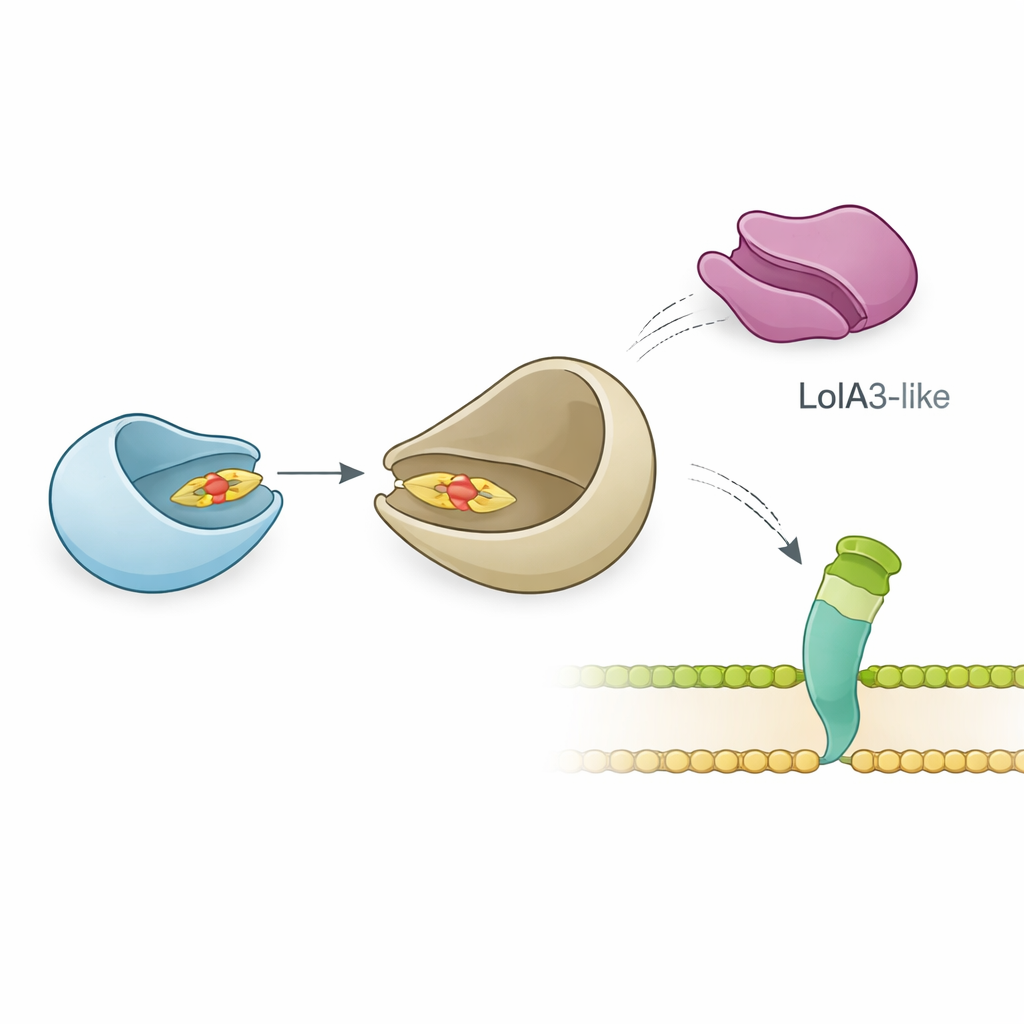
表面组装的惊人灵活性
鉴于这种明确的伙伴关系,研究者原以为去除LolB-PG会严重干扰细菌的外膜。为了验证这一点,他们敲除了pgn0994基因,检查细菌是否仍能构建其由脂蛋白部分组成的长表面纤维(纤毛)。令人惊讶的是,突变株生长正常,且形成的纤毛在外观和功能上与未改造细菌非常相似。关键的纤毛组分仍能被适当加工、运送到包膜并组装成聚合体。这表明,至少在所测试的实验室条件下,P. gingivalis可以使用替代途径转运这些脂蛋白,或者在缺失LolB-PG时有其他系统介入补偿。
对未来治疗的意义
这项工作表明P. gingivalis确实携带一个功能性的类LolB蛋白,并且它与主要的LolA伴侣形成特异性配对,维持了广泛细菌中保守的脂蛋白转运步骤。与此同时,LolB-PG的加宽结合槽、其选择性的配对以及去除该蛋白后未见明显缺陷,都表明这一转运网络比先前认为的更具弹性和多样化。对非专业读者而言,核心结论是:即使是高度保守的细菌系统也会在不同物种中被重新设计,这可能影响抗生素策略从一种病原体向另一种病原体的可推广性。详尽绘制这些变异将对设计能够瓦解像P. gingivalis这样的有害细菌而不广泛损害我们依赖的有益微生物的药物至关重要。
引用: Jaiman, D., Hirohata, M., Hasegawa, Y. et al. Identification of a LolB-like protein in Porphyromonas gingivalis reveals selective LolA–LolB pairing. Sci Rep 16, 13157 (2026). https://doi.org/10.1038/s41598-026-49975-1
关键词: 脂蛋白转运, 牙龈卟啉单胞菌, LolA LolB 系统, 细菌外膜, 抗生素靶点