Clear Sky Science · pl
Identyfikacja białka podobnego do LolB w Porphyromonas gingivalis ujawnia selektywne parowanie LolA–LolB
Dlaczego ten bakteryjny mieszkaniec ust ma znaczenie
Wiele osób zna Porphyromonas gingivalis jako sprawcę chorób dziąseł, ale ten mikroorganizm powiązano także z takimi schorzeniami jak choroba Alzheimera czy reumatoidalne zapalenie stawów. Aby przetrwać, bakteria polega na wyszukanym systemie transportowym, który przenosi pewne białka zwane lipoproteinami na jej zewnętrzną powierzchnię. Lipoproteiny pomagają bakteriom budować ochronną powłokę i wchodzić w interakcje z organizmem gospodarza. Zrozumienie, jak działa ten system transportowy, nie tylko oświetla podstawową biologię bakteryjną, lecz także może ujawnić nowe słabe punkty dla antybiotyków, które oszczędzają pożyteczne mikroby.
Bakteryjna autostrada białkowa
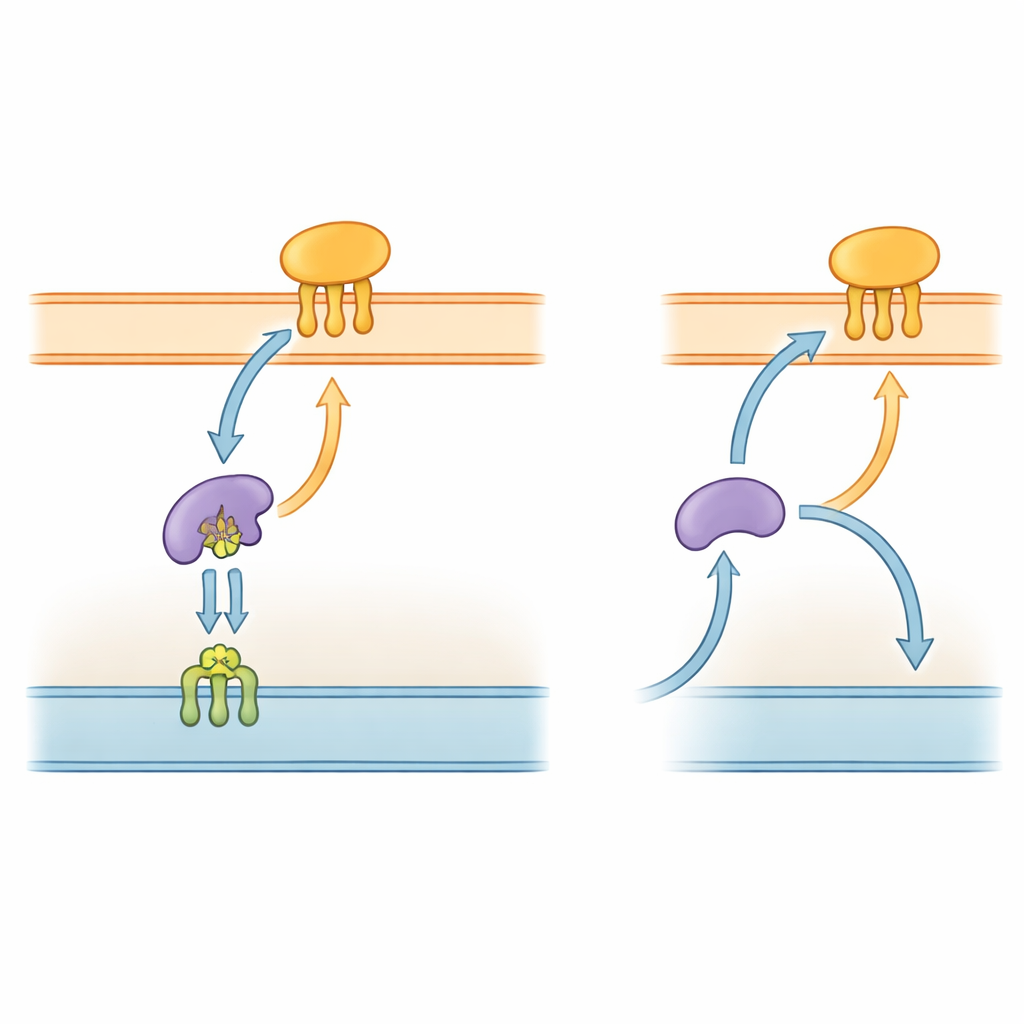
Bakterie Gram-ujemne, w tym P. gingivalis, są otoczone złożoną otoczką składającą się z dwóch błon i wodnistej przestrzeni pomiędzy nimi. Wiele ich kluczowych narzędzi to lipoproteiny — białka zakotwiczone w błonach przez krótkie łańcuchy tłuszczopodobne. W dobrze poznanych gatunkach, takich jak Escherichia coli, pięcioelementowy system „Lol” transportuje te lipoproteiny z błony wewnętrznej, przez periplazmę, do błony zewnętrznej. Jeden składnik, LolA, działa jak wahadłowy przenośnik w periplazmie, podczas gdy LolB w błonie zewnętrznej odbiera ładunek i wbija go w warstwę powierzchniową. Ponieważ ta droga dostarczania jest niezbędna do budowy błony zewnętrznej, elementy systemu Lol są już badane jako potencjalne cele nowych antybiotyków.
Brakująca część, która w rzeczywistości nie była brakująca
Przez lata badacze uważali, że P. gingivalis i wielu jej krewnych z grupy Bacteroidota całkowicie pozbawione są LolB. To rodziło zagadkę: jak te bakterie wstawiają lipoproteiny do błony zewnętrznej? Wykorzystując nowoczesne narzędzia do przewidywania struktur (takie jak AlphaFold) oraz późniejsze eksperymenty, autorzy zidentyfikowali długo poszukiwany kandydat w P. gingivalis — białko kodowane przez gen pgn0994. Pokazali, że to białko, które nazwali LolB-PG, fałduje się niemal w ten sam sposób co znane białka LolB z innych bakterii, mimo znaczących różnic w sekwencji aminokwasowej. Jego trójwymiarowa struktura ujawniła zakrzywioną płytę tworzącą głęboką szczelinę, kształt dobrze nadający się do podtrzymania tłuszczowego ogonka lipoproteiny.
Uszyta na miarę molekularna współpraca
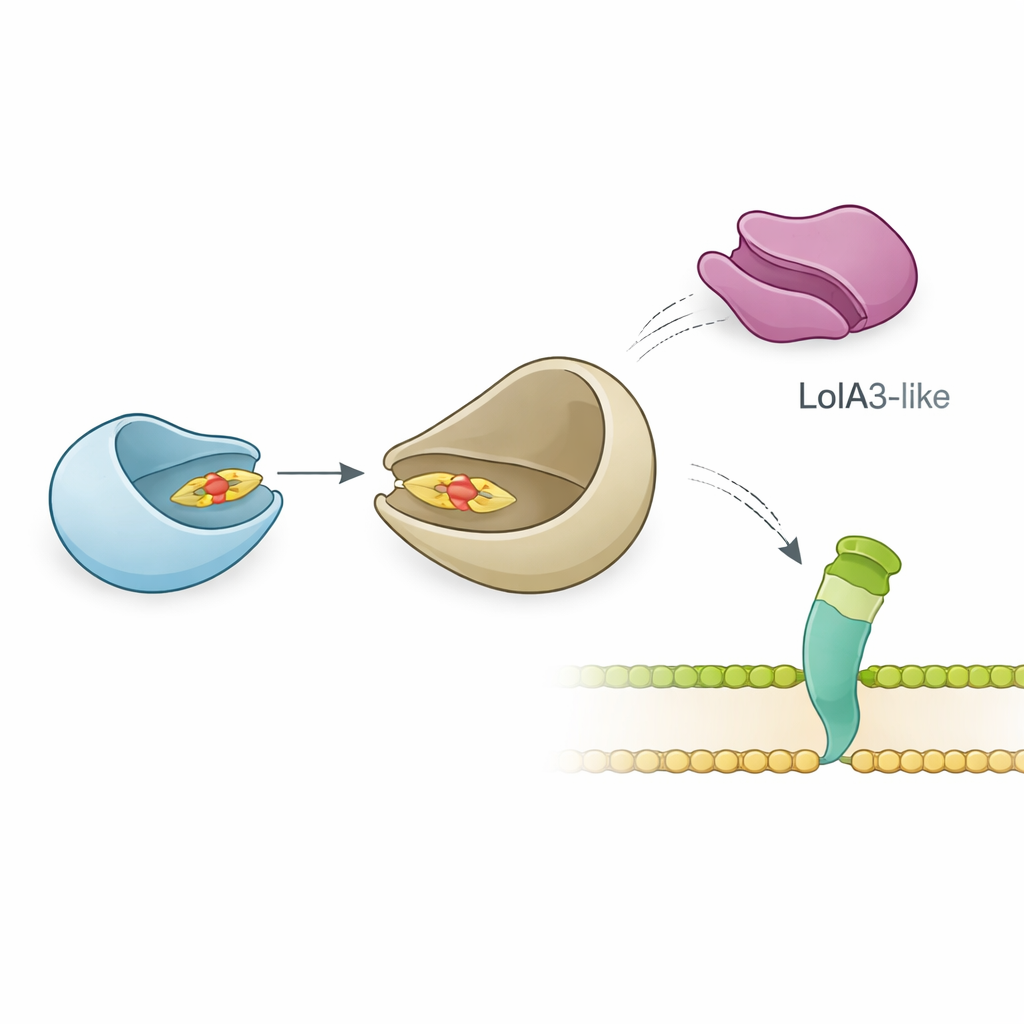
Zespół zbadał, jak LolB-PG wchodzi w interakcję ze swoim prawdopodobnym partnerem, LolA, który przewozi lipoproteiny przez periplazmę. Dokładne pomiary biofizyczne wykazały, że LolB-PG wiąże się silnie i specyficznie z głównym białkiem LolA z P. gingivalis, z powinowactwem porównywalnym do klasycznych par LolA–LolB w E. coli i innych bakteriach. W przeciwieństwie do tego, LolB-PG prawie nie oddziałuje z drugim, podobnym do LolA białkiem w P. gingivalis, nazwanym LolA3, ani z LolA z innych gatunków. Modelowanie strukturalne zasugerowało dlaczego: LolB-PG i podstawowy LolA łączą się w sposób „twarz w twarz”, wyrównując swoje szczeliny tak, by lipidowy ogonek mógł przesunąć się z jednego do drugiego, podczas gdy powierzchnia LolA3 jest niepasująca. Wyniki te wskazują na selektywne parowanie, w którym każde białko pełni dedykowaną rolę zamiast uniwersalnej interakcji.
Zaskakująca elastyczność w montażu powierzchni
Mając tę wyraźną współpracę, badacze spodziewali się, że usunięcie LolB-PG poważnie zaburzy błonę zewnętrzną bakterii. Aby to sprawdzić, usunęli gen pgn0994 i zbadali, czy bakteria nadal potrafi budować swoje długie włókna powierzchniowe, tzw. fimbrie, które są częściowo zbudowane z lipoprotein. Ku zaskoczeniu, szczep mutantów rósł normalnie i tworzył fimbrie wyglądające i zachowujące się podobnie jak u niezmodyfikowanych bakterii. Kluczowe składniki fimbrialne były nadal prawidłowo przetwarzane, transportowane do otoczki i składane w polimery. To sugeruje, że przynajmniej w warunkach laboratoryjnych P. gingivalis potrafi korzystać z alternatywnych dróg przemieszczania tych lipoprotein lub że inne układy wkraczają do akcji, gdy brakuje LolB-PG.
Co to oznacza dla przyszłych terapii
Ta praca pokazuje, że P. gingivalis rzeczywiście posiada funkcjonalne białko podobne do LolB, które tworzy specyficzne partnerstwo ze swoim głównym opiekunem LolA, zachowując kluczowy etap transportu lipoprotein obecny w wielu bakteriach. Jednocześnie powiększona szczelina wiążąca LolB-PG, jego selektywne parowanie oraz brak oczywistych wad po usunięciu białka wskazują na bardziej elastyczną i zdywersyfikowaną sieć transportową niż sądzono wcześniej. Dla laików najważniejszy wniosek jest taki, że nawet silnie zachowane systemy bakteryjne mogą być przekształcane w różnych gatunkach, co może wpływać na skuteczność strategii antybiotykowych przenoszonych z jednego patogenu na innego. Mapowanie tych wariacji w szczegółach będzie kluczowe przy projektowaniu leków, które unieszkodliwią szkodliwe bakterie, takie jak P. gingivalis, bez szerokiego uszkadzania pożytecznych mikroorganizmów, od których jesteśmy zależni.
Cytowanie: Jaiman, D., Hirohata, M., Hasegawa, Y. et al. Identification of a LolB-like protein in Porphyromonas gingivalis reveals selective LolA–LolB pairing. Sci Rep 16, 13157 (2026). https://doi.org/10.1038/s41598-026-49975-1
Słowa kluczowe: transport lipoprotein, Porphyromonas gingivalis, układ LolA LolB, zewnętrzna błona bakteryjna, cele antybiotyków