Clear Sky Science · ru
Идентификация белка, подобного LolB, в Porphyromonas gingivalis выявляет селективное спаривание LolA–LolB
Почему этот ротавый бактерий важен
Большинство людей знают Porphyromonas gingivalis как возбудителя заболеваний десен, но этот микроорганизм также связывают с такими состояниями, как болезнь Альцгеймера и ревматоидный артрит. Для выживания он полагается на сложную систему «доставки», которая перемещает определённые белки — липопротеины — на его внешний слой. Эти липопротеины помогают бактерии формировать защитную оболочку и взаимодействовать с нашим организмом. Понимание того, как работает этот транспорт, не только проясняет базовую биологию бактерий, но и может выявить новые уязвимые места для антибиотиков, щадящих полезную микрофлору.
Белковая магистраль бактерий
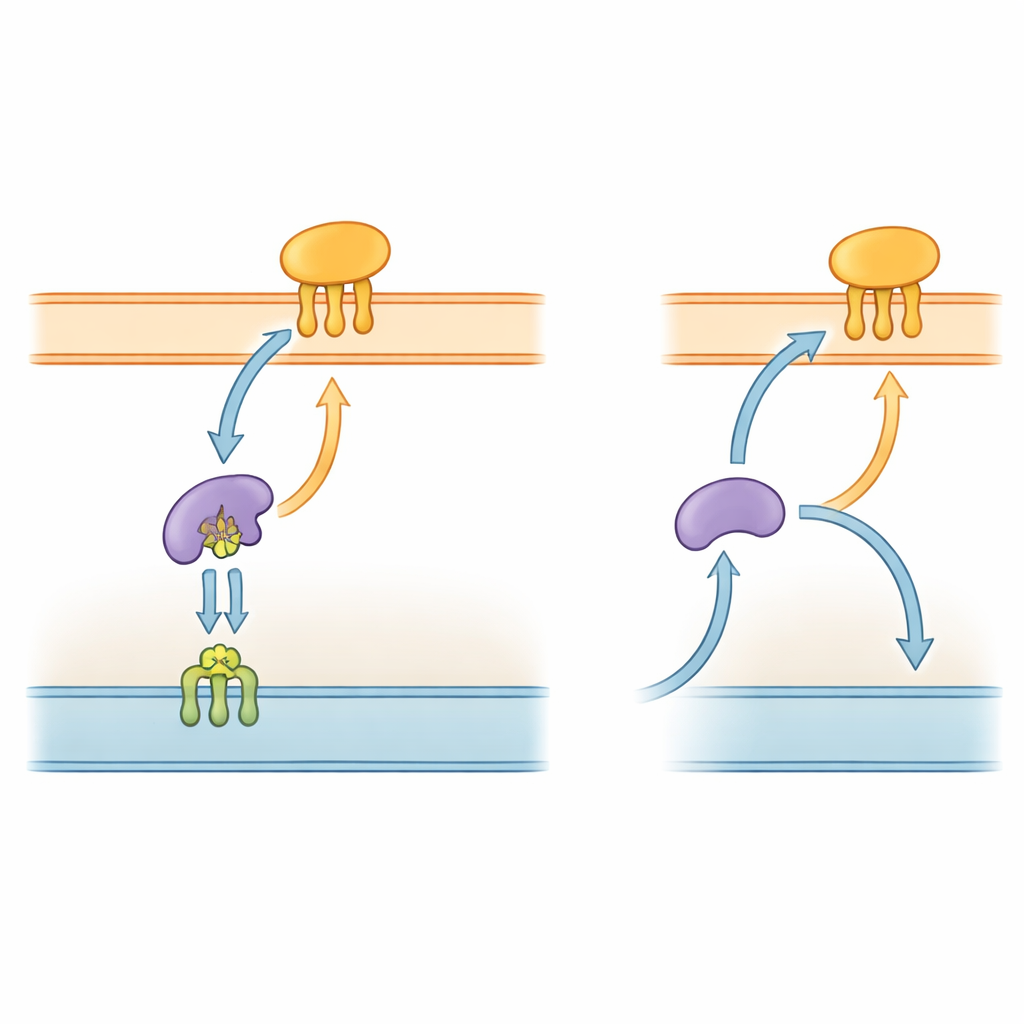
Грам-отрицательные бактерии, включая P. gingivalis, окружены сложной оболочкой с двумя мембранами и водной периплазматической зоной между ними. Многие их ключевые инструменты — это липопротеины: белки, якорящиеся в мембране короткими жироподобными цепочками. У хорошо изученных видов, таких как Escherichia coli, пятимерная система «Lol» вывозит эти липопротеины из внутренней мембраны через периплазму и встраивает их в наружную мембрану. Один компонент, LolA, действует как носильщик в периплазме, тогда как LolB в наружной мембране принимает груз и вставляет его в поверхностный слой. Поскольку этот путь доставки необходим для сборки наружной мембраны, компоненты системы Lol уже рассматриваются как потенциальные мишени для новых антибиотиков.
Отсутствовавшая деталь, которой на самом деле не было
В течение многих лет исследователи считали, что у P. gingivalis и у многих её родственников из группы Bacteroidota вовсе отсутствует LolB. Это вызывало вопрос: как эти бактерии встраивают липопротеины в свою наружную мембрану? С помощью современных инструментов предсказания структуры (таких как AlphaFold) и последующих экспериментов авторы выявили давно разыскиваемого кандидата в P. gingivalis — белок, кодируемый геном pgn0994. Они показали, что этот белок, который назвали LolB-PG, складывается почти так же, как известные LolB у других бактерий, несмотря на значительные различия в аминокислотной последовательности. Его трёхмерная структура открыла изогнутый лист, формирующий глубокую борозду — форму, хорошо подходящую для удержания жирного хвоста липопротеина.
Подогнанное молекулярное партнёрство
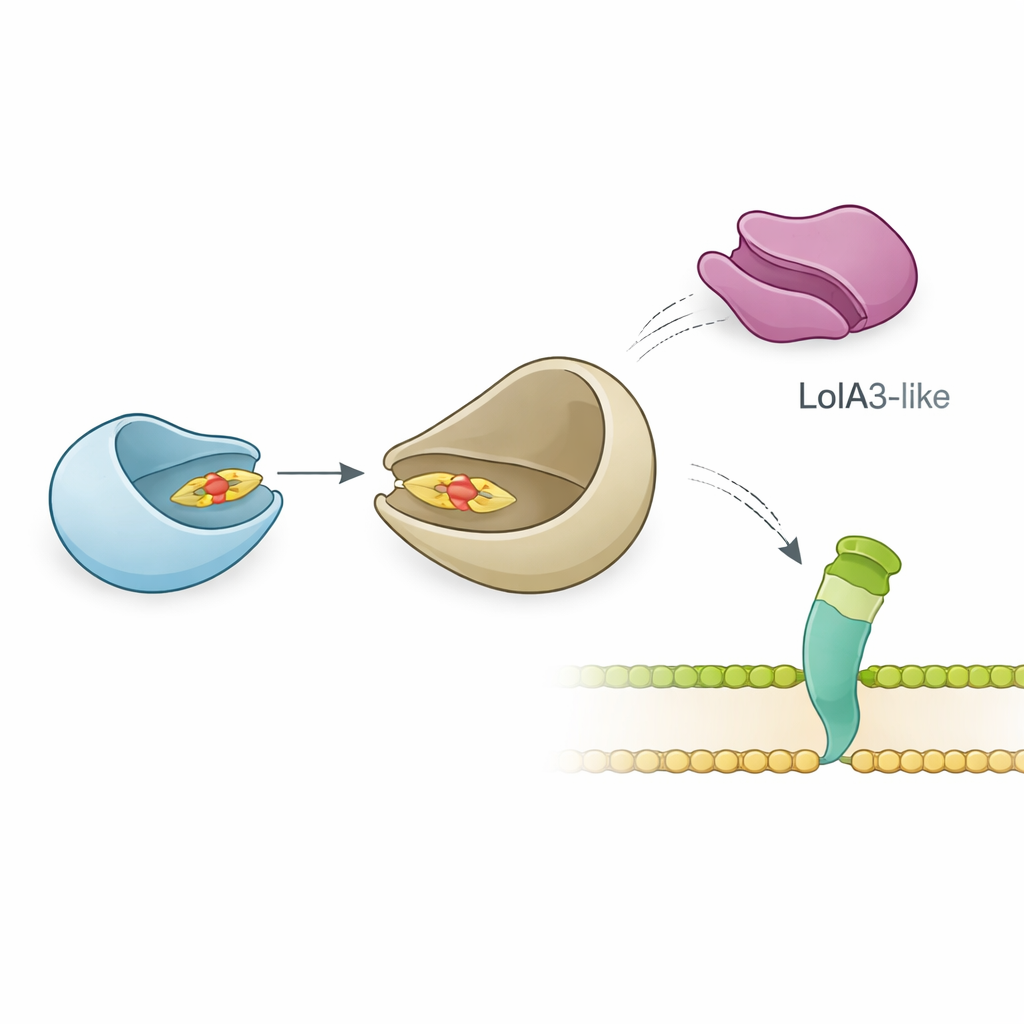
Команда далее изучила, как LolB-PG взаимодействует с вероятным партнёром, LolA, который переносит липопротеины через периплазму. Точные биофизические измерения показали, что LolB-PG сильно и специфично связывается с основным белком LolA у P. gingivalis с аффинностью, сопоставимой с классическими парами LolA–LolB у E. coli и других бактерий. Напротив, LolB-PG почти не взаимодействовал со вторым похожим на LolA белком в P. gingivalis, называемым LolA3, или с LolA из других видов. Модель структурного взаимодействия объяснила причину: LolB-PG и основной LolA стыкуются «рот к рту», выравнивая свои борозды так, чтобы липидный хвост мог скользнуть от одного к другому, тогда как у LolA3 поверхность не совпадает. Эти результаты указывают на избирательное спаривание, в котором каждый белок выполняет свою специализированную роль, а не универсальное взаимодействие.
Неожиданная гибкость в сборке поверхности
Учитывая это явное партнёрство, исследователи ожидали, что удаление LolB-PG серьёзно нарушит наружную мембрану бактерии. Чтобы проверить это, они удалили ген pgn0994 и исследовали, могла ли бактерия по-прежнему собирать длинные поверхностные волокна — фимбрии, частично состоящие из липопротеинов. Удивительно, мутантный штамм рос нормально и формировал фимбрии, похожие по внешнему виду и поведению на фимбрии немодифицированной бактерии. Ключевые компоненты фимбрий по-прежнему корректно обрабатывались, транспортировались в оболочку и собирались в полимеры. Это говорит о том, что, по крайней мере в исследованных лабораторных условиях, P. gingivalis может использовать альтернативные пути для перемещения этих липопротеинов или что другие системы включаются в компенсацию при отсутствии LolB-PG.
Что это значит для будущих методов лечения
Эта работа демонстрирует, что P. gingivalis действительно несёт функциональный белок, подобный LolB, который образует специфическое партнёрство с основным шапероном LolA, сохраняя фундаментальный этап транспорта липопротеинов, наблюдаемый у многих бактерий. В то же время расширенная связывающая борозда LolB-PG, его селективность и отсутствие явных дефектов при удалении белка указывают на более гибкую и диверсифицированную сеть транспорта, чем считалось ранее. Для неспециалиста основная мысль такова: даже высококонсервативные бактериальные системы могут быть переработаны у разных видов, что может влиять на переносимость антибиотических стратегий от одного патогена к другому. Подробная картография таких вариаций будет критична для разработки препаратов, которые обезвреживают вредные бактерии, например P. gingivalis, не причиняя широкого вреда полезным микроорганизмам, от которых мы зависим.
Цитирование: Jaiman, D., Hirohata, M., Hasegawa, Y. et al. Identification of a LolB-like protein in Porphyromonas gingivalis reveals selective LolA–LolB pairing. Sci Rep 16, 13157 (2026). https://doi.org/10.1038/s41598-026-49975-1
Ключевые слова: транспорт липопротеинов, Porphyromonas gingivalis, система LolA LolB, наружная мембрана бактерий, молекулярные мишени антибиотиков