Clear Sky Science · pt
Identificação de uma proteína do tipo LolB em Porphyromonas gingivalis revela emparelhamento seletivo LolA–LolB
Por que esta bactéria oral importa
A maioria das pessoas conhece Porphyromonas gingivalis como um agente problemático na doença gengival, mas esse microrganismo também tem sido ligado a condições como Alzheimer e artrite reumatoide. Para sobreviver, depende de um sistema sofisticado de transporte que leva certas proteínas, chamadas lipoproteínas, à sua superfície externa. Essas lipoproteínas ajudam a bactéria a construir sua camada protetora e a interagir com nosso organismo. Entender como esse sistema de transporte funciona não apenas ilumina a biologia bacteriana básica, como também pode revelar novas vulnerabilidades para antibióticos que preservem nossos micróbios benéficos.
A rodovia proteica bacteriana
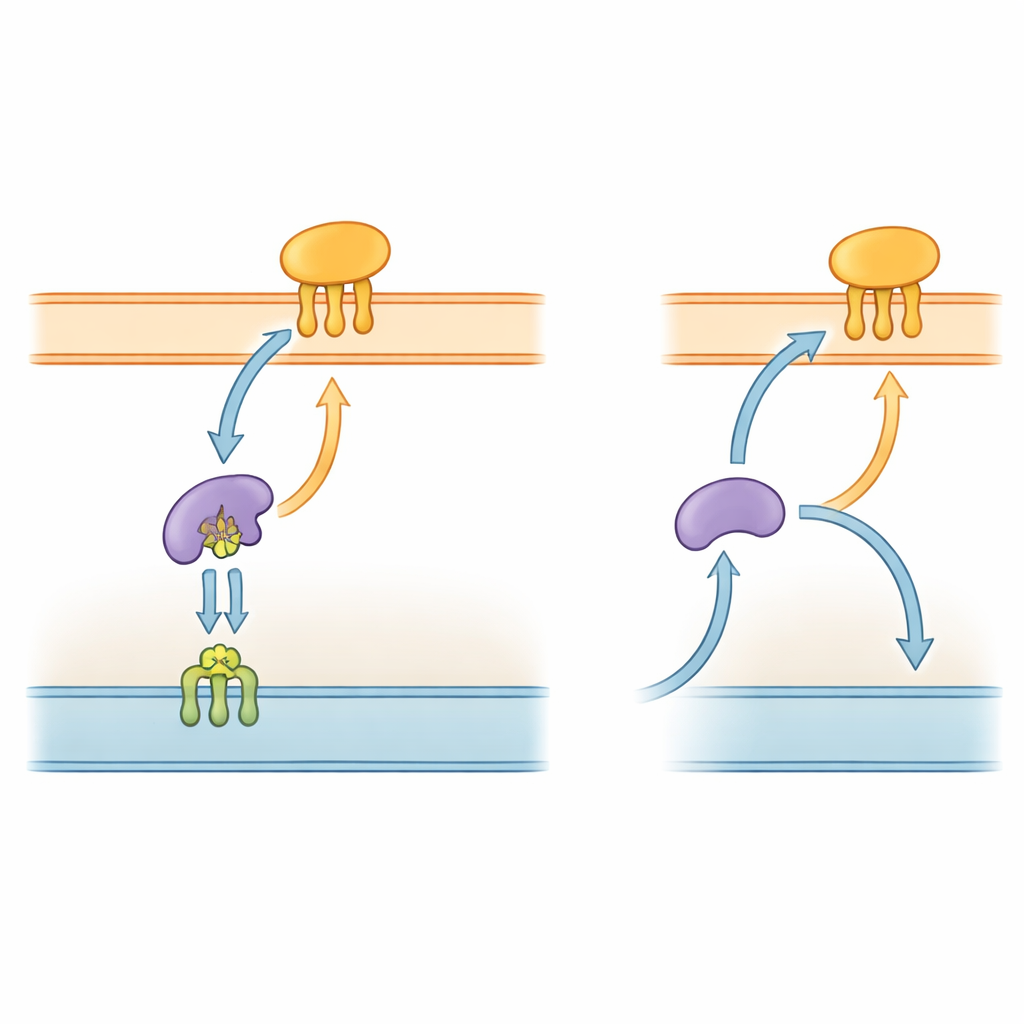
Bactérias Gram-negativas, incluindo P. gingivalis, são envoltas por um envelope complexo com duas membranas e um espaço aquoso entre elas. Muitas de suas ferramentas-chave são lipoproteínas — proteínas ancoradas às membranas por cadeias curtas semelhantes a gorduras. Em espécies bem estudadas, como Escherichia coli, um sistema “Lol” de cinco componentes transporta essas lipoproteínas da membrana interna, através do espaço periplasmático, até a membrana externa. Um componente, LolA, atua como um ônibus no periplasma, enquanto LolB, na membrana externa, recebe a carga e a insere na camada superficial. Como essa via de entrega é essencial para construir a membrana externa, partes do sistema Lol já estão sendo exploradas como alvos para novos antibióticos.
Uma peça ausente que, na verdade, não estava ausente
Durante anos, pesquisadores acharam que P. gingivalis e muitos de seus parentes no grupo Bacteroidota não possuíam LolB. Isso levantou um quebra-cabeça: como essas bactérias conseguiam inserir lipoproteínas em sua membrana externa? Usando ferramentas modernas de predição de estrutura (como AlphaFold) e experimentos de acompanhamento, os autores identificaram um candidato muito procurado em P. gingivalis, uma proteína codificada pelo gene pgn0994. Eles mostraram que essa proteína, que chamam de LolB-PG, se dobra de maneira quase idêntica às proteínas LolB conhecidas de outras bactérias, apesar de sua sequência de aminoácidos ser bastante diferente. Sua estrutura tridimensional revelou uma folha curva formando um sulco profundo, uma forma bem adequada para acomodar a cauda lipídica de uma lipoproteína.
Uma parceria molecular feita sob medida
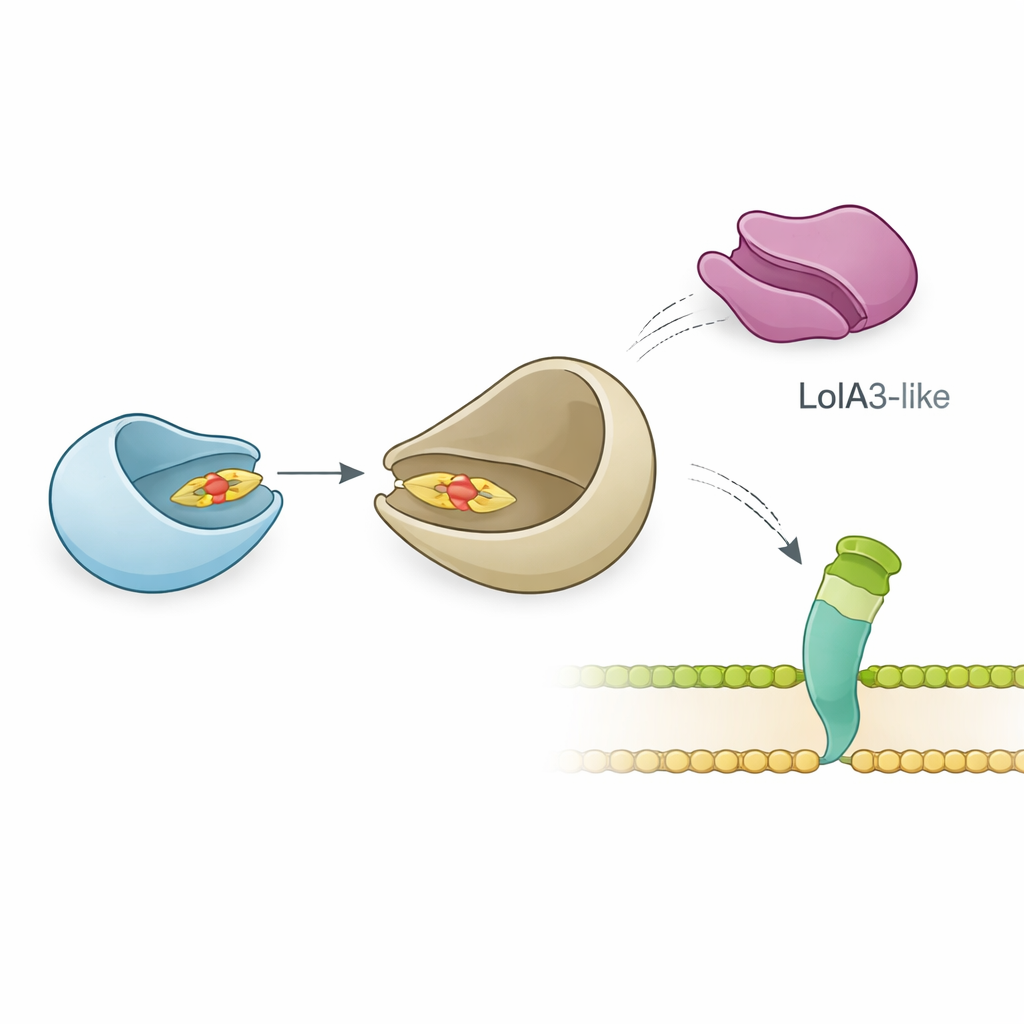
A equipe examinou como LolB-PG interage com seu provável parceiro, LolA, que transporta lipoproteínas pelo periplasma. Medições biofísicas precisas demonstraram que LolB-PG se liga forte e especificamente à principal proteína LolA de P. gingivalis, com afinidade similar aos pares clássicos LolA–LolB de E. coli e outras bactérias. Em contraste, LolB-PG quase não interage com uma segunda proteína semelhante a LolA em P. gingivalis, chamada LolA3, nem com LolA de outras espécies. Modelagens estruturais sugeriram o motivo: LolB-PG e a LolA principal encaixam-se em um arranjo “boca-a-boca”, alinhando seus sulcos para que a cauda lipídica deslize de uma para a outra, enquanto LolA3 apresenta uma superfície incompatível. Esses resultados apontam para um emparelhamento seletivo em que cada proteína tem um papel dedicado, ao invés de uma interação única para todos os casos.
Surpreendente flexibilidade na montagem da superfície
Diante dessa parceria clara, os pesquisadores esperavam que remover LolB-PG interrompesse seriamente a membrana externa da bactéria. Para testar isso, deletaram o gene pgn0994 e examinaram se a bactéria ainda podia construir suas longas fibras superficiais, chamadas fímbria, que são em parte compostas por lipoproteínas. Surpreendentemente, a cepa mutante cresceu normalmente e formou fímbria que pareciam e se comportavam de modo muito semelhante às das bactérias não modificadas. Componentes-chave das fímbria ainda foram corretamente processados, transportados ao envelope e montados em polímeros. Isso sugere que, pelo menos nas condições laboratoriais testadas, P. gingivalis pode usar rotas alternativas para mover essas lipoproteínas, ou que outros sistemas assumem a função quando LolB-PG está ausente.
O que isso significa para tratamentos futuros
Este trabalho mostra que P. gingivalis, de fato, carrega uma proteína funcional do tipo LolB que forma uma parceria específica com sua chaperona LolA principal, preservando um passo fundamental do transporte de lipoproteínas observado em muitas bactérias. Ao mesmo tempo, o sulco de ligação ampliado de LolB-PG, seu emparelhamento seletivo e a falta de defeitos óbvios quando a proteína é removida apontam para uma rede de transporte mais flexível e diversificada do que se pensava. Para não especialistas, a mensagem principal é que mesmo sistemas bacterianos altamente conservados podem ser redesenhados em espécies diferentes, o que pode influenciar o quão bem estratégias antibióticas se traduzem de um patógeno para outro. Mapear essas variações em detalhe será crucial para projetar fármacos capazes de desarmar bactérias nocivas como P. gingivalis sem prejudicar amplamente os micróbios benéficos dos quais dependemos.
Citação: Jaiman, D., Hirohata, M., Hasegawa, Y. et al. Identification of a LolB-like protein in Porphyromonas gingivalis reveals selective LolA–LolB pairing. Sci Rep 16, 13157 (2026). https://doi.org/10.1038/s41598-026-49975-1
Palavras-chave: transporte de lipoproteínas, Porphyromonas gingivalis, sistema LolA LolB, membrana externa bacteriana, alvos antibióticos