Clear Sky Science · sv
Identifiering av ett LolB-liknande protein i Porphyromonas gingivalis avslöjar selektivt LolA–LolB-parning
Varför denna munsbakterie spelar roll
De flesta känner igen Porphyromonas gingivalis som en bov i tandköttssjukdomar, men denna mikrob har även kopplats till tillstånd som Alzheimers och reumatoid artrit. För att överleva är den beroende av ett sofistikerat transportsystem som flyttar vissa proteiner, kallade lipoproteiner, till dess yttre yta. Dessa lipoproteiner hjälper bakterien att bygga sitt skyddande hölje och att interagera med vår kropp. Att förstå hur detta transportsystem fungerar belyser inte bara grundläggande bakteriebiologi utan kan också avslöja nya svaga punkter för antibiotika som skonar våra hjälpsamma mikrober.
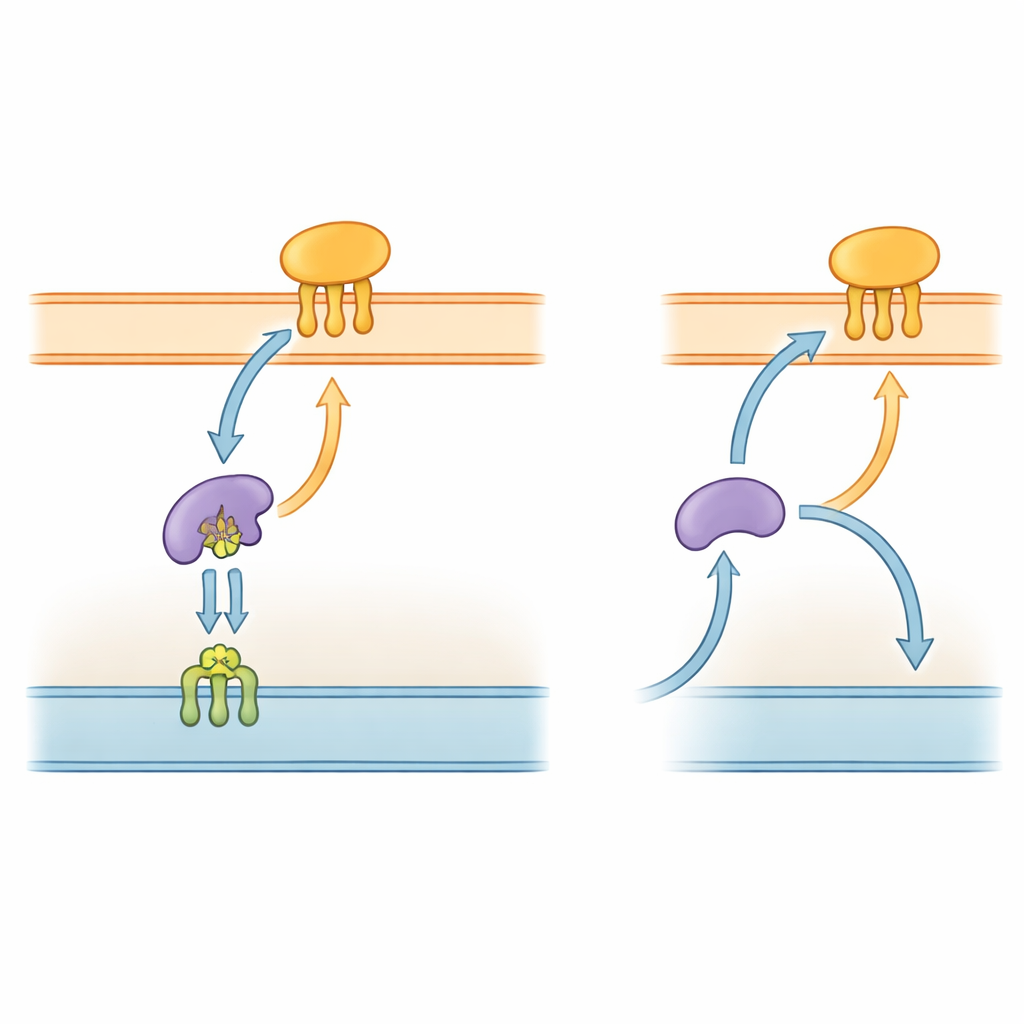
Bakteriens proteinmotorväg
Gramnegativa bakterier, inklusive P. gingivalis, är omslutna av ett komplext hölje med två membran och ett vattenfyllt utrymme däremellan. Många av deras viktigaste verktyg är lipoproteiner — proteiner förankrade i membran genom korta fettliknande kedjor. I välstuderade arter som Escherichia coli transporterar ett femdelat ”Lol”-system dessa lipoproteiner från det inre membranet, genom periplasman, och in i det yttre membranet. En komponent, LolA, fungerar som en färdväg i periplasman, medan LolB i det yttre membranet tar emot lasten och sätter in den i ytlagret. Eftersom denna leveransväg är avgörande för att bygga det yttre membranet undersöks delar av Lol-systemet redan som möjliga mål för nya antibiotika.
En saknad del som egentligen inte var saknad
I åratal trodde forskare att P. gingivalis och många av dess släktingar i Bacteroidota-gruppen saknade LolB helt. Det väckte en gåta: hur lyckades dessa bakterier få in lipoproteiner i sitt yttre membran? Med moderna strukturförutsägelseverktyg (såsom AlphaFold) och uppföljande experiment identifierade författarna en länge eftertraktad kandidat i P. gingivalis, ett protein som kodas av genen pgn0994. De visade att detta protein, som de kallar LolB-PG, veckar sig nästan på samma sätt som kända LolB-proteiner från andra bakterier, trots att dess aminosyrasekvens är ganska annorlunda. Dess tredimensionella struktur visade ett krökt blad som bildar en djup fåra, en form väl lämpad att vagga lipoproteinets fettsvans.
En skräddarsydd molekylär partnerskap
Gruppen undersökte vidare hur LolB-PG interagerar med sin sannolika partner, LolA, som transporterar lipoproteiner genom periplasman. Exakta biofysiska mätningar visade att LolB-PG binder starkt och specifikt till P. gingivalis huvudsakliga LolA-protein, med en affinitet liknande klassiska LolA–LolB-par i E. coli och andra bakterier. I kontrast interagerar LolB-PG knappt med ett andra LolA-liknande protein i P. gingivalis, kallat LolA3, eller med LolA från andra arter. Strukturell modellering föreslog varför: LolB-PG och den primära LolA:n dockar i en ”mun-mot-mun”-konfiguration, där deras fåror alignerar så att lipidsvansen kan glida från den ena till den andra, medan LolA3 presenterar en mismatchad yta. Dessa resultat pekar på en selektiv parning där varje protein har en dedikerad roll snarare än en universell interaktion.
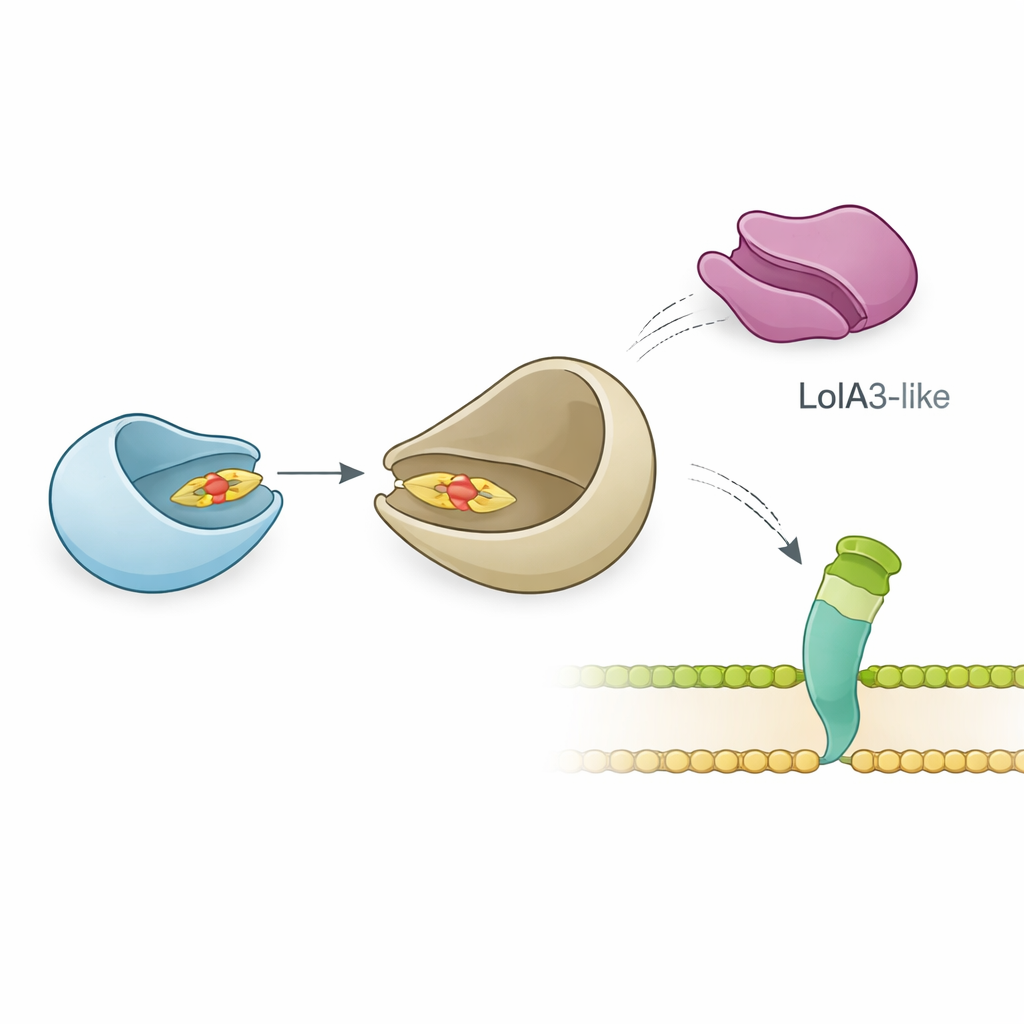
Överraskande flexibilitet i ytsamansättningen
Givet detta tydliga partnerskap förväntade sig forskarna att borttagning av LolB-PG skulle allvarligt störa bakteriens yttre membran. För att testa detta tog de bort genen pgn0994 och undersökte om bakterien fortfarande kunde bygga sina långa ytfibrer, kallade fimbriae, som delvis består av lipoproteiner. Överraskande nog växte mutanten normalt och bildade fimbriae som såg ut och fungerade mycket likt dem hos de omodifierade bakterierna. Nyckelkomponenter i fimbriae bearbetades fortfarande korrekt, transporterades till höljet och monterades till polymerer. Detta tyder på att, åtminstone under de laboratorieförhållanden som testades, kan P. gingivalis använda alternativa vägar för att flytta dessa lipoproteiner, eller att andra system träder in för att kompensera när LolB-PG saknas.
Vad detta betyder för framtida behandlingar
Denne studie visar att P. gingivalis faktiskt bär på ett funktionellt LolB-liknande protein som bildar ett specifikt partnerskap med sin huvudsakliga LolA-chaperon, och bevarar ett grundläggande steg i lipoproteintransport som ses över många bakterier. Samtidigt pekar LolB-PG:s förstorade bindningsfåra, dess selektiva parning och avsaknaden av uppenbara defekter när proteinet tas bort mot ett mer flexibelt och diversifierat transportsystem än man tidigare trott. För icke-specialister är budskapet att även mycket konserverade bakteriesystem kan omformas i olika arter, vilket kan påverka hur väl antibiotikastrategier översätts från en patogen till en annan. Att kartlägga dessa variationer i detalj blir avgörande för att utforma läkemedel som kan oskadliggöra skadliga bakterier som P. gingivalis utan att i stor utsträckning skada de nyttiga mikrober vi är beroende av.
Citering: Jaiman, D., Hirohata, M., Hasegawa, Y. et al. Identification of a LolB-like protein in Porphyromonas gingivalis reveals selective LolA–LolB pairing. Sci Rep 16, 13157 (2026). https://doi.org/10.1038/s41598-026-49975-1
Nyckelord: lipoproteintransport, Porphyromonas gingivalis, LolA LolB-systemet, bakteriens yttre membran, antibiotiska mål