Clear Sky Science · ar
تحديد بروتين شبيه بـ LolB في Porphyromonas gingivalis يكشف اقترانًا انتقائيًا بين LolA وLolB
لماذا يهم هذا البكتيريا الفموية
يعرف معظم الناس Porphyromonas gingivalis كعامل مسبب لمشاكل اللثة، لكن هذه الميكروبة ارتبطت أيضًا بحالات مثل مرض ألزهايمر والتهاب المفاصل الروماتويدي. للبقاء، تعتمد على نظام شحن متقن ينقل بروتينات معينة تُسمى البروتينات الدهنية إلى سطحها الخارجي. تساعد هذه البروتينات الدهنية البكتيريا في بناء قشرتها الواقية والتفاعل مع أجسامنا. فهم كيف يعمل هذا النظام الخاص بالنقل لا يضيء فقط بيولوجيا بكتيرية أساسية، بل قد يكشف أيضًا نقاط ضعف جديدة للمضادات الحيوية التي تحمي الميكروبات المفيدة لدينا.
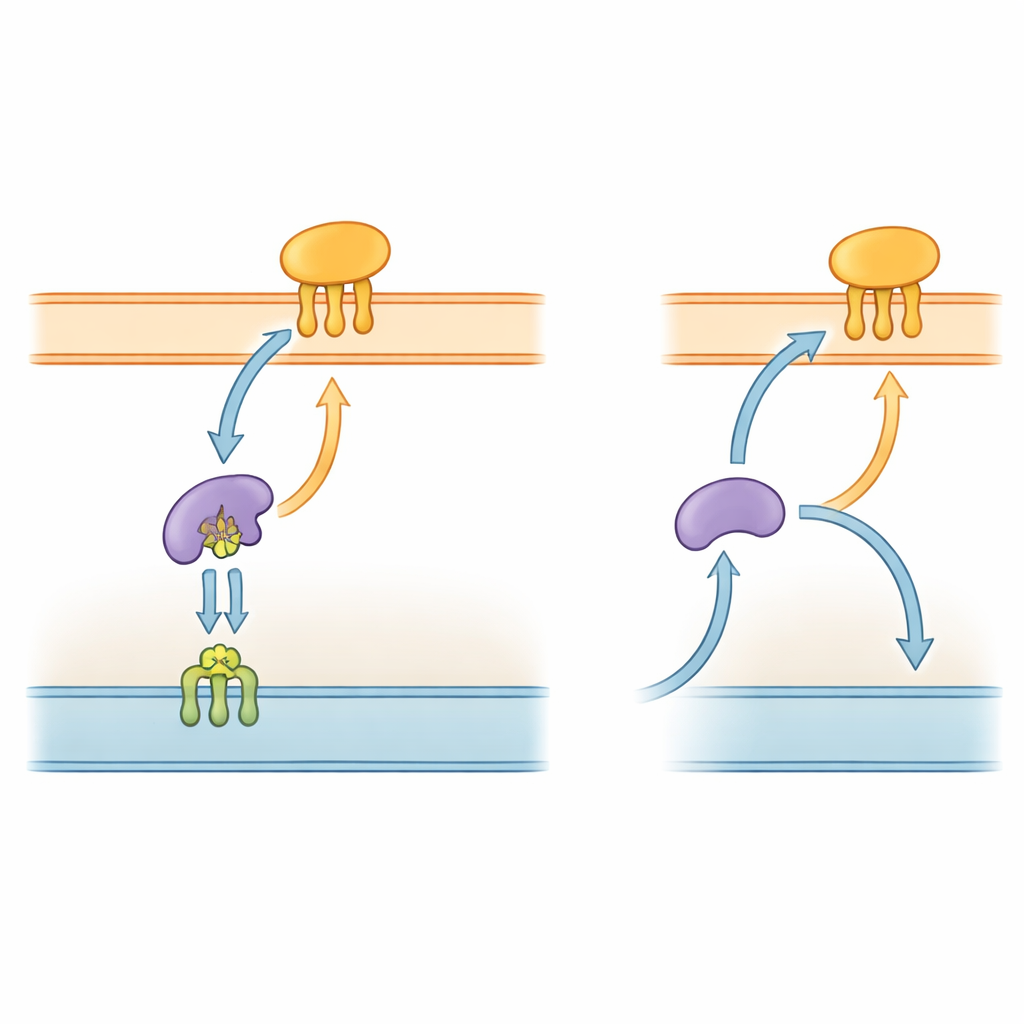
الطريق السريع البروتيني البكتيري
البكتيريا سالبة الجرام، بما في ذلك P. gingivalis، ملفوفة في غلاف معقد يتكوّن من غشائين ومساحة مائية بينهما. كثير من أدواتها الرئيسية هي بروتينات دهنية—بروتينات مرتبطة بالأغشية بواسطة سلاسل دهنية قصيرة. في أنواع مُدرسة جيدًا مثل Escherichia coli، نظام مكوّن من خمسة أجزاء يُدعى «Lol» ينقل هذه البروتينات الدهنية من الغشاء الداخلي عبر الحيز المحيطي إلى الغشاء الخارجي. أحد المكونات، LolA، يعمل كنافلة في الحيز المحيطي، بينما يستقبل LolB في الغشاء الخارجي الحمولة ويُدخلها في الطبقة السطحية. ولأن مسار التسليم هذا أساسي لبناء الغشاء الخارجي، فإن أجزاء من نظام Lol تُستكشف بالفعل كأهداف لمضادات حيوية جديدة.
جزء مفقود لم يكن مفقودًا حقًا
لسنوات، اعتقد الباحثون أن P. gingivalis والعديد من أقاربها في مجموعة Bacteroidota تفتقر تمامًا إلى LolB. وكان هذا يثير لغزًا: كيف كانت هذه البكتيريا تُدرج البروتينات الدهنية في غشائها الخارجي؟ باستخدام أدوات توقع البنية الحديثة (مثل AlphaFold) وتجارب متابعة، حدّد المؤلفون مرشحًا طال انتظاره في P. gingivalis، وهو بروتين يُشفَّر بواسطة الجين pgn0994. وأظهروا أن هذا البروتين، الذي أطلقوا عليه LolB-PG، يطوى بطريقة تشبه تقريبًا بروتينات LolB المعروفة من بكتيريا أخرى، رغم اختلاف تسلسله الأميني إلى حد كبير. كشف شكله ثلاثي الأبعاد عن ورقة منحنية تُكوّن أخدودًا عميقًا، شكل ملائم لاحتضان الذيل الدهني للبروتين الدهني.
شراكة جزيئية مفصلة حسب الطلب
تابع الفريق فحص كيف يتفاعل LolB-PG مع شريكه المرجح، LolA، الذي ينقل البروتينات الدهنية عبر الحيز المحيطي. أظهرت قياسات فيزيوكيميائية دقيقة أن LolB-PG يرتبط بقوة وبانتقائية مع بروتين LolA الرئيسي في P. gingivalis، بميل مشابه لأزواج LolA–LolB الكلاسيكية في E. coli وبكتيريا أخرى. بالمقابل، بالكاد يتفاعل LolB-PG مع بروتين شبيه بـ LolA ثانٍ في P. gingivalis يُدعى LolA3، أو مع LolA من أنواع أخرى. اقترحت نمذجة بنيوية سبب ذلك: يركب LolB-PG وLolA الأساسيان معًا بطريقة «فم إلى فم»، محاذين أخاديدهما بحيث يمكن لذيل الليبيد الانزلاق من أحدهما إلى الآخر، بينما يقدم LolA3 سطحًا غير متطابق. تشير هذه النتائج إلى اقتران انتقائي حيث لكل بروتين دور مخصص بدلًا من تفاعل واحد يناسب الجميع.
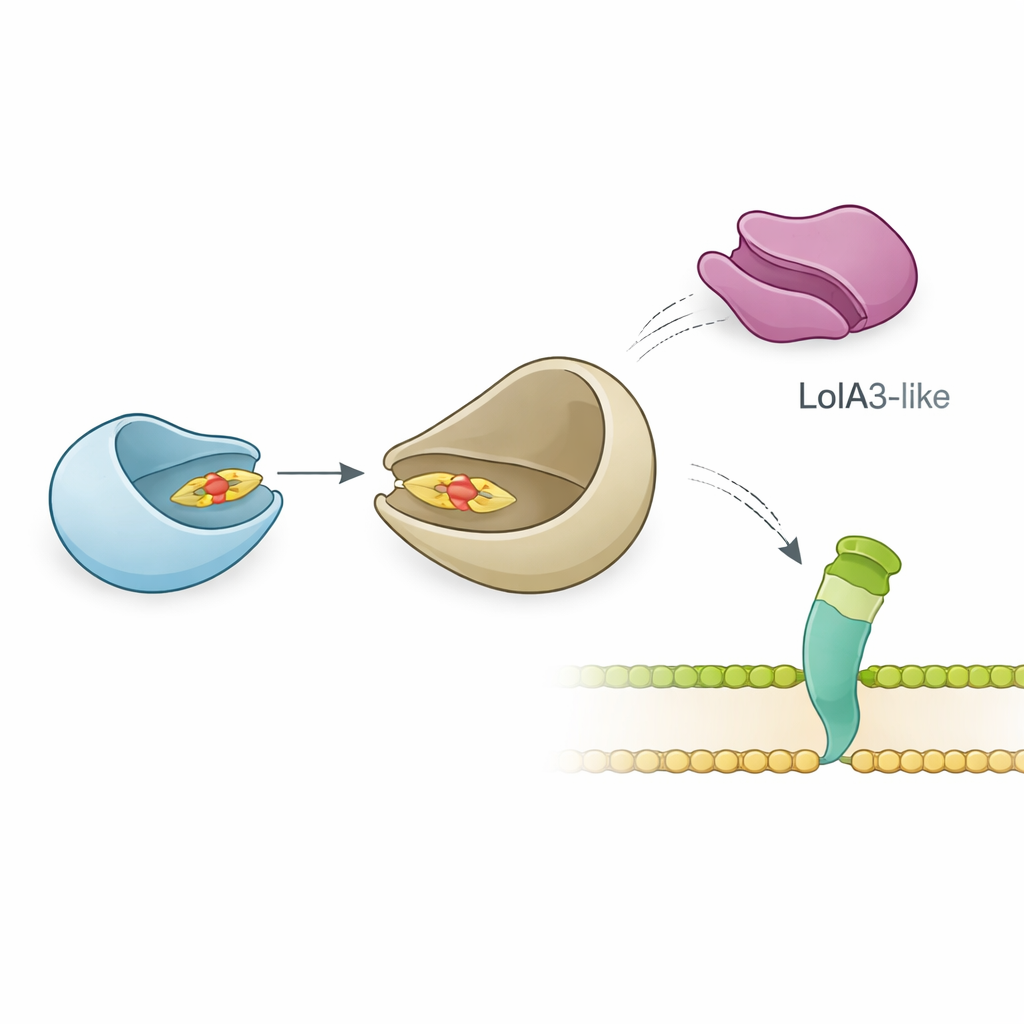
مرونة مفاجئة في تجميع السطح
نظرًا إلى هذه الشراكة الواضحة، توقع الباحثون أن حذف LolB-PG سيعطل الغشاء الخارجي للبكتيريا بشكل خطير. لاختبار ذلك، حذفوا جين pgn0994 وفحصوا ما إذا كانت البكتيريا لا تزال قادرة على بناء أليافها السطحية الطويلة، المسماة الزغابات (fimbriae)، التي تُصنع جزئيًا من بروتينات دهنية. والمفاجأة أن السلالة الطافرة نمت بشكل طبيعي وشكلت زغابات بدت وتصرّفت بشكل مشابه لتلك في البكتيريا غير المعدلة. استمرت مكوّنات الزغابات الرئيسية في المعالجة المناسبة، والنقل إلى الغلاف، والتجمع إلى سلاسل بوليمرية. يشير هذا إلى أنه، على الأقل في ظروف المختبر المختبرة، يمكن لـ P. gingivalis أن تستخدم مسارات بديلة لنقل هذه البروتينات الدهنية، أو أن أنظمة أخرى تتدخل لتعويض غياب LolB-PG.
ماذا يعني هذا للعلاجات المستقبلية
يُظهر هذا العمل أن P. gingivalis تحمل في الواقع بروتينًا وظيفيًا شبيهًا بـ LolB يشكل شراكة محددة مع حاميه الرئيسي LolA، محافظًا على خطوة نقل البروتينات الدهنية الأساسية التي تُرى عبر العديد من البكتيريا. وفي الوقت نفسه، يشير اتساع أخدود الربط في LolB-PG، وانتقائية الاقتران، وعدم وجود عيوب واضحة عند إزالة البروتين، إلى شبكة نقل أكثر مرونة وتنوّعًا مما كان يُعتقد سابقًا. للقراء غير المتخصصين، الخلاصة أن حتى الأنظمة البكتيرية المحافظة بشدة يمكن إعادة تشكيلها في أنواع مختلفة، وهو ما قد يؤثر على مدى قابلية استنساخ استراتيجيات المضادات الحيوية من ممرض إلى آخر. سيكون رسم هذه الاختلافات بتفصيل أمرًا حاسمًا لتصميم أدوية تعطل البكتيريا الضارة مثل P. gingivalis دون الإضرار على نطاق واسع بالميكروبات المفيدة التي نعتمد عليها.
الاستشهاد: Jaiman, D., Hirohata, M., Hasegawa, Y. et al. Identification of a LolB-like protein in Porphyromonas gingivalis reveals selective LolA–LolB pairing. Sci Rep 16, 13157 (2026). https://doi.org/10.1038/s41598-026-49975-1
الكلمات المفتاحية: نقل البروتين الدهني, Porphyromonas gingivalis, نظام LolA LolB, الغشاء الخارجي البكتيري, أهداف مضادات الميكروبات