Clear Sky Science · nl
Identificatie van een LolB-achtig eiwit in Porphyromonas gingivalis toont selectieve LolA–LolB-koppeling
Waarom deze mondbacterie ertoe doet
De meeste mensen kennen Porphyromonas gingivalis als een boosdoener bij tandvleesontsteking, maar deze microbe wordt ook in verband gebracht met aandoeningen zoals de ziekte van Alzheimer en reumatoïde artritis. Om te overleven is hij afhankelijk van een verfijnd transportsysteem dat bepaalde eiwitten, lipoproteïnen genoemd, naar zijn buitenzijde brengt. Deze lipoproteïnen helpen de bacterie zijn beschermende laag op te bouwen en met ons lichaam te interageren. Begrijpen hoe dit transportsysteem werkt werpt niet alleen licht op fundamentele bacteriële biologie, het kan ook nieuwe kwetsbaarheden voor antibiotica blootleggen die onze nuttige microben sparen.
De eiwit-snelweg van bacteriën
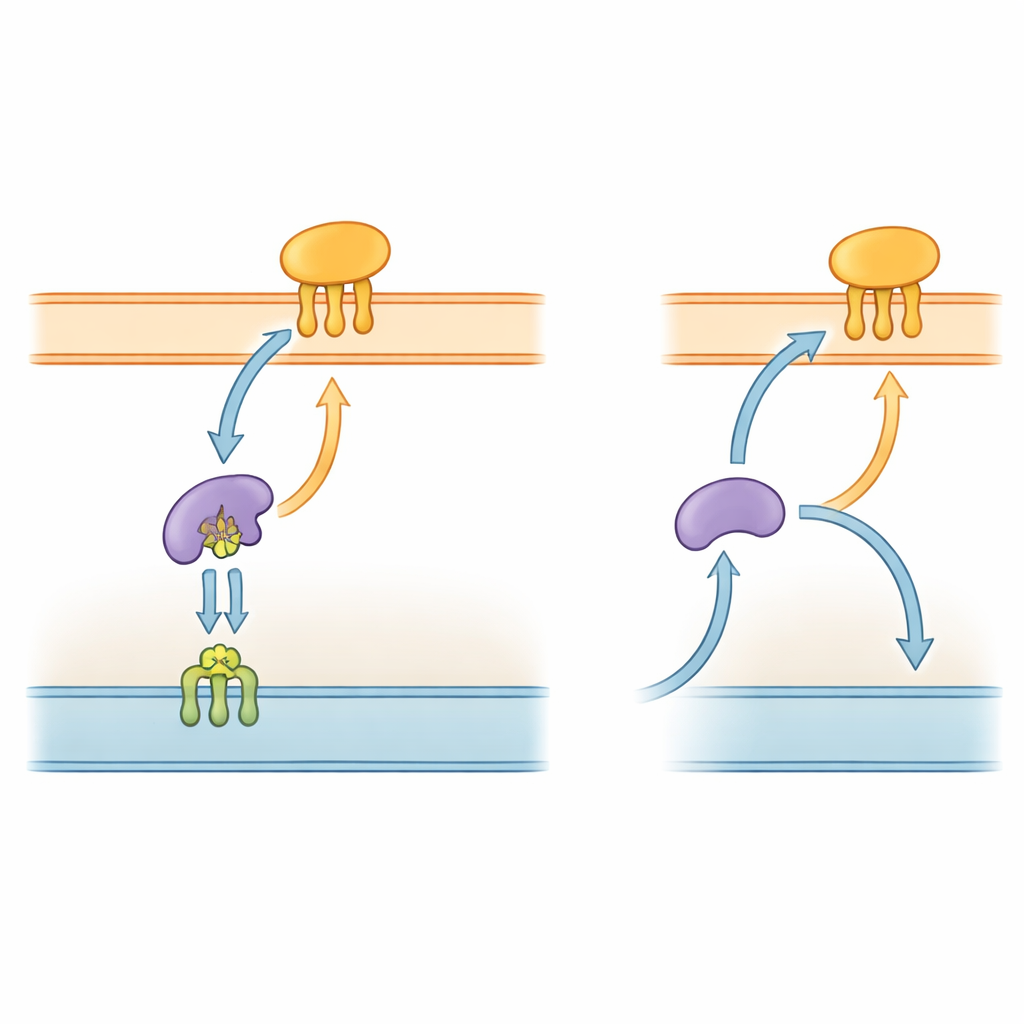
Gramnegatieve bacteriën, waaronder P. gingivalis, zijn omhuld door een complexe envelop met twee membranen en een waterige ruimte daartussen. Veel van hun belangrijkste instrumenten zijn lipoproteïnen—eiwitten verankerd in membranen door korte vetachtige ketens. In goed bestudeerde soorten zoals Escherichia coli transporteert een vijfdelig “Lol”-systeem deze lipoproteïnen van het binnenmembraan, door de periplasmatische ruimte, naar het buitenmembraan. Eén component, LolA, fungeert als een pendel in het periplasma, terwijl LolB in het buitenmembraan de lading ontvangt en in de buitenlaag invoegt. Omdat dit afleveringspad essentieel is voor de opbouw van het buitenmembraan, worden onderdelen van het Lol-systeem al onderzocht als potentiële doelen voor nieuwe antibiotica.
Een missend onderdeel dat eigenlijk niet ontbrak
Jarenlang dachten onderzoekers dat P. gingivalis en veel van zijn verwanten in de Bacteroidota-groep helemaal geen LolB hadden. Dat riep een vraag op: hoe slaagden deze bacteriën erin lipoproteïnen in hun buitenmembraan in te voegen? Met moderne structuurvoorspellende hulpmiddelen (zoals AlphaFold) en vervolgexperimenten identificeerden de auteurs een lang gezochte kandidaat in P. gingivalis: een eiwit gecodeerd door het gen pgn0994. Ze toonden aan dat dit eiwit, dat ze LolB-PG noemen, bijna op dezelfde manier opvouwt als bekende LolB-eiwitten van andere bacteriën, hoewel de aminozuursequentie behoorlijk verschilt. De driedimensionale structuur onthulde een gebogen plaat die een diepe groef vormt, een vorm die goed geschikt is om de vette staart van een lipoproteïne te omsluiten.
Een op maat gemaakte moleculaire samenwerking
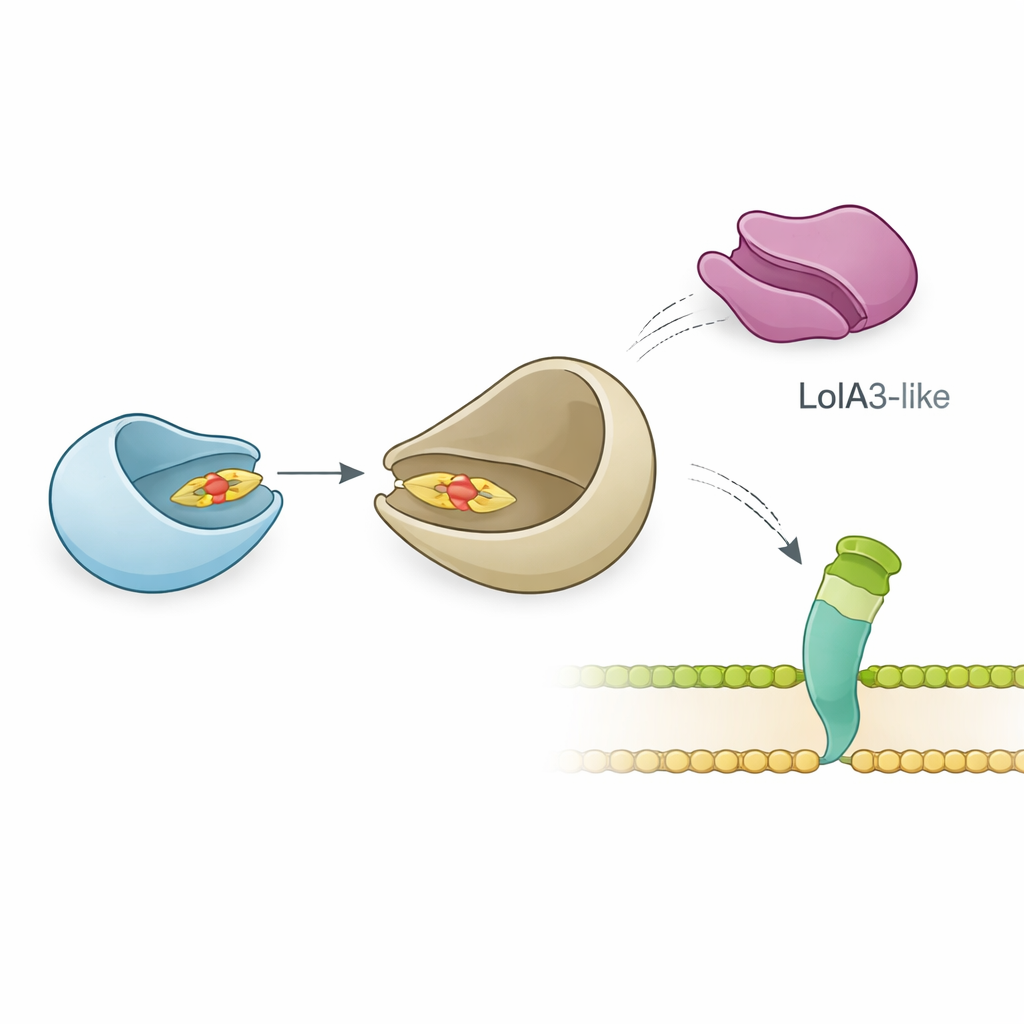
Het team onderzocht vervolgens hoe LolB-PG interageert met zijn waarschijnlijke partner, LolA, die lipoproteïnen door het periplasma vervoert. Nauwkeurige biofysische metingen toonden aan dat LolB-PG sterk en specifiek bindt aan het belangrijkste LolA-eiwit van P. gingivalis, met een affiniteit die vergelijkbaar is met klassieke LolA–LolB-paren in E. coli en andere bacteriën. In tegenstelling daarmee heeft LolB-PG nauwelijks interactie met een tweede LolA-achtig eiwit in P. gingivalis, genaamd LolA3, of met LolA uit andere soorten. Structurele modellering suggereerde waarom: LolB-PG en het primaire LolA sluiten aan in een “mond-tot-mond”-configuratie, waarbij hun groeven op één lijn liggen zodat de lipidevacht van het ene naar het andere kan glijden, terwijl LolA3 een niet-passend oppervlak presenteert. Deze resultaten wijzen op een selectieve koppeling waarbij elk eiwit een toegewijde rol heeft in plaats van een alles-in-één-interactie.
Verrassende flexibiliteit bij opbouw van het oppervlak
Gezien deze duidelijke samenwerking verwachtten de onderzoekers dat het verwijderen van LolB-PG het buitenmembraan van de bacterie ernstig zou verstoren. Om dit te testen verwijderden ze het pgn0994-gen en onderzochten of de bacterie nog steeds zijn lange oppervlaktevezels, fimbriae genoemd, kon opbouwen—structuren die deels uit lipoproteïnen bestaan. Verrassend genoeg groeide de gemuteerde stam normaal en vormde fimbriae die er qua uiterlijk en gedrag sterk op die van de ongewijzigde bacteriën leken. Belangrijke fimbriale componenten werden nog steeds correct verwerkt, naar de envelop getransporteerd en in polymeren geassembleerd. Dit suggereert dat P. gingivalis, althans onder de geteste laboratoriumomstandigheden, alternatieve routes kan gebruiken om deze lipoproteïnen te verplaatsen, of dat andere systemen inspringen om te compenseren wanneer LolB-PG ontbreekt.
Wat dit betekent voor toekomstige behandelingen
Dit werk toont aan dat P. gingivalis wel degelijk een functioneel LolB-achtig eiwit draagt dat een specifieke samenwerking aangaat met zijn belangrijkste LolA-chaperonne, waarmee een fundamentele stap van lipoproteïnentransport behouden blijft die bij veel bacteriën voorkomt. Tegelijk wijzen de vergrote bindingsgroef van LolB-PG, de selectieve koppeling en het gebrek aan duidelijke defecten bij verwijdering van het eiwit allemaal op een flexibeler en gevarieerder transportsysteem dan eerder werd aangenomen. Voor niet-specialisten is de kernboodschap dat zelfs sterk geconserveerde bacteriële systemen in verschillende soorten op andere manieren kunnen worden ingericht, wat invloed kan hebben op hoe succesvol antibiotische strategieën van de ene pathogeen op de andere zijn over te dragen. Het in kaart brengen van deze variaties in detail is cruciaal voor het ontwerpen van geneesmiddelen die schadelijke bacteriën zoals P. gingivalis kunnen uitschakelen zonder de nuttige microben waarop wij vertrouwen, breed te schaden.
Bronvermelding: Jaiman, D., Hirohata, M., Hasegawa, Y. et al. Identification of a LolB-like protein in Porphyromonas gingivalis reveals selective LolA–LolB pairing. Sci Rep 16, 13157 (2026). https://doi.org/10.1038/s41598-026-49975-1
Trefwoorden: lipoproteïnentransport, Porphyromonas gingivalis, LolA LolB-systeem, bacteriële buitenmembraan, antibiotica-doelwitten