Clear Sky Science · it
Identificazione di una proteina simile a LolB in Porphyromonas gingivalis rivela un accoppiamento selettivo LolA–LolB
Perché questo batterio orale conta
La maggior parte delle persone conosce Porphyromonas gingivalis come un protagonista della malattia parodontale, ma questo microbo è stato collegato anche a patologie come l’Alzheimer e l’artrite reumatoide. Per sopravvivere dipende da un sofisticato sistema di trasporto che sposta certe proteine, chiamate lipoproteine, verso la sua superficie esterna. Queste lipoproteine aiutano il batterio a costruire la sua corazza protettiva e a interagire con il nostro organismo. Capire come funziona questo sistema di trasporto non solo illumina aspetti fondamentali della biologia batterica, ma può anche rivelare nuovi punti deboli per antibiotici che risparmino i microbi utili.
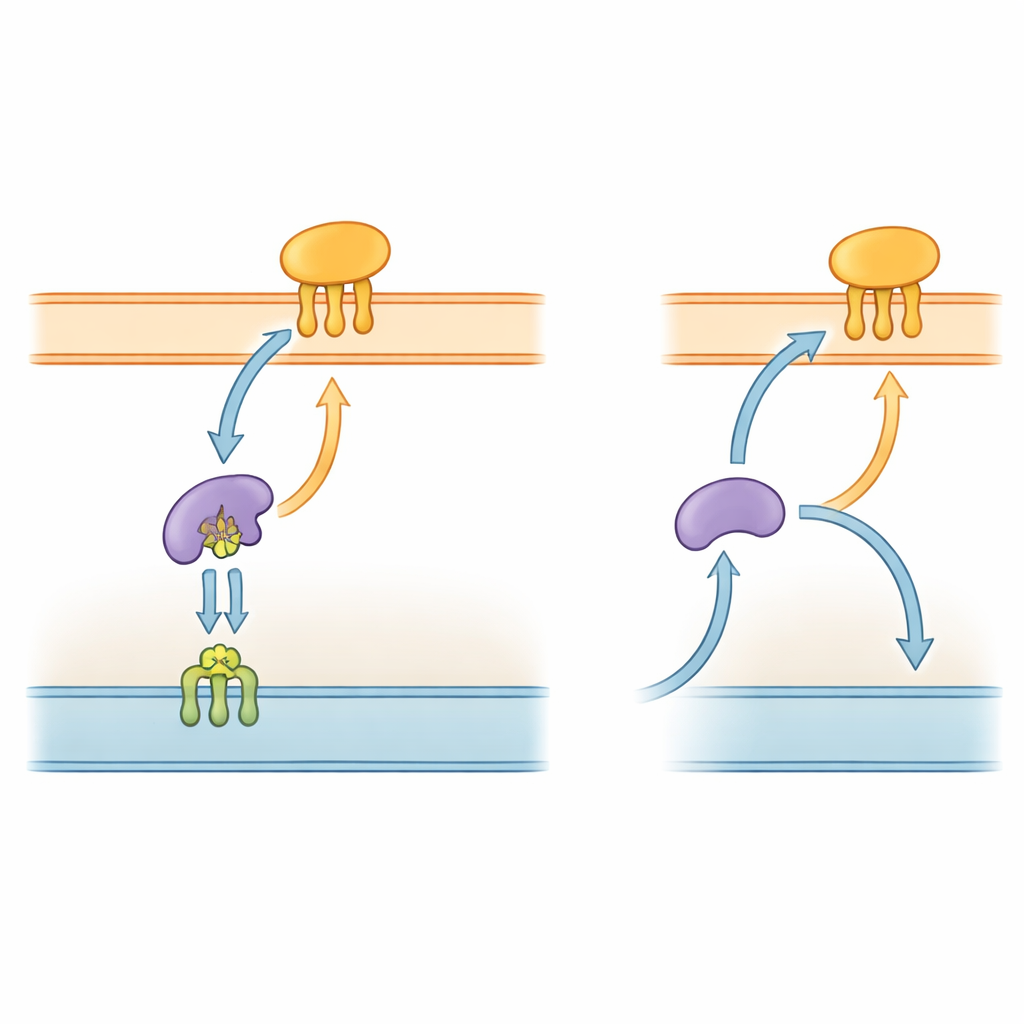
L’autostrada proteica batterica
I batteri Gram-negativi, inclusa P. gingivalis, sono avvolti in un involucro complesso con due membrane e uno spazio acquoso intermedio. Molti dei loro strumenti chiave sono lipoproteine—proteine ancorate alle membrane da catene corte di tipo lipidico. In specie ben studiate come Escherichia coli, un sistema “Lol” formato da cinque componenti trasporta queste lipoproteine dalla membrana interna, attraverso il periplasma, fino alla membrana esterna. Un componente, LolA, agisce come uno shuttle nel periplasma, mentre LolB nella membrana esterna riceve il carico e lo inserisce nello strato superficiale. Poiché questa via di consegna è essenziale per costruire la membrana esterna, alcune parti del sistema Lol sono già esplorate come bersagli per nuovi antibiotici.
Una parte mancante che in realtà non era scomparsa
Per anni i ricercatori hanno pensato che P. gingivalis e molti suoi parenti del gruppo Bacteroidota fossero privi di LolB. Ciò sollevava un enigma: come riuscivano questi batteri a inserire le lipoproteine nella membrana esterna? Utilizzando strumenti moderni di predizione strutturale (come AlphaFold) e esperimenti di follow-up, gli autori hanno identificato un candidato a lungo ricercato in P. gingivalis, una proteina codificata dal gene pgn0994. Hanno dimostrato che questa proteina, che chiamano LolB-PG, si ripiega in modo quasi identico alle note proteine LolB di altri batteri, nonostante la sua sequenza aminoacidica sia abbastanza diversa. La sua struttura tridimensionale ha rivelato un foglio curvato che forma una profonda solcatura, una forma adatta ad accogliere la coda lipidica di una lipoproteina.
Un partenariato molecolare su misura
Il gruppo ha poi esaminato come LolB-PG interagisce con il suo probabile partner, LolA, che trasporta le lipoproteine attraverso il periplasma. Misurazioni biofisiche precise hanno mostrato che LolB-PG si lega in modo forte e specifico alla principale proteina LolA di P. gingivalis, con un’affinità simile a quella dei classici accoppiamenti LolA–LolB in E. coli e in altri batteri. Al contrario, LolB-PG interagisce a malapena con una seconda proteina di tipo LolA in P. gingivalis, chiamata LolA3, o con LolA di altre specie. Il modellamento strutturale suggerisce il perché: LolB-PG e la LolA principale si incastrano in modo “bocca‑a‑bocca”, allineando le loro solcature così che la coda lipidica possa scorrere da una all’altra, mentre LolA3 presenta una superficie non compatibile. Questi risultati indicano un accoppiamento selettivo in cui ogni proteina ha un ruolo dedicato piuttosto che un’interazione universale.
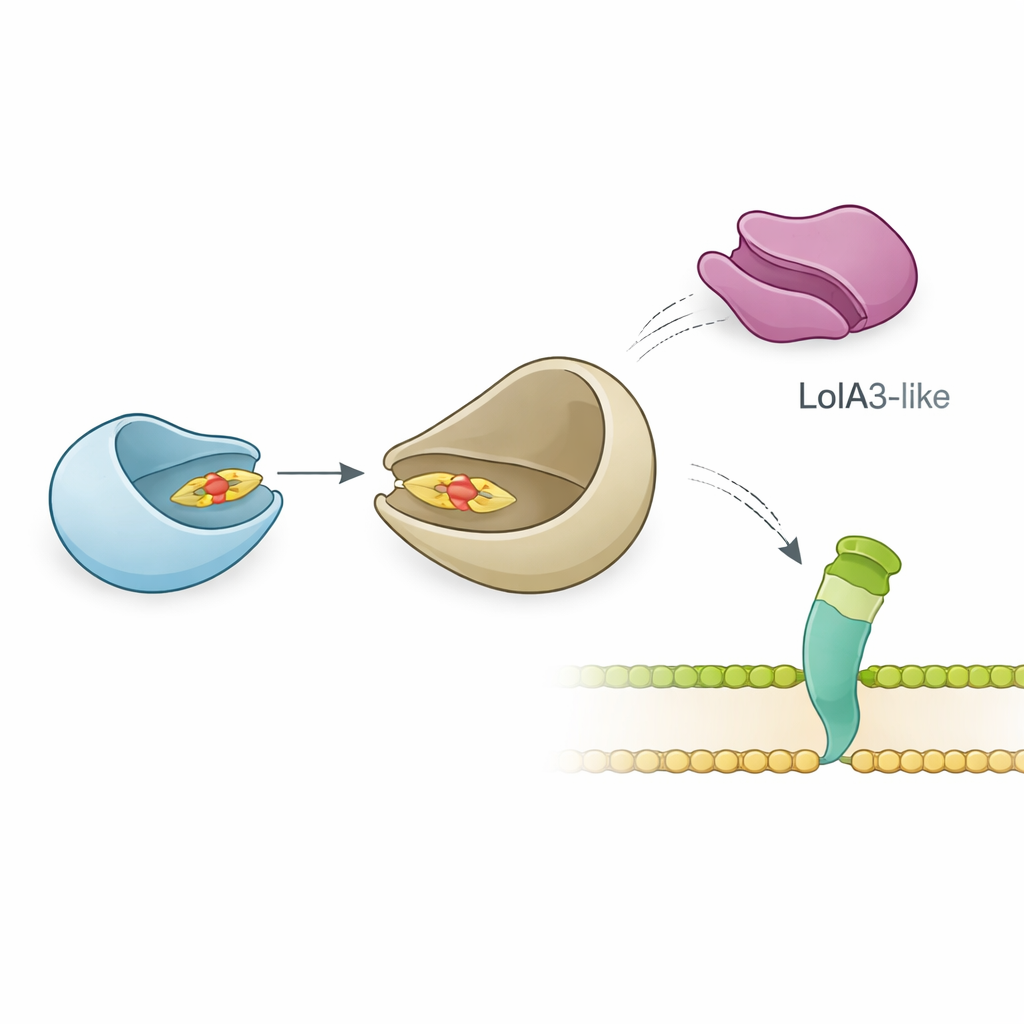
Sorprendente flessibilità nell’assemblaggio della superficie
Dato questo chiaro partenariato, i ricercatori si aspettavano che la rimozione di LolB-PG perturbasse seriamente la membrana esterna del batterio. Per verificarlo, hanno cancellato il gene pgn0994 ed esaminato se il batterio fosse ancora in grado di costruire le sue lunghe fibre superficiali, chiamate fimbrie, che sono in parte costituite da lipoproteine. Sorprendentemente, il ceppo mutante è cresciuto normalmente e ha formato fimbrie che apparivano e si comportavano in modo molto simile a quelle dei batteri non modificati. I componenti chiave delle fimbrie erano ancora correttamente processati, trasportati all’involucro e assemblati in polimeri. Ciò suggerisce che, almeno nelle condizioni di laboratorio testate, P. gingivalis può usare rotte alternative per spostare queste lipoproteine, o che altri sistemi intervengono per compensare l’assenza di LolB-PG.
Cosa significa per i trattamenti futuri
Questo lavoro mostra che P. gingivalis possiede, di fatto, una proteina funzionale simile a LolB che forma un partenariato specifico con la sua principale chaperone LolA, preservando un fondamentale passaggio del trasporto delle lipoproteine osservato in molti batteri. Allo stesso tempo, la solcatura di legame ampliata di LolB-PG, il suo accoppiamento selettivo e la mancanza di difetti evidenti quando la proteina viene rimossa indicano un network di trasporto più flessibile e diversificato di quanto si ritenesse. Per i non specialisti, il messaggio principale è che anche sistemi batterici altamente conservati possono essere riorganizzati in specie diverse, il che può influenzare l’efficacia con cui strategie antibiotiche si trasferiscono da un patogeno a un altro. Mappare queste variazioni in dettaglio sarà cruciale per progettare farmaci in grado di disarmare batteri dannosi come P. gingivalis senza danneggiare ampiamente i microbi benefici di cui ci avvaliamo.
Citazione: Jaiman, D., Hirohata, M., Hasegawa, Y. et al. Identification of a LolB-like protein in Porphyromonas gingivalis reveals selective LolA–LolB pairing. Sci Rep 16, 13157 (2026). https://doi.org/10.1038/s41598-026-49975-1
Parole chiave: trasporto di lipoproteine, Porphyromonas gingivalis, sistema LolA LolB, <keyword>bersagli antibiotici