Clear Sky Science · de
Identifizierung eines LolB‑ähnlichen Proteins in Porphyromonas gingivalis zeigt selektive LolA–LolB‑Paarung
Warum dieses Mundbakterium wichtig ist
Die meisten Menschen kennen Porphyromonas gingivalis als Mitverursacher von Zahnfleischerkrankungen, doch dieses Mikroorganismus wurde auch mit Erkrankungen wie Alzheimer und rheumatoider Arthritis in Verbindung gebracht. Zum Überleben ist es auf ein ausgeklügeltes Transportsystem angewiesen, das bestimmte Proteine, sogenannte Lipoproteine, an seine Außenseite bringt. Diese Lipoproteine helfen dem Bakterium, seine Schutzschicht aufzubauen und mit unserem Körper zu interagieren. Das Verständnis dieses Transportsystems beleuchtet nicht nur grundlegende bakterielle Biologie, sondern kann auch neue Schwachstellen für Antibiotika offenbaren, die unsere nützlichen Mikroben schonen.
Die Proteinautobahn der Bakterien
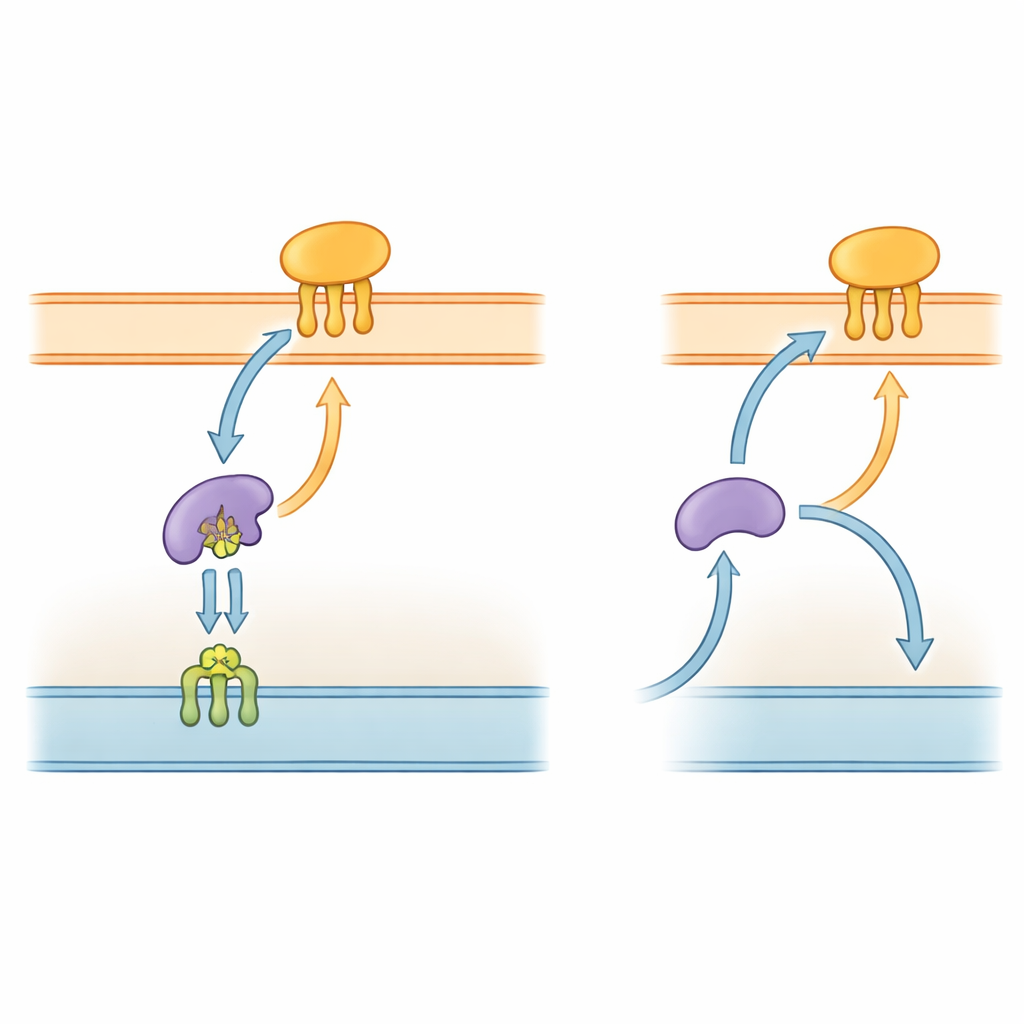
Gramnegative Bakterien, darunter P. gingivalis, sind in eine komplexe Hülle mit zwei Membranen und einem wässrigen Raum dazwischen eingebettet. Viele ihrer wichtigen Werkzeuge sind Lipoproteine—Proteine, die durch kurze fettähnliche Ketten an Membranen verankert sind. In gut untersuchten Arten wie Escherichia coli transportiert ein fünfteiliger „Lol“-Apparat diese Lipoproteine von der inneren Membran über den Periplasma‑Bereich in die äußere Membran. Eine Komponente, LolA, wirkt im Periplasma wie ein Shuttle, während LolB in der äußeren Membran die Fracht annimmt und in die Oberfläche einfügt. Da dieser Auslieferungsweg für den Aufbau der äußeren Membran essenziell ist, werden Teile des Lol‑Systems bereits als Ansatzpunkte für neue Antibiotika untersucht.
Ein fehlendes Teil, das in Wahrheit nicht fehlte
Jahrelang nahmen Forscher an, dass P. gingivalis und viele seiner Verwandten in der Gruppe der Bacteroidota ganz auf LolB verzichten. Das war rätselhaft: Wie schafften es diese Bakterien, Lipoproteine in ihre äußere Membran einzubauen? Mithilfe moderner Struktur‑Vorhersagewerkzeuge (etwa AlphaFold) und anschließenden Experimenten identifizierten die Autoren in P. gingivalis nun einen lange gesuchten Kandidaten—ein von dem Gen pgn0994 kodiertes Protein. Sie zeigten, dass dieses Protein, das sie LolB‑PG nennen, sich nahezu genauso faltet wie bekannte LolB‑Proteine aus anderen Bakterien, obwohl seine Aminosäuresequenz recht unterschiedlich ist. Seine dreidimensionale Struktur enthüllte ein gebogenes Blatt, das eine tiefe Rinne bildet—eine Form, die sich gut eignet, um den fetten Schwanz eines Lipoproteins aufzunehmen.
Eine maßgeschneiderte molekulare Partnerschaft
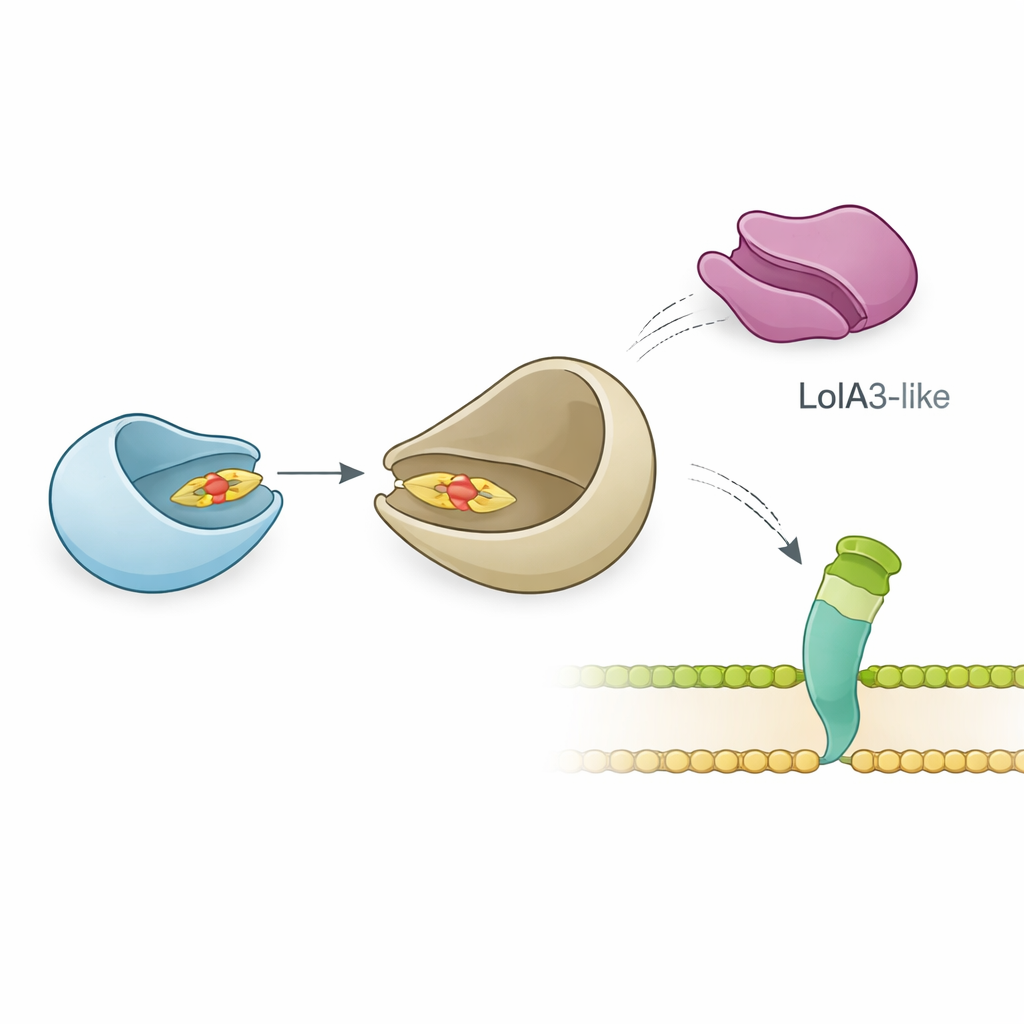
Das Team untersuchte anschließend, wie LolB‑PG mit seinem wahrscheinlichen Partner LolA interagiert, der Lipoproteine durch das Periplasma transportiert. Präzise biophysikalische Messungen zeigten, dass LolB‑PG stark und spezifisch an das Haupt‑LolA von P. gingivalis bindet, mit einer Affinität, die klassischen LolA–LolB‑Paaren in E. coli und anderen Bakterien ähnelt. Im Gegensatz dazu interagiert LolB‑PG kaum mit einem zweiten LolA‑ähnlichen Protein in P. gingivalis, genannt LolA3, oder mit LolA aus anderen Arten. Strukturmodelle lieferten eine Erklärung: LolB‑PG und das primäre LolA docken in einer „Mund‑zu‑Mund“-Anordnung aneinander an, sodass sich ihre Rinnen ausrichten und der Lipid‑Schwanz von einem zum anderen gleiten kann, während LolA3 eine unpassende Oberfläche bietet. Diese Ergebnisse deuten auf eine selektive Paarung hin, bei der jedes Protein eine dedizierte Rolle hat, statt in beliebiger Kombination zu funktionieren.
Unerwartete Flexibilität beim Aufbau der Oberfläche
Angesichts dieser klaren Partnerschaft erwarteten die Forscher, dass das Entfernen von LolB‑PG die äußere Membran des Bakteriums stark stören würde. Um das zu prüfen, löschten sie das Gen pgn0994 und untersuchten, ob das Bakterium noch seine langen Oberflächenfasern, die Fimbrien, bilden kann—diese bestehen teilweise aus Lipoproteinen. Überraschenderweise wuchs der Mutant normal und bildete Fimbrien, die in Aussehen und Verhalten denen der unveränderten Bakterien sehr ähnlich waren. Wichtige fimbriale Komponenten wurden weiterhin korrekt prozessiert, zur Hülle transportiert und zu Polymeren zusammengebaut. Das legt nahe, dass P. gingivalis—zumindest unter den getesteten Laborbedingungen—alternative Wege nutzen kann, um diese Lipoproteine zu bewegen, oder dass andere Systeme einspringen, wenn LolB‑PG fehlt.
Was das für künftige Behandlungen bedeutet
Diese Arbeit zeigt, dass P. gingivalis tatsächlich ein funktionales LolB‑ähnliches Protein trägt, das eine spezifische Partnerschaft mit seinem Haupt‑LolA‑Chaperon bildet und einen grundlegenden Schritt des Lipoproteintransports bewahrt, der in vielen Bakterien vorkommt. Gleichzeitig deuten die erweiterte Bindungsrinne von LolB‑PG, seine selektive Paarung und das Fehlen offensichtlicher Defekte beim Entfernen des Proteins auf ein flexibleres und diversifizierteres Transportsystem hin als bisher angenommen. Für Nichtfachleute lautet die Kernaussage: Selbst hochkonservierte bakterielle Systeme können in verschiedenen Arten umgestaltet sein, was beeinflussen kann, wie gut Antibiotika‑Strategien von einem Erreger auf einen anderen übertragbar sind. Das genaue Kartieren dieser Variationen wird entscheidend sein, um Wirkstoffe zu entwickeln, die schädliche Bakterien wie P. gingivalis außer Gefecht setzen, ohne die nützlichen Mikroben, auf die wir angewiesen sind, breit zu schädigen.
Zitation: Jaiman, D., Hirohata, M., Hasegawa, Y. et al. Identification of a LolB-like protein in Porphyromonas gingivalis reveals selective LolA–LolB pairing. Sci Rep 16, 13157 (2026). https://doi.org/10.1038/s41598-026-49975-1
Schlüsselwörter: Transport von Lipoproteinen, Porphyromonas gingivalis, LolA LolB System, bakterielle Außenmembran, Antibiotika‑Ziele