Clear Sky Science · es
Identificación de una proteína tipo LolB en Porphyromonas gingivalis revela un emparejamiento selectivo LolA–LolB
Por qué importa esta bacteria bucal
La mayoría de la gente conoce a Porphyromonas gingivalis como un causante de problemas en las encías, pero este microbio también se ha asociado con afecciones como el Alzheimer y la artritis reumatoide. Para sobrevivir, depende de un sofisticado sistema de envío que traslada ciertas proteínas, llamadas lipoproteínas, a su superficie externa. Estas lipoproteínas ayudan a la bacteria a construir su capa protectora e interactuar con nuestro organismo. Entender cómo funciona este sistema de transporte no solo aclara la biología bacteriana básica, sino que también puede revelar nuevas vulnerabilidades para antibióticos que respeten a los microbios beneficiosos.
La autopista proteica bacteriana
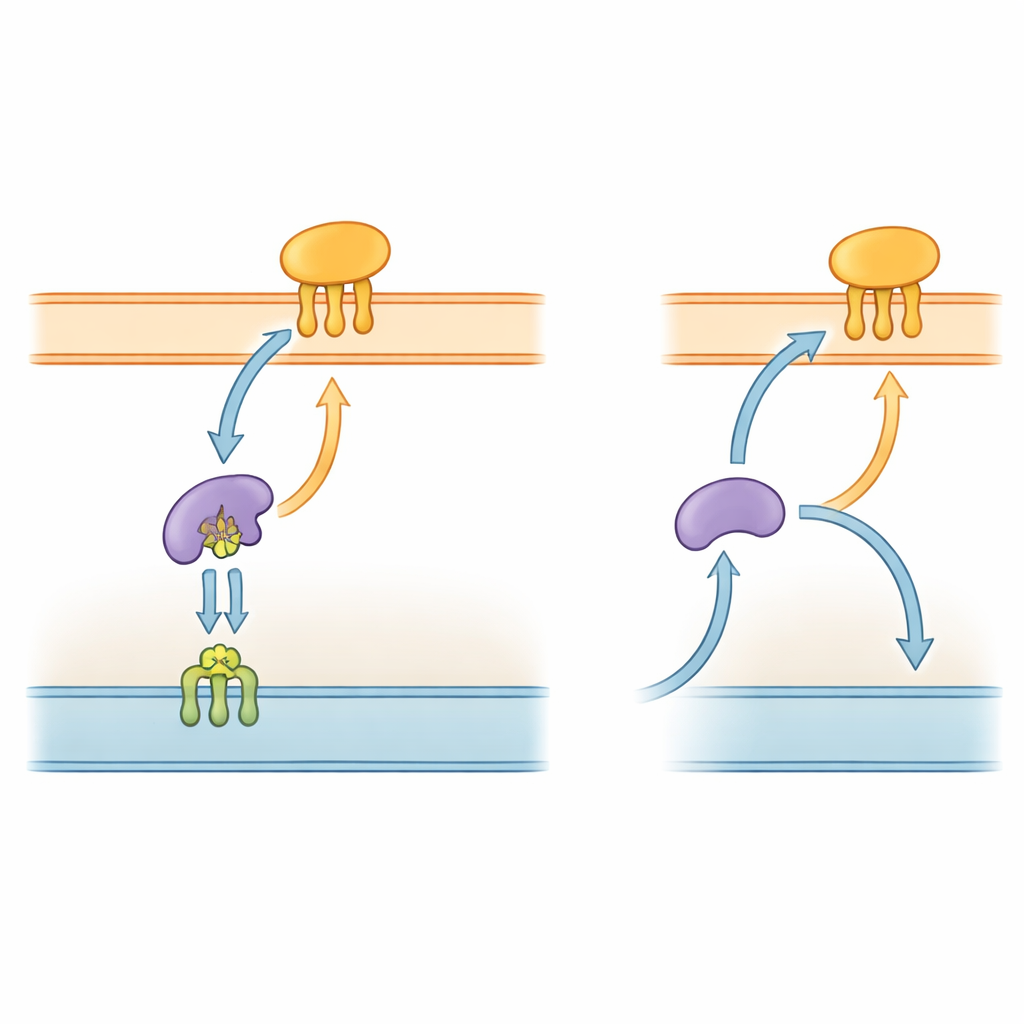
Las bacterias Gram negativas, incluida P. gingivalis, están envueltas en una envoltura compleja con dos membranas y un espacio acuoso intermedio. Muchas de sus herramientas clave son lipoproteínas: proteínas ancladas a las membranas por cadenas cortas de tipo graso. En especies bien estudiadas como Escherichia coli, un sistema de cinco componentes llamado “Lol” transporta estas lipoproteínas desde la membrana interna, a través del periplasma, hacia la membrana externa. Un componente, LolA, actúa como un transbordador en el periplasma, mientras que LolB en la membrana externa recibe la carga e la inserta en la capa superficial. Dado que esta vía de entrega es esencial para construir la membrana externa, partes del sistema Lol ya se exploran como dianas para nuevos antibióticos.
Una pieza faltante que en realidad no estaba perdida
Durante años, los investigadores pensaron que P. gingivalis y muchos de sus parientes del grupo Bacteroidota carecían por completo de LolB. Eso planteaba un enigma: ¿cómo insertaban estas bacterias las lipoproteínas en su membrana externa? Utilizando herramientas modernas de predicción estructural (como AlphaFold) y experimentos complementarios, los autores identificaron un candidato largamente buscado en P. gingivalis, una proteína codificada por el gen pgn0994. Demostraron que esta proteína, que denominan LolB-PG, se pliega de manera casi idéntica a las proteínas LolB conocidas de otras bacterias, a pesar de que su secuencia de aminoácidos es bastante diferente. Su estructura tridimensional reveló una hoja curva que forma una ranura profunda, una forma bien adaptada para acunar la cola lipídica de una lipoproteína.
Una asociación molecular a medida
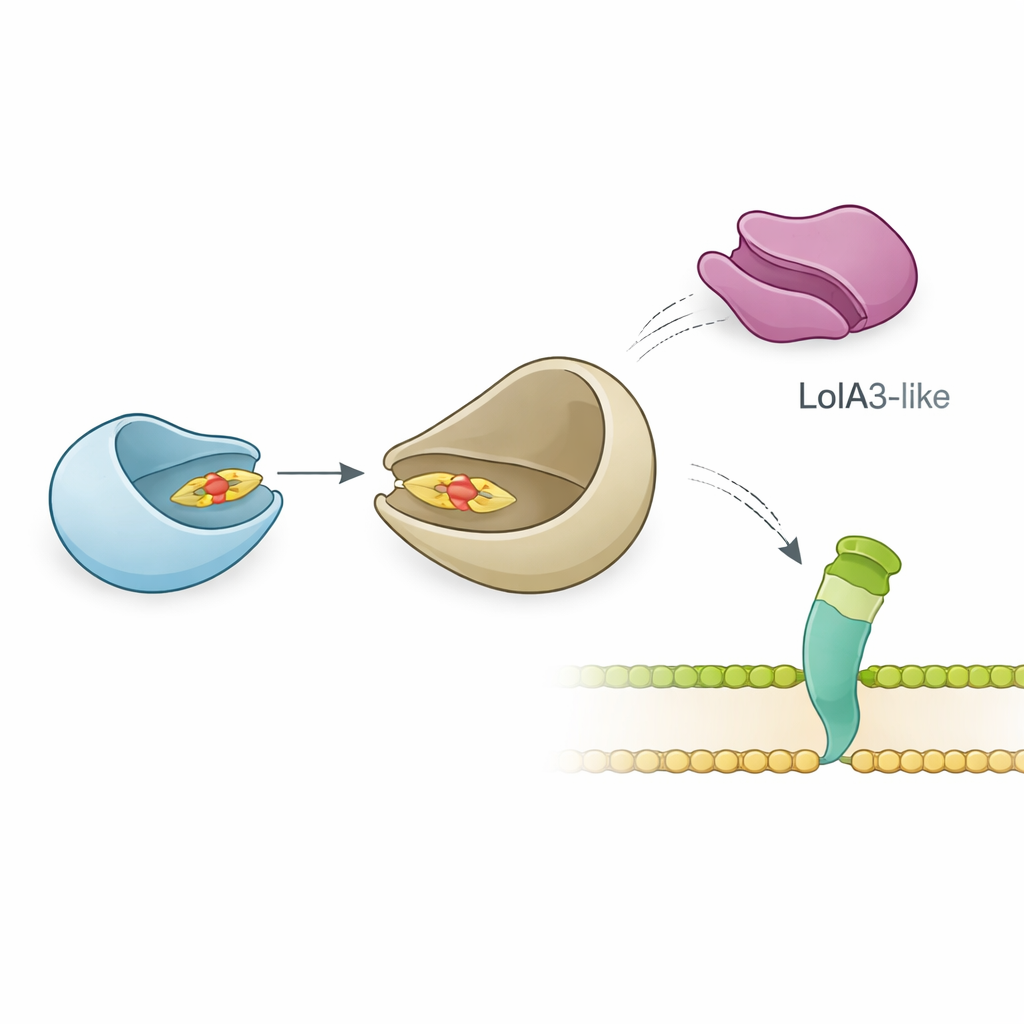
El equipo analizó cómo LolB-PG interactúa con su probable pareja, LolA, que transporta las lipoproteínas a través del periplasma. Mediciones biofísicas precisas demostraron que LolB-PG se une con fuerza y especificidad a la principal proteína LolA de P. gingivalis, con una afinidad similar a la de los pares clásicos LolA–LolB en E. coli y otras bacterias. En contraste, LolB-PG casi no interactúa con una segunda proteína tipo LolA en P. gingivalis, llamada LolA3, ni con LolA de otras especies. Modelos estructurales sugirieron el motivo: LolB-PG y la LolA principal encajan en una disposición “boca a boca”, alineando sus ranuras para que la cola lipídica pueda deslizarse de una a la otra, mientras que LolA3 presenta una superficie desajustada. Estos resultados apuntan a un emparejamiento selectivo en el que cada proteína tiene un papel dedicado en lugar de una interacción única para todos.
Sorprendente flexibilidad en el ensamblaje de la superficie
Dada esta asociación clara, los investigadores esperaban que eliminar LolB-PG perturbara seriamente la membrana externa de la bacteria. Para probarlo, suprimieron el gen pgn0994 y examinaron si la bacteria seguía pudiendo construir sus largas fibras superficiales, llamadas fimbrias, que están formadas en parte por lipoproteínas. Sorprendentemente, la cepa mutante creció con normalidad y formó fimbrias que parecían y se comportaban de forma muy parecida a las de las bacterias no modificadas. Los componentes clave de las fimbrias todavía se procesaron adecuadamente, se transportaron al envoltorio y se ensamblaron en polímeros. Esto sugiere que, al menos en las condiciones de laboratorio probadas, P. gingivalis puede usar rutas alternativas para mover estas lipoproteínas, o que otros sistemas intervienen para compensar cuando falta LolB-PG.
Qué implica esto para futuros tratamientos
Este trabajo demuestra que P. gingivalis sí porta una proteína funcional tipo LolB que forma una asociación específica con su chaperona LolA principal, preservando un paso fundamental del transporte de lipoproteínas presente en muchas bacterias. Al mismo tiempo, la ranura de unión ampliada de LolB-PG, su emparejamiento selectivo y la ausencia de defectos evidentes al eliminar la proteína apuntan a una red de transporte más flexible y diversificada de lo que se pensaba. Para los no especialistas, la conclusión es que incluso sistemas bacterianos muy conservados pueden reconfigurarse en distintas especies, lo que puede influir en la eficacia con la que las estrategias antibióticas se trasladan de un patógeno a otro. Cartografiar estas variaciones en detalle será crucial para diseñar fármacos capaces de desactivar bacterias dañinas como P. gingivalis sin perjudicar de forma general a los microbios beneficiosos de los que dependemos.
Cita: Jaiman, D., Hirohata, M., Hasegawa, Y. et al. Identification of a LolB-like protein in Porphyromonas gingivalis reveals selective LolA–LolB pairing. Sci Rep 16, 13157 (2026). https://doi.org/10.1038/s41598-026-49975-1
Palabras clave: transporte de lipoproteínas, Porphyromonas gingivalis, sistema LolA LolB, membrana externa bacteriana, objetivos antibióticos