Clear Sky Science · fr
Identification d’une protéine de type LolB chez Porphyromonas gingivalis révèle un appariement sélectif LolA–LolB
Pourquoi cette bactérie buccale compte
La plupart des gens connaissent Porphyromonas gingivalis comme un agent responsable des maladies des gencives, mais ce microbe a aussi été associé à des affections telles que la maladie d’Alzheimer et la polyarthrite rhumatoïde. Pour survivre, il dépend d’un système de transport sophistiqué qui déplace certaines protéines, appelées lipoprotéines, vers sa surface externe. Ces lipoprotéines aident la bactérie à construire son enveloppe protectrice et à interagir avec notre organisme. Comprendre le fonctionnement de ce système de transport éclaire non seulement la biologie bactérienne fondamentale, mais peut aussi révéler de nouvelles faiblesses exploitables par des antibiotiques qui épargnent nos microbes utiles.
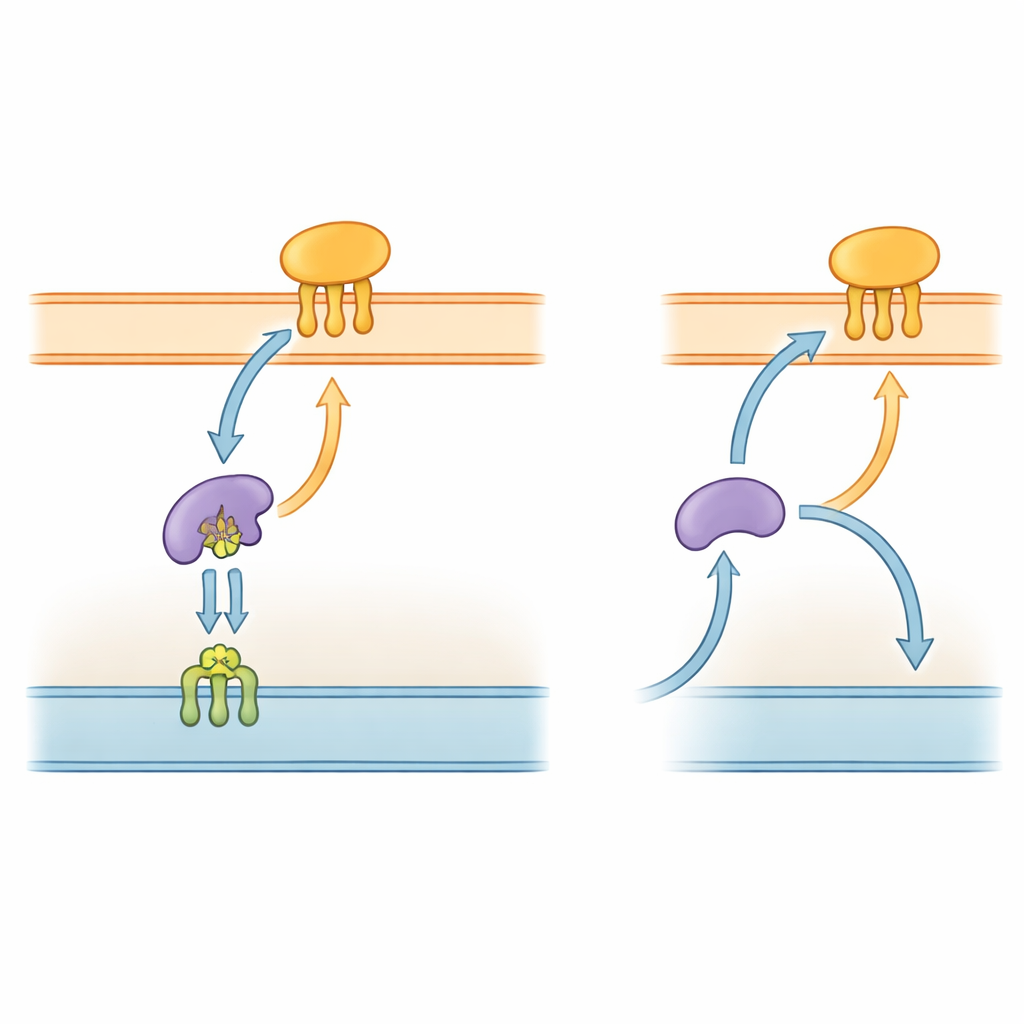
L’autoroute protéique bactérienne
Les bactéries à Gram négatif, y compris P. gingivalis, sont enveloppées d’une architecture complexe comprenant deux membranes et un espace aqueux intermédiaire. Nombre de leurs outils clés sont des lipoprotéines — des protéines ancrées aux membranes par de courtes chaînes lipidiques. Chez des espèces bien étudiées comme Escherichia coli, un système « Lol » en cinq parties transporte ces lipoprotéines de la membrane interne, à travers le périplasme, jusqu’à la membrane externe. Un composant, LolA, sert de navette dans le périplasme, tandis que LolB, situé dans la membrane externe, reçoit la cargaison et l’insère dans la couche de surface. Parce que cette voie de livraison est essentielle à la construction de la membrane externe, des éléments du système Lol sont déjà étudiés comme cibles potentielles pour de nouveaux antibiotiques.
Une pièce manquante qui n’était pas vraiment absente
Pendant des années, les chercheurs ont pensé que P. gingivalis et nombre de ses apparentés du groupe Bacteroidota étaient dépourvus de LolB. Cela posait une énigme : comment ces bactéries inséraient-elles les lipoprotéines dans leur membrane externe ? En utilisant des outils modernes de prédiction structurale (comme AlphaFold) et des expériences complémentaires, les auteurs ont identifié un candidat longtemps recherché chez P. gingivalis, une protéine codée par le gène pgn0994. Ils ont montré que cette protéine, qu’ils appellent LolB-PG, se replie presque de la même manière que les protéines LolB connues d’autres bactéries, malgré une séquence en acides aminés assez différente. Sa structure tridimensionnelle révèle une feuille incurvée formant un sillon profond, une forme adaptée pour accueillir la queue lipidique d’une lipoprotéine.
Un partenariat moléculaire sur-mesure
L’équipe a ensuite étudié comment LolB-PG interagit avec son probable partenaire, LolA, qui transporte les lipoprotéines à travers le périplasme. Des mesures biophysiques précises ont montré que LolB-PG se lie fortement et spécifiquement à la principale protéine LolA de P. gingivalis, avec une affinité similaire à celle des paires classiques LolA–LolB chez E. coli et d’autres bactéries. En revanche, LolB-PG interagit à peine avec une seconde protéine de type LolA chez P. gingivalis, nommée LolA3, ou avec LolA d’autres espèces. La modélisation structurelle suggère pourquoi : LolB-PG et la LolA principale s’arriment de façon « bouche à bouche », alignant leurs sillons de sorte que la queue lipidique puisse glisser de l’une à l’autre, tandis que LolA3 présente une surface mal adaptée. Ces résultats indiquent un appariement sélectif où chaque protéine a un rôle dédié plutôt qu’une interaction universelle.
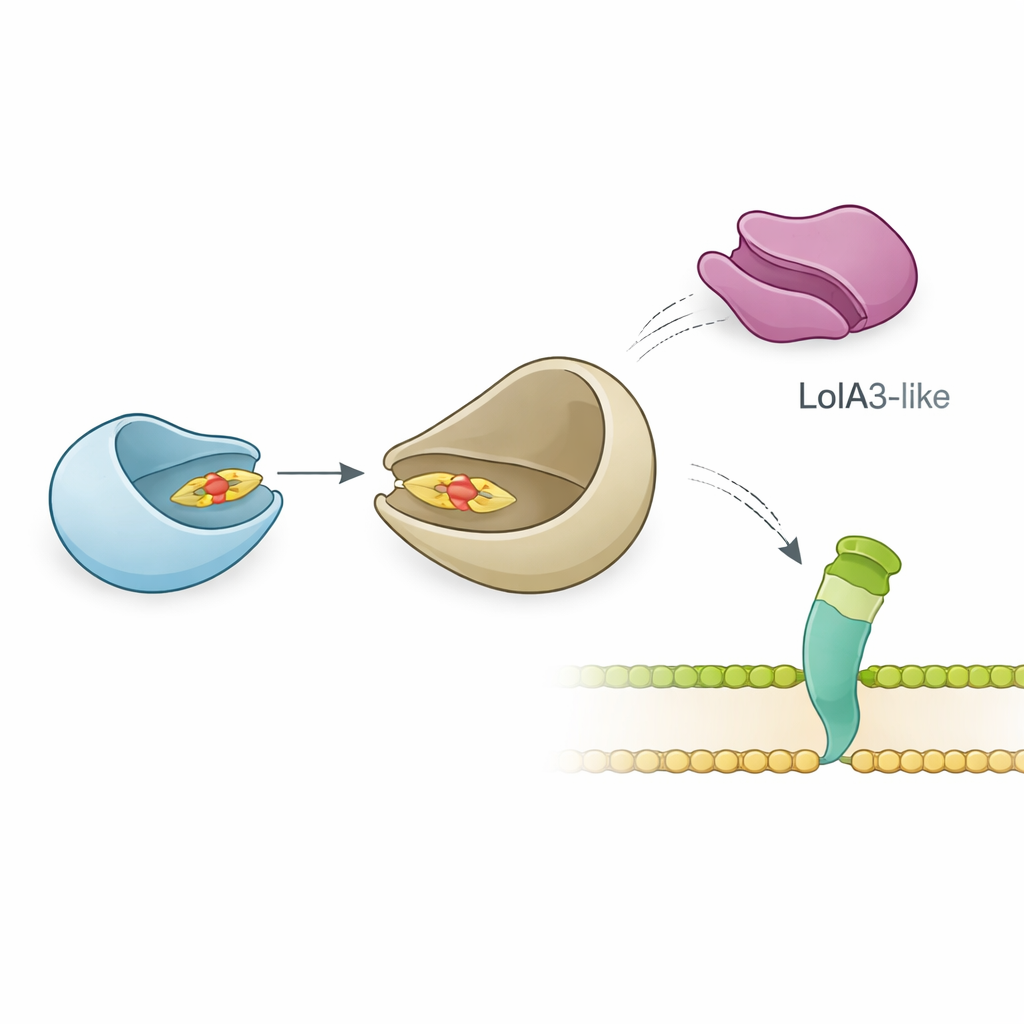
Une flexibilité surprenante dans l’assemblage de la surface
Étant donné ce partenariat évident, les chercheurs s’attendaient à ce que la suppression de LolB-PG perturbe fortement la membrane externe de la bactérie. Pour tester cela, ils ont supprimé le gène pgn0994 et examiné si la bactérie pouvait encore construire ses longues fibres de surface, appelées fimbriae, qui sont en partie composées de lipoprotéines. De manière surprenante, la souche mutante a poussé normalement et a formé des fimbriae qui ressemblaient et se comportaient beaucoup comme ceux des bactéries non modifiées. Les composants clés des fimbriae étaient toujours correctement traités, transportés vers l’enveloppe et assemblés en polymères. Cela suggère que, du moins dans les conditions de laboratoire testées, P. gingivalis peut utiliser des voies alternatives pour déplacer ces lipoprotéines, ou que d’autres systèmes interviennent pour compenser l’absence de LolB-PG.
Ce que cela signifie pour les traitements futurs
Ce travail montre que P. gingivalis possède bien une protéine de type LolB fonctionnelle qui forme un partenariat spécifique avec sa chaperonne LolA principale, préservant une étape fondamentale du transport des lipoprotéines observée chez de nombreuses bactéries. En même temps, l’élargissement du sillon de liaison de LolB-PG, son appariement sélectif et l’absence de défauts évidents après suppression de la protéine pointent tous vers un réseau de transport plus flexible et diversifié que ce que l’on pensait. Pour le grand public, la conclusion est que même des systèmes bactériens très conservés peuvent être réaménagés chez différentes espèces, ce qui peut influencer la transférabilité des stratégies antibiotiques d’un pathogène à l’autre. Cartographier ces variations en détail sera crucial pour concevoir des médicaments capables de neutraliser des bactéries nuisibles comme P. gingivalis sans nuire largement aux microbes bénéfiques sur lesquels nous comptons.
Citation: Jaiman, D., Hirohata, M., Hasegawa, Y. et al. Identification of a LolB-like protein in Porphyromonas gingivalis reveals selective LolA–LolB pairing. Sci Rep 16, 13157 (2026). https://doi.org/10.1038/s41598-026-49975-1
Mots-clés: transport des lipoprotéines, Porphyromonas gingivalis, système LolA LolB, membrane externe bactérienne, cibles antibiotiques