Clear Sky Science · zh
糖苷二烯负载纳米铁氧体(GLONF)对埃利希实体瘤诱导的肝毒性中氧化应激及P53/PCNA信号的调节
这项研究为何重要
癌症治疗常常损伤健康器官,尤其是负责代谢多种药物和肿瘤代谢产物的肝脏。本研究探讨了一种新的微小、可磁控的载体,它将一种糖基抗癌化合物直接输送至肿瘤,同时为肝脏提供保护。对读者而言,这项工作展示了纳米技术与智能化学如何在未来可能使癌症治疗更有效且毒性更低。
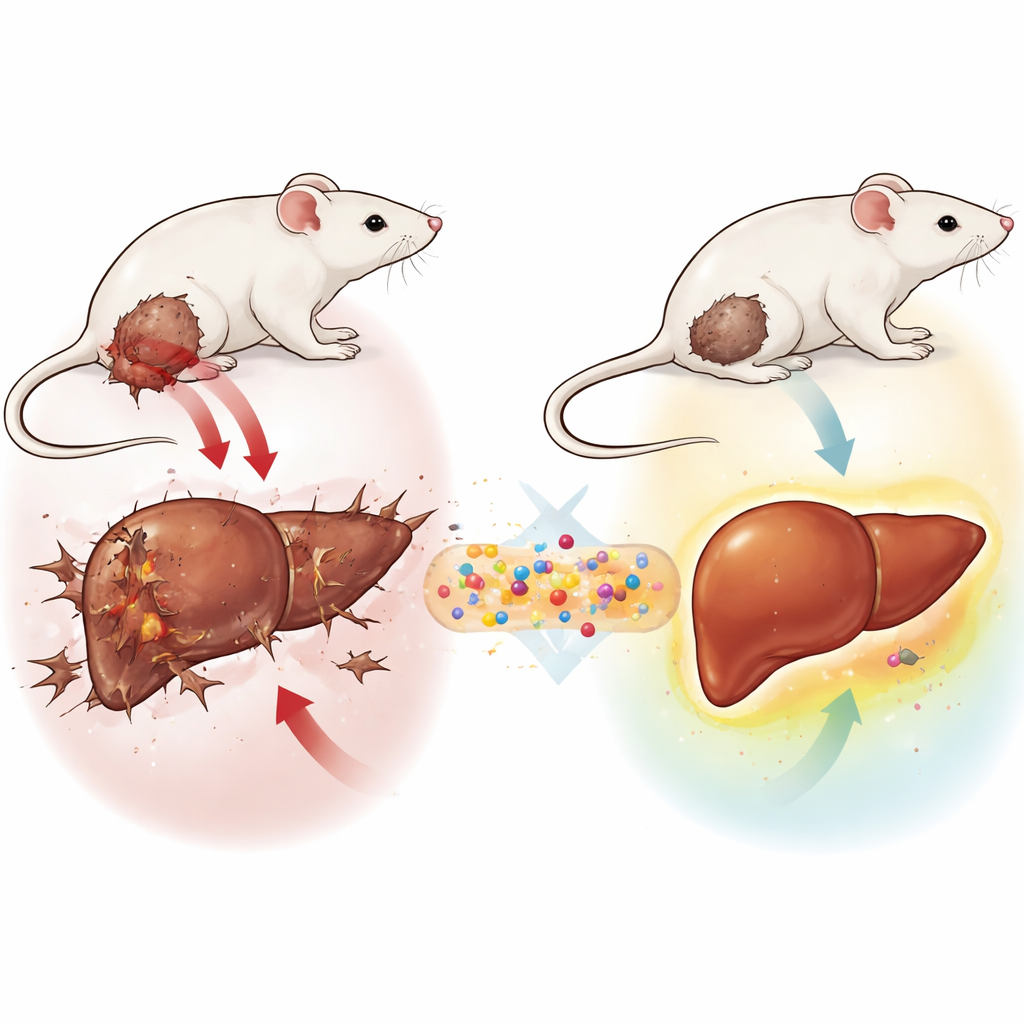
小巧的递送系统,却承担重任
研究人员构建了一种由三部分组成的纳米系统,称为GLONF。其核心是由特殊铁基材料构成的磁性矿物核。核外包裹了一层天然糖基壳层 — 壳聚糖,这种材料因其安全性和稳定性常被用于医疗材料。最后,他们连接上了一种新型糖衍生分子,称为糖苷二烯,旨在干扰癌细胞对葡萄糖的“饥饿”需求并缓和肿瘤周围的酸性微环境。组合在一起,这些成分形成了一个微小载体,理论上可用磁场引导,在体内安全迁移,并在需要处释放抗癌剂。
在类乳腺癌小鼠模型中的测试
为评估GLONF在癌症过程中能否保护肝脏,团队采用了公认的小鼠模型——埃利希实体瘤。该肿瘤来源于乳腺组织,皮下生长迅速,模拟了许多侵袭性人类癌症的特征。雌性小鼠被分为若干组:部分为健康对照,部分仅接受纳米制剂,部分植入肿瘤但不治疗,另一些在肿瘤植入同时或肿瘤形成后接受GLONF治疗。随后,研究人员测量了肿瘤体积、常规血液肝功能指标以及肝脏内一系列化学和显微学的损伤与修复标志。
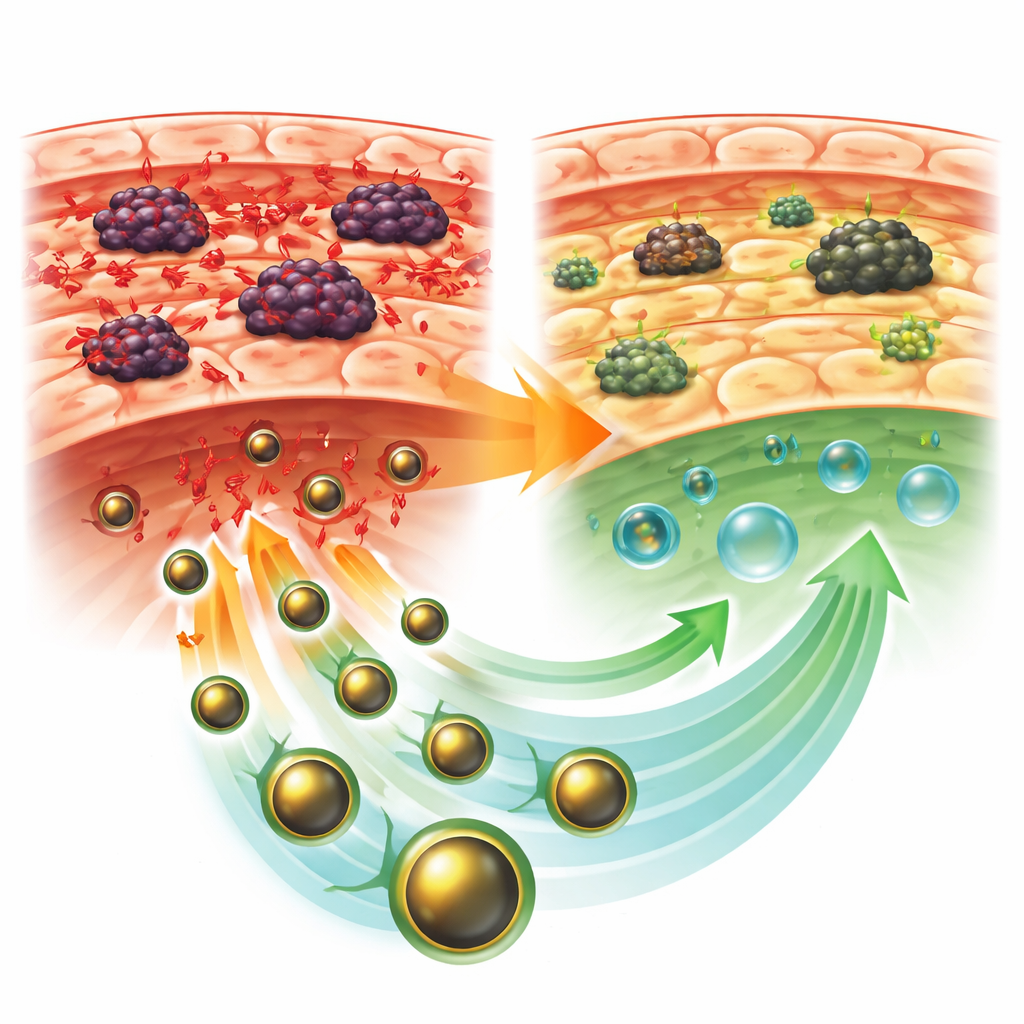
保护肝脏免受应激与损伤
未治疗的肿瘤小鼠呈现典型的肝损伤表现。受损肝细胞释放到血液中的酶明显升高,有益的血浆蛋白则下降。肝内氧化副产物增加,而保护性酶类和谷胱甘肽等天然防御物质减少。组织切片在显微镜下显示肝脏结构紊乱,细胞肿胀坏死、类瘢痕改变及大量炎性细胞浸润。相比之下,接受GLONF处理的小鼠肿瘤体积较小且肝脏明显更健康。其血液指标向正常值恢复,氧化损伤降低,抗氧化防御体系回升,尤其是在允许肿瘤形成后再给予GLONF的情况下更为显著。
平抑失控的细胞信号
研究团队还检测了肝细胞内两种关键蛋白。其一PCNA与细胞增殖相关;另一种P53对DNA损伤作出反应并可诱导细胞凋亡。在未治疗的肿瘤小鼠中,这两种标志物都显著升高,表明强烈的应激和失控的修复尝试。GLONF处理显著降低了肝组织中这些标志物的丰度,提示该纳米系统减少了应急修复的需求并有助于稳定细胞环境。这与生化和组织学发现一致,表明氧化应激和损伤得到了协同缓解。
对未来癌症护理的可能意义
总之,这项工作表明GLONF——一种可磁控的糖基纳米载体——在小鼠中既能缩小肿瘤,又能保护肝脏免受严重损害。通过将靶向递送与抗氧化和代谢干预结合,该系统提供了一种可能性,能使癌症治疗对重要器官更温和。尽管这些结果仍来自动物研究,距离常规临床应用尚远,但它们展示了通过精细设计的纳米结构,未来治疗可能在攻击肿瘤的同时保护身体的天然“过滤器”。
引用: Tousson, E., Atrash, A.E., Abdelrasol, M.Y. et al. Modulation of oxidative stress and P53/PCNA signaling by glucosodiene-loaded nanoferrites (GLONF) in ehrlich solid tumor–induced hepatotoxicity. Sci Rep 16, 12351 (2026). https://doi.org/10.1038/s41598-026-45548-4
关键词: 纳米医学, 肝脏保护, 乳腺癌模型, 氧化应激, 药物递送