Clear Sky Science · ru
Модуляция окислительного стресса и сигнального пути P53/PCNA глюкозодиен-загруженными наноферритами (GLONF) при вызванной опухолью Эрлиха гепатотоксичности
Почему это исследование важно
Лечение рака часто повреждает здоровые органы, особенно печень, которой приходится расщеплять многие лекарства и продукты распада опухолей. В этом исследовании изучается новый крошечный магнитно управляемый носитель, доставляющий сахаросодержащее противораковое соединение непосредственно к опухолям и одновременно защищающий печень от вреда. Для читателей это даёт представление о том, как нанотехнологии и рациональная химия могут в будущем сделать лечение рака более эффективным и менее токсичным.
Крошечная система доставки с большой задачей
Исследователи создали трёхкомпонентную наноразмерную систему под названием GLONF. В её центре — магнитное минеральное ядро из специального железосодержащего материала. Вокруг ядра они поместили природную сахарную оболочку хитозан, часто используемую в медицинских материалах за её безопасность и стабильность. Наконец, к системе присоединили новое сахаропроизводное соединение — глюкозодиен, разработанное для вмешательства в потребление глюкозы раковыми клетками и смягчения жесткой кислой среды вокруг опухолей. В совокупности эти компоненты создают миниатюрный транспорт, который в принципе может управляться магнитами, безопасно перемещаться в организме и высвобождать противораковое средство там, где оно наиболее нужно.
Испытания на мышиной модели, похожей на рак молочной железы
Чтобы выяснить, может ли GLONF защищать печень во время рака, команда использовала хорошо изученную мышиную модель — твердую опухоль Эрлиха. Эта опухоль, изначально полученная из ткани молочной железы, быстро растёт под кожей и имитирует многие черты агрессивных человеческих опухолей. Самок мышей разделили на группы: одни оставались здоровыми, другим вводили только наноформуляцию, некоторые развивали опухоль без лечения, а другие получали GLONF либо одновременно с имплантацией опухоли, либо после формирования опухоли. Учёные затем измеряли размер опухоли, стандартные показатели здоровья печени в крови и набор химических и микроскопических признаков повреждения и восстановления в самой печени.
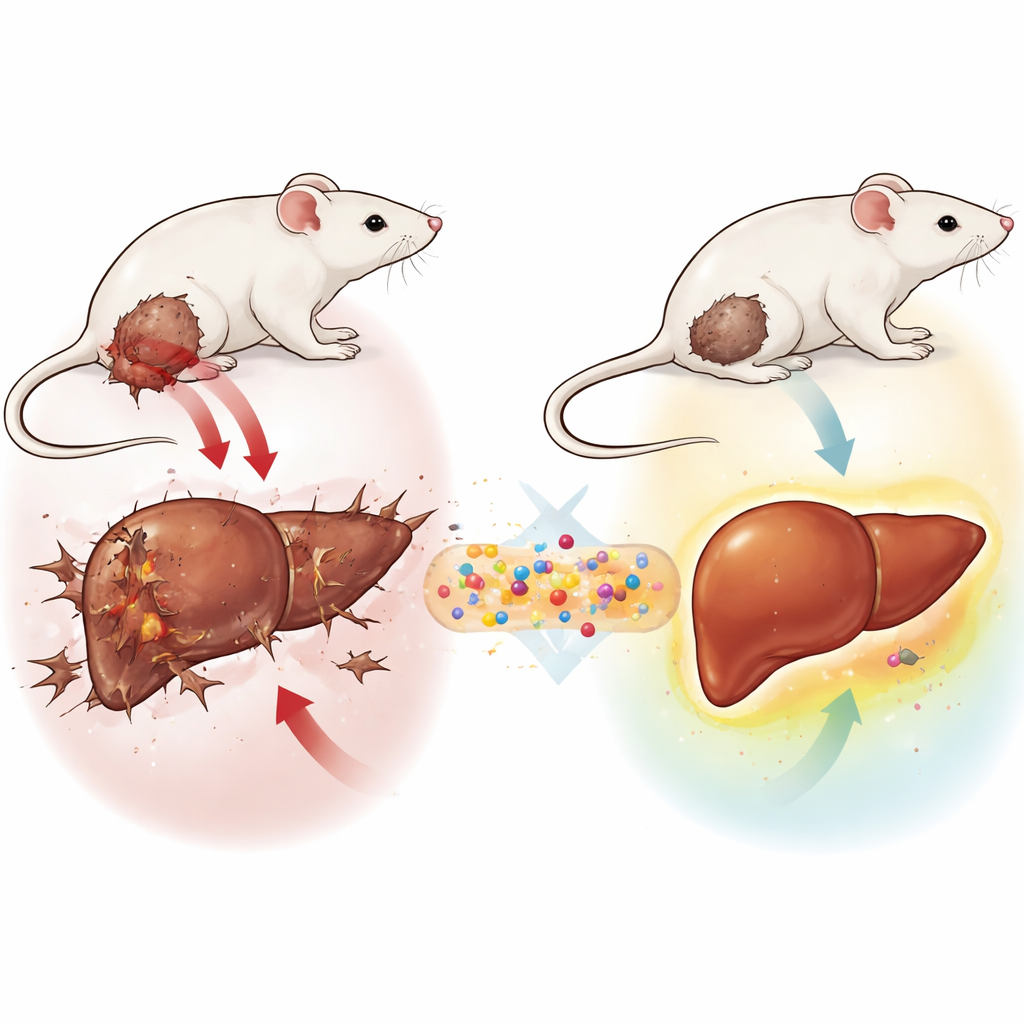
Защита печени от стресса и повреждений
У мышей с опухолями без лечения наблюдалась типичная картина повреждения печени. Ферменты, которые попадают в кровь при повреждении печёночных клеток, резко повышались, тогда как полезные белки крови снижались. Внутри печени увеличивался уровень вредных продуктов окисления, а природные защитные механизмы, такие как защитные ферменты и глутатион, уменьшались. Ткани под микроскопом показывали нарушенную архитектуру печени с отёчными и умирающими клетками, рубцевыми изменениями и интенсивной инвазией воспалительных клеток. Напротив, у животных, получавших GLONF, опухоли были меньше, а печень заметно здоровее. Их анализы крови приближались к норме, окислительное повреждение снижалось, а антиоксидантная защита восстанавливалась, особенно когда GLONF вводили после формирования опухоли.
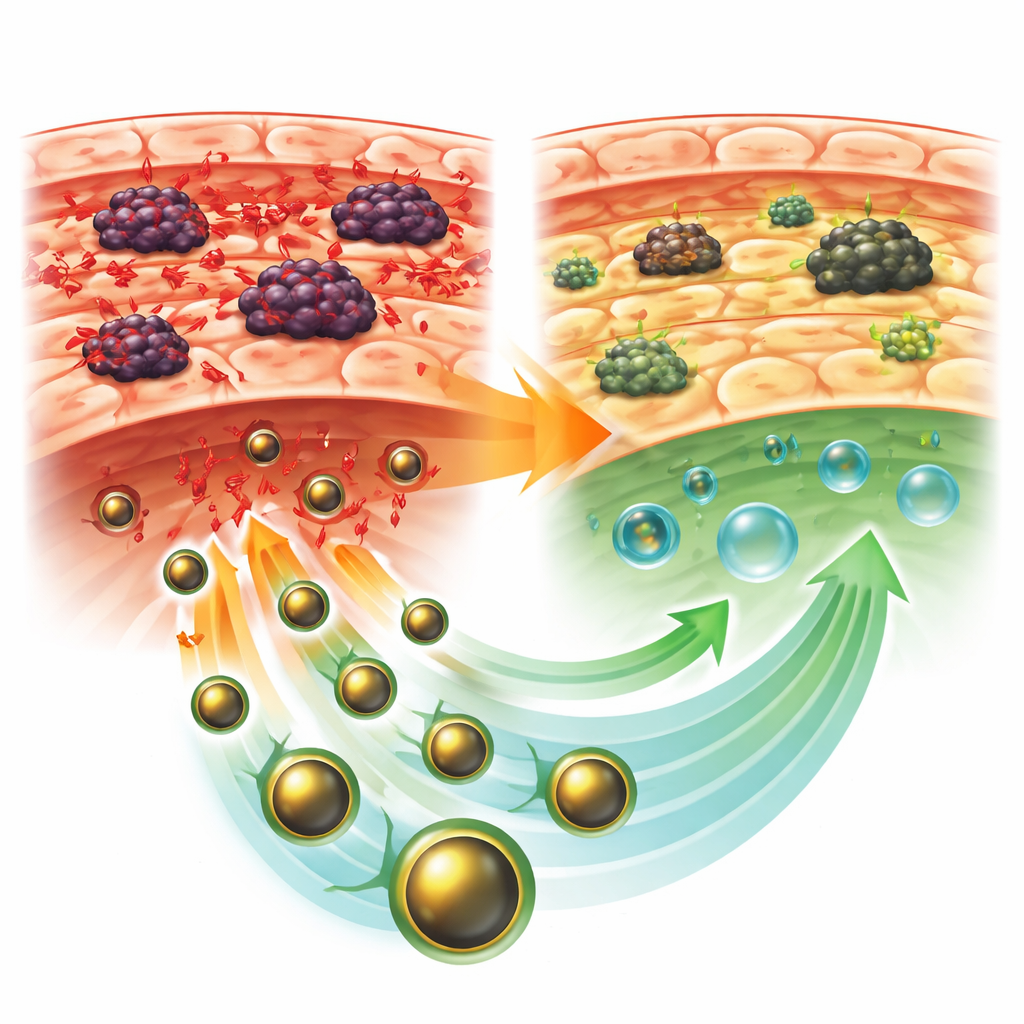
Усмирение неконтролируемых клеточных сигналов
Команда также изучала два ключевых белка внутри печёночных клеток. Один, PCNA, связан с пролиферацией клеток, другой, P53, реагирует на повреждение ДНК и может запускать гибель клеток. У животных с опухолями без лечения оба маркера были сильно повышены, что указывало на интенсивный стресс и неконтролируемые попытки восстановления. Лечение GLONF заметно снижало уровень этих маркеров в тканях печени, что говорит о том, что нано-система уменьшала потребность в экстренном восстановлении и помогала стабилизировать клеточную среду. Это согласуется с биохимическими и структурными данными, указывая на согласованное ослабление окислительного стресса и повреждений.
Что это может значить для будущей терапии рака
В заключение, работа показывает, что GLONF — магниточувствительный, сахаросодержащий нанокарриер — может уменьшать опухоли у мышей и одновременно защищать печень от серьёзного вреда. Комбинируя таргетированную доставку с антиоксидантными и метаболическими эффектами, система предлагает потенциальный путь сделать лечение рака более щадящим для жизненно важных органов. Хотя эти результаты получены на животных и далеко от рутинного клинического применения, они демонстрируют, как тщательно спроектированные наноструктуры могут в будущем помочь терапиям атаковать опухоли, щадя природные «фильтры» организма.
Цитирование: Tousson, E., Atrash, A.E., Abdelrasol, M.Y. et al. Modulation of oxidative stress and P53/PCNA signaling by glucosodiene-loaded nanoferrites (GLONF) in ehrlich solid tumor–induced hepatotoxicity. Sci Rep 16, 12351 (2026). https://doi.org/10.1038/s41598-026-45548-4
Ключевые слова: наномедицина, защита печени, модель рака молочной железы, окислительный стресс, доставка лекарств