Clear Sky Science · sv
Modulation of oxidative stress and P53/PCNA signaling by glucosodiene-loaded nanoferrites (GLONF) in ehrlich solid tumor–induced hepatotoxicity
Varför denna forskning är viktig
Cancerbehandlingar skadar ofta friska organ, särskilt levern, som måste bryta ner många läkemedel och avfallsprodukter från tumörer. Denna studie undersöker en ny, mycket liten magnetiskt styrd bärare som levererar en sockerbaserad anticancerförening direkt mot tumörer samtidigt som levern skyddas från skada. För läsaren ger den en inblick i hur nanoteknik och smart kemi en dag kan göra cancerbehandling mer effektiv och mindre giftig.
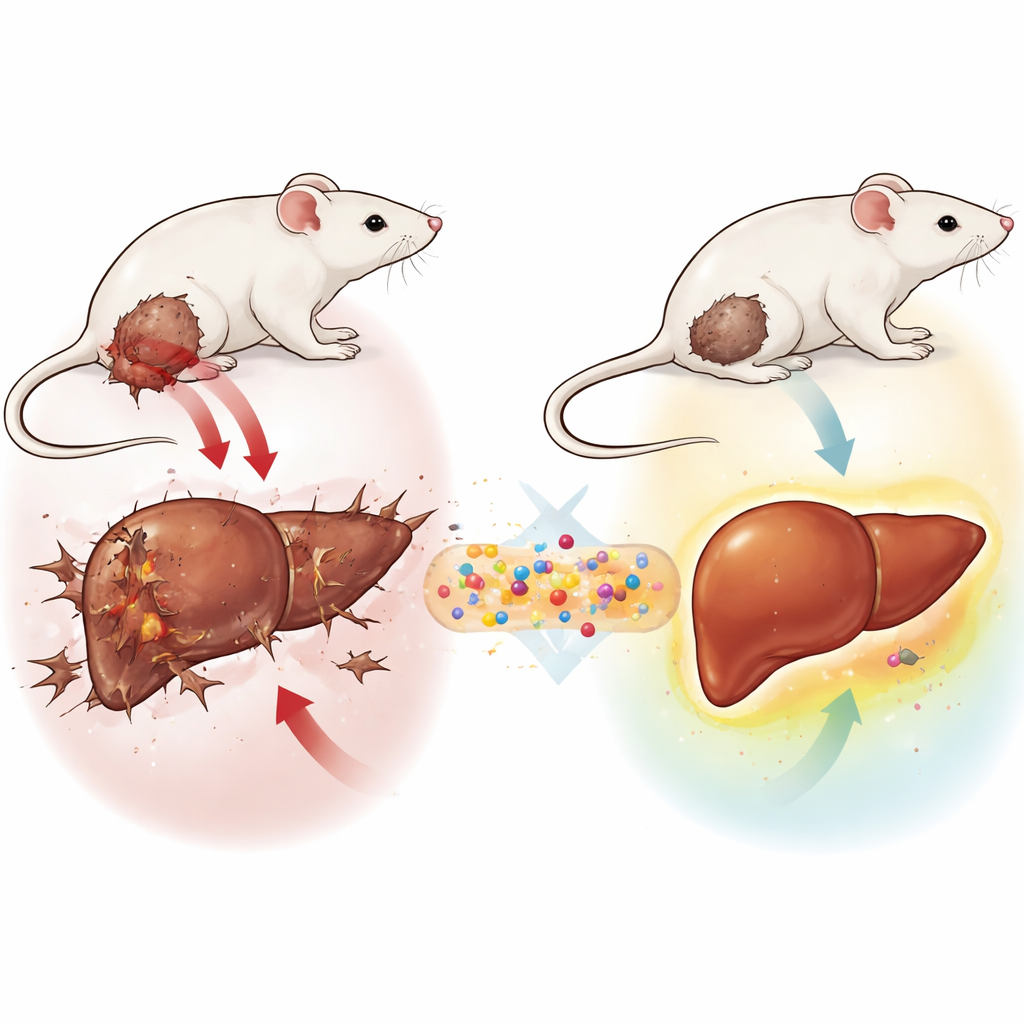
Systemet är litet men har ett stort uppdrag
Forskarna byggde ett tredelat nanosystem kallat GLONF. I dess centrum finns en magnetisk mineralisk kärna gjord av ett särskilt järnbaserat material. Runt kärnan lade de ett naturligt sockerbaserat hölje kallat kitin (chitosan), ofta använt i medicinska material för dess säkerhet och stabilitet. Slutligen kopplade de på en ny sockeravledd molekyl kallad glucosodiene, utformad för att störa cancercellers glukosbehov och mildra den hårda, sura miljön runt tumörer. Tillsammans skapar dessa komponenter ett miniatyrfordon som i princip kan styras med magneter, färdas säkert i kroppen och frigöra ett anticancerämne där det behövs mest.
Testning i en musmodell av bröstliknande cancer
För att se om GLONF kunde skydda levern under cancer använde teamet en väletablerad musmodell kallad Ehrlich solid tumor. Denna tumör, ursprungligen härledd från bröstvävnad, växer snabbt under huden och efterliknar många egenskaper hos aggressiva mänskliga cancerformer. Honmöss delades in i grupper: några förblev friska, några fick endast nanoformuleringen, några utvecklade tumörer utan behandling, och andra fick GLONF antingen samtidigt som tumörimplantationen eller efter att tumören hade bildats. Forskarna mätte sedan tumörstorlek, vanliga blodmarkörer för leverhälsa samt en rad kemiska och mikroskopiska tecken på skada och återhämtning i levern.
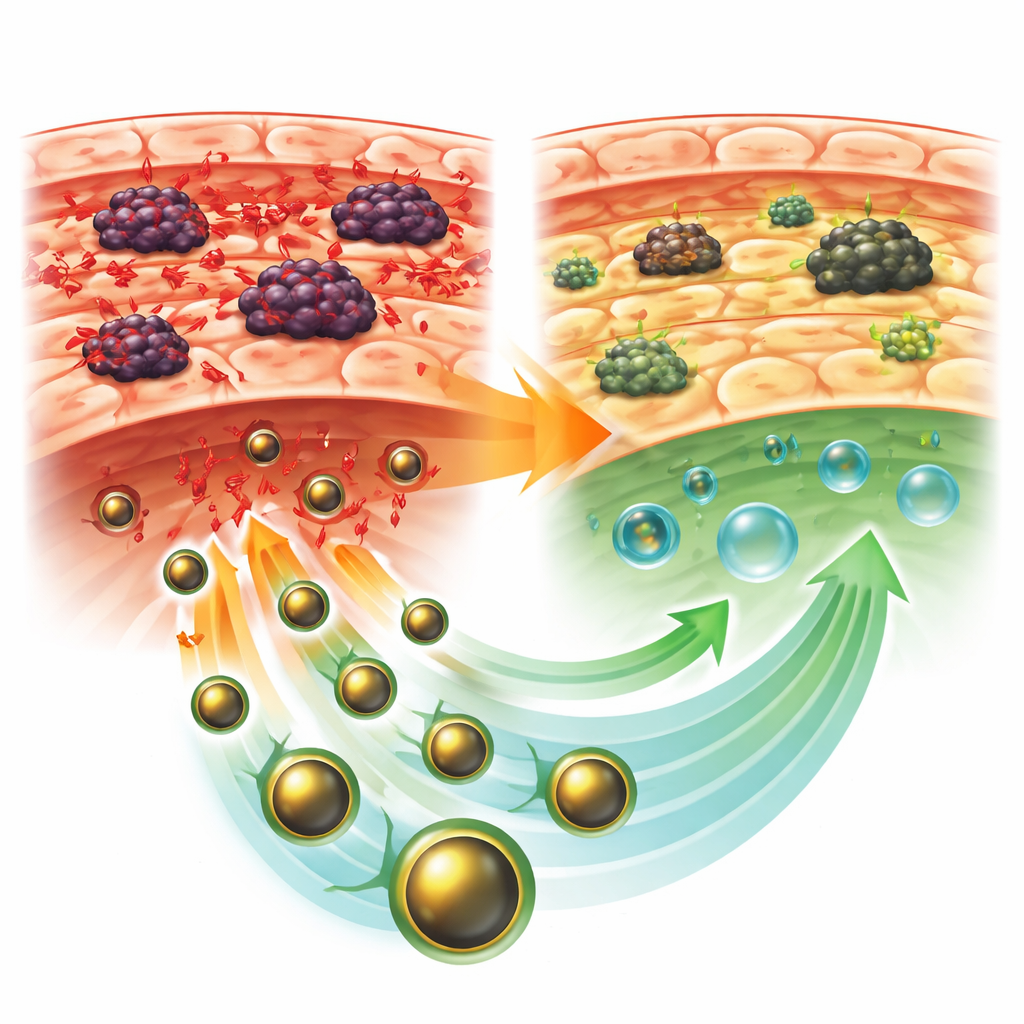
Skydd för levern mot stress och skada
Möss med obehandlade tumörer visade en klassisk bild av leverskada. Enzymer som läcker ut i blodet när leverceller skadas ökade kraftigt, medan nyttiga blodproteiner sjönk. Inuti levern ökade nivåerna av skadliga oxidationsprodukter och de naturliga försvaren, såsom skyddande enzymer och glutation, föll. Vävnadssektioner under mikroskopet visade förvrängd leverarkitektur med svullna och döende celler, ärrliknande förändringar och kraftig invasion av inflammatoriska celler. I kontrast hade möss som behandlats med GLONF mindre tumörer och betydligt friskare levervärden. Deras blodprov rörde sig mot det normala, oxidativ skada minskade och antioxidanternas försvar återhämtade sig, särskilt när GLONF gavs efter att tumören fått bildas.
Lugna överaktiva cellsignaler
Teamet undersökte också två nyckelproteiner inne i levercellerna. Det ena, PCNA, är associerat med cellproliferation, och det andra, P53, svarar på DNA-skador och kan utlösa celldöd. Hos tumörbärande möss utan behandling var båda markörerna starkt förhöjda, vilket signalerade intensiv stress och okontrollerade reparationsförsök. GLONF-behandling minskade märkbart förekomsten av dessa markörer i levervävnaden, vilket tyder på att nanosystemet minskade behovet av akut reparation och hjälpte till att stabilisera den cellulära miljön. Detta stämmer överens med de biokemiska och strukturella fynden och pekar på en samordnad lättnad av oxidativ stress och skada.
Vad detta kan innebära för framtida cancerbehandling
Sammanfattningsvis visar detta arbete att GLONF, en magnetiskt responsiv, sockerbaserad nanobärare, kan krympa tumörer hos möss samtidigt som den skyddar levern från allvarlig skada. Genom att kombinera riktad leverans med antioxidant- och metabola effekter erbjuder systemet ett potentiellt sätt att göra cancerbehandling snällare mot livsviktiga organ. Även om dessa resultat ännu är begränsade till djurstudier och långt från rutinmässig klinisk användning, visar de hur noggrant konstruerade nanostrukturer kan hjälpa framtida terapier att angripa tumörer samtidigt som kroppens naturliga filter skonas.
Citering: Tousson, E., Atrash, A.E., Abdelrasol, M.Y. et al. Modulation of oxidative stress and P53/PCNA signaling by glucosodiene-loaded nanoferrites (GLONF) in ehrlich solid tumor–induced hepatotoxicity. Sci Rep 16, 12351 (2026). https://doi.org/10.1038/s41598-026-45548-4
Nyckelord: nanomedicine, liver protection, breast cancer model, oxidative stress, drug delivery