Clear Sky Science · it
Modulazione dello stress ossidativo e del segnalamento P53/PCNA da parte di nanoferriti caricate con glucosodiene (GLONF) nella epatotossicità indotta da tumore solido di Ehrlich
Perché questa ricerca è importante
I trattamenti contro il cancro spesso danneggiano organi sani, in particolare il fegato, che deve smaltire molti farmaci e prodotti di scarto derivati dai tumori. Questo studio esplora un nuovo vettore minuscolo, guidabile magneticamente, che consegna un composto anticancro a base di zucchero direttamente ai tumori, proteggendo al contempo il fegato dai danni. Per i lettori offre uno sguardo su come la nanotecnologia e la chimica intelligente potrebbero un giorno rendere le terapie contro il cancro più efficaci e meno tossiche.
Un minuscolo sistema di rilascio con un grande compito
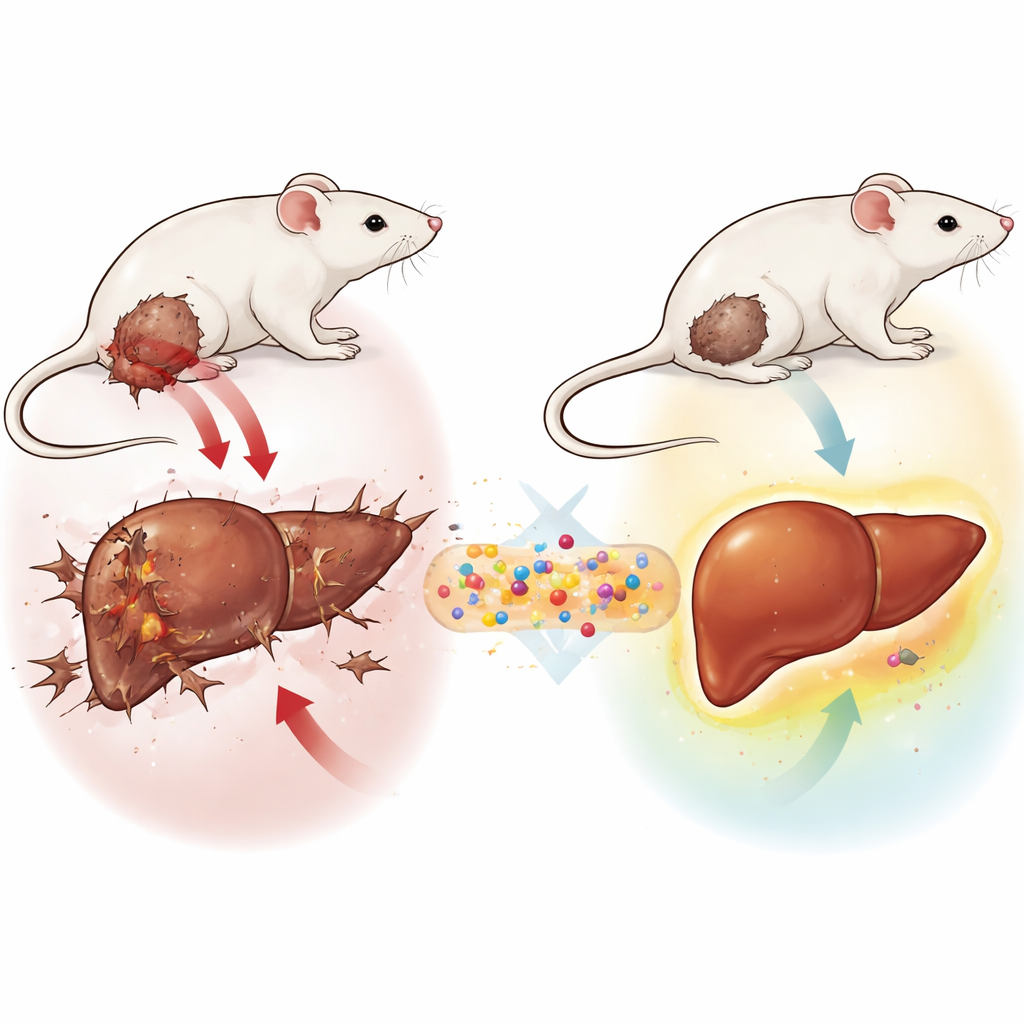
I ricercatori hanno realizzato un sistema a tre componenti di dimensioni nanometriche chiamato GLONF. Al suo centro c’è un nucleo minerale magnetico composto da un materiale a base di ferro. Attorno a quel nucleo hanno aggiunto un involucro naturale a base di zucchero chiamato chitosano, spesso impiegato nei materiali medici per la sua sicurezza e stabilità. Infine hanno legato una nuova molecola derivata dagli zuccheri chiamata glucosodiene, progettata per interferire con la fame di glucosio delle cellule tumorali e per attenuare l’ambiente acido e ostile che circonda i tumori. Insieme, questi componenti creano un veicolo in miniatura che, in linea di principio, può essere guidato da magneti, viaggiare in modo sicuro nell’organismo e rilasciare un agente anticancro dove è più necessario.
Test in un modello murino di cancro simile al seno
Per verificare se GLONF potesse proteggere il fegato durante il cancro, il team ha utilizzato un modello murino ben consolidato chiamato tumore solido di Ehrlich. Questo tumore, originariamente derivato dal tessuto mammario, cresce rapidamente sotto la pelle e riproduce molte caratteristiche dei tumori umani aggressivi. Topi femmina sono stati suddivisi in gruppi: alcuni rimasero sani, alcuni ricevettero solo la nanoformulazione, alcuni svilupparono tumori senza trattamento e altri ricevettero GLONF sia contemporaneamente all’impianto del tumore sia dopo la formazione del tumore. Gli scienziati hanno quindi misurato le dimensioni del tumore, i marcatori ematici standard della salute epatica e una serie di segni chimici e microscopici di danno e riparazione all’interno del fegato.
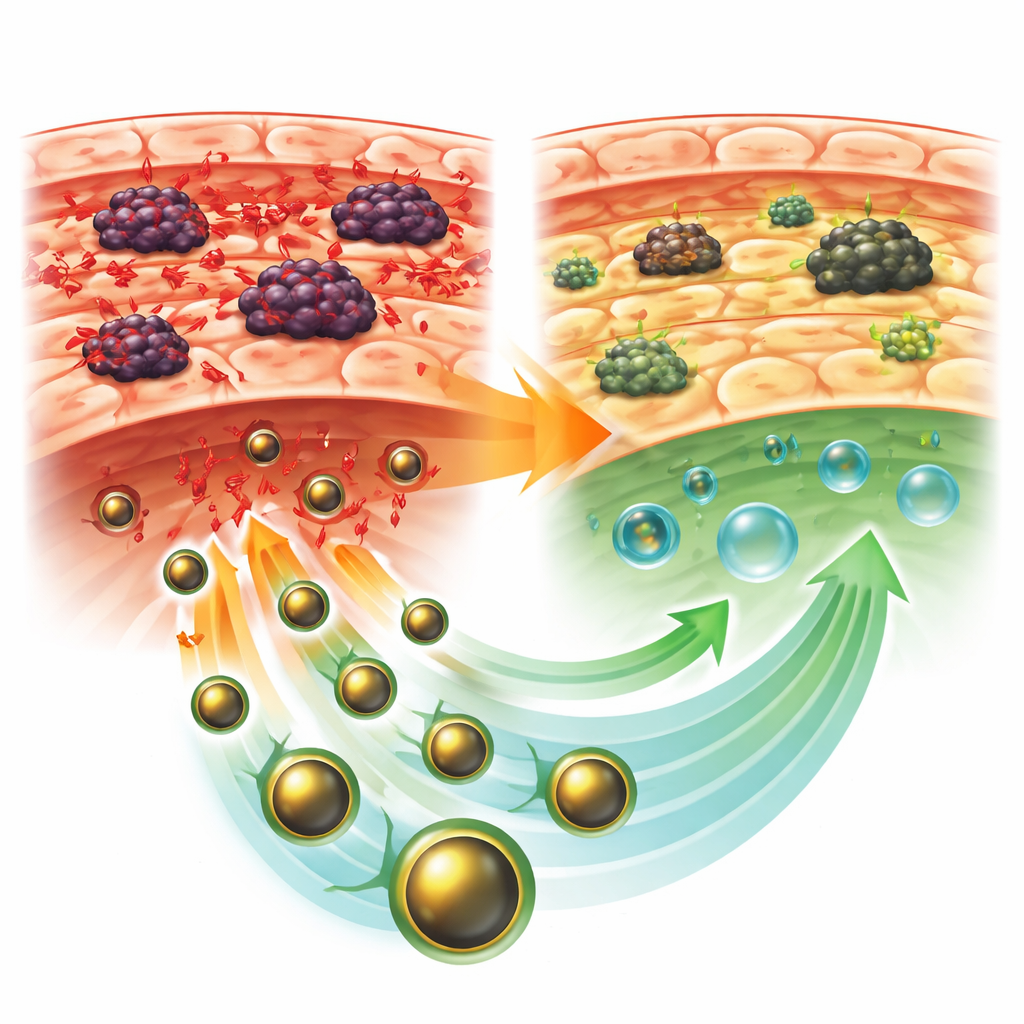
Proteggere il fegato dallo stress e dal danno
I topi portatori di tumore non trattati mostrarono il quadro classico di lesione epatica. Gli enzimi che fuoriescono nel sangue quando le cellule del fegato sono danneggiate aumentarono vistosamente, mentre le proteine ematiche benefiche diminuirono. All’interno del fegato, i livelli di prodotti dannosi derivati dall’ossidazione aumentarono e le difese naturali come gli enzimi protettivi e il glutatione calarono. Le sezioni tissutali al microscopio rivelarono un’architettura epatica distorta, con cellule gonfie e necrotiche, alterazioni simili a cicatrici e una massiccia invasione di cellule infiammatorie. Al contrario, i topi trattati con GLONF presentarono tumori più piccoli e fegati sostanzialmente più sani. Gli esami del sangue tornarono verso valori normali, il danno ossidativo si ridusse e le difese antiossidanti si ripresero, soprattutto quando GLONF fu somministrato dopo la formazione del tumore.
Calmare segnali cellulari fuori controllo
Il team ha anche esaminato due proteine chiave all’interno delle cellule epatiche. Una, PCNA, è associata alla proliferazione cellulare, e l’altra, P53, risponde al danno al DNA e può innescare la morte cellulare. Nei topi portatori di tumore non trattati entrambi i marcatori risultarono fortemente elevati, segnalando intenso stress e tentativi di riparazione incontrollati. Il trattamento con GLONF ridusse in modo evidente l’abbondanza di questi marcatori nel tessuto epatico, suggerendo che il nano-sistema ridusse la necessità di riparazioni d’emergenza e contribuì a stabilizzare l’ambiente cellulare. Ciò è coerente con i riscontri biochimici e strutturali, indicando un alleggerimento coordinato dello stress ossidativo e del danno.
Che cosa potrebbe significare per la cura del cancro in futuro
In sintesi, questo lavoro dimostra che GLONF, un nano-vettore zuccherino reattivo a campi magnetici, può ridurre le dimensioni dei tumori nei topi proteggendo al contempo il fegato da danni seri. Combinando la consegna mirata con effetti antiossidanti e metabolici, il sistema offre una potenziale via per rendere le terapie oncologiche meno dannose per gli organi vitali. Sebbene questi risultati siano ancora limitati ad animali e lontani dall’uso clinico di routine, mostrano come nanostrutture attentamente progettate potrebbero aiutare terapie future ad attaccare i tumori risparmiando i filtri naturali del corpo.
Citazione: Tousson, E., Atrash, A.E., Abdelrasol, M.Y. et al. Modulation of oxidative stress and P53/PCNA signaling by glucosodiene-loaded nanoferrites (GLONF) in ehrlich solid tumor–induced hepatotoxicity. Sci Rep 16, 12351 (2026). https://doi.org/10.1038/s41598-026-45548-4
Parole chiave: nanomedicina, protezione del fegato, modello di cancro al seno, stress ossidativo, veicolazione del farmaco