Clear Sky Science · nl
Modulatie van oxidatieve stress en P53/PCNA-signalerng door glucosodien-beladen nanoferrieten (GLONF) bij Ehrlich-solidetumor-geïnduceerde hepatotoxiciteit
Waarom dit onderzoek ertoe doet
Cancercures beschadigen vaak ook gezonde organen, met name de lever die veel geneesmiddelen en afvalproducten uit tumoren moet afbreken. Deze studie onderzoekt een nieuwe, zeer kleine magnetisch geleide drager die een suikergemedieerde antikankerverbinding rechtstreeks naar tumoren brengt en tegelijkertijd de lever beschermt. Voor lezers biedt het een blik op hoe nanotechnologie en slimme chemie mogelijk de behandeling van kanker effectiever en minder toxisch kunnen maken.
Een klein bezorgsysteem met een grote taak
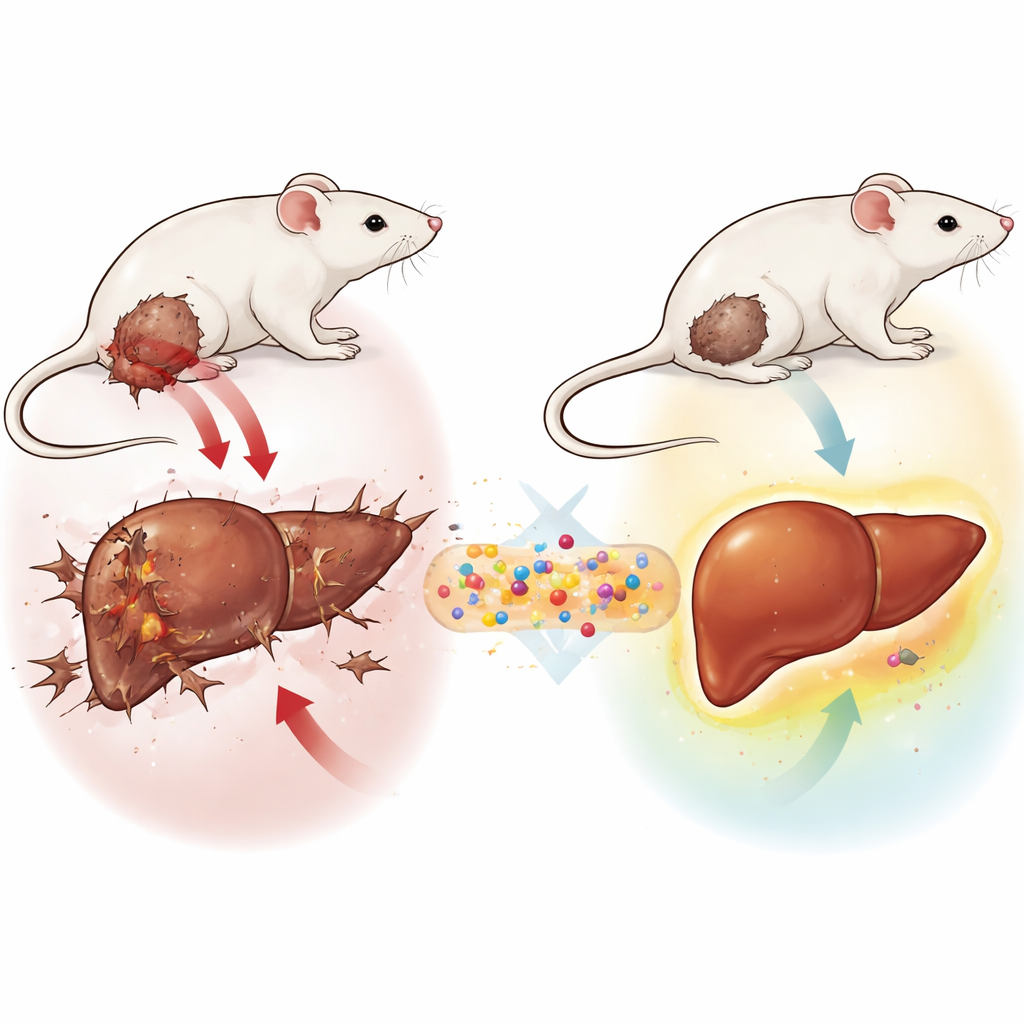
De onderzoekers bouwden een driedelig nanosysteem genaamd GLONF. In het centrum bevindt zich een magnetische mineraalkern van een speciaal ijzerhoudend materiaal. Rond die kern voegden ze een natuurlijke, suikerhoudende schaal toe, chitosan, vaak gebruikt in medische materialen vanwege de veiligheid en stabiliteit. Ten slotte hechtten ze een nieuw suikerafgeleid molecuul, glucosodien, dat is ontworpen om de honger van kankercellen naar glucose te verstoren en het zure, vijandige milieu rond tumoren te verzachten. Samen vormen deze componenten een miniatuurvoertuig dat, in principe, door magneten geleid kan worden, veilig door het lichaam kan reizen en een antikankermiddel vrijgeeft waar het het meest nodig is.
Testen in een muismodel van borstvocht-achtige kanker
Om te onderzoeken of GLONF de lever tijdens kanker kon beschermen, gebruikte het team een goed vastgesteld muismodel dat bekend staat als de Ehrlich solid tumor. Deze tumor, oorspronkelijk afkomstig van borstweefsel, groeit snel onder de huid en bootst veel kenmerken van agressieve menselijke kankers na. Vrouwelijke muizen werden in groepen verdeeld: sommige bleven gezond, sommige kregen alleen de nanoformulering, sommige ontwikkelden tumoren zonder behandeling en anderen kregen GLONF ofwel gelijktijdig met de tumoringang of nadat de tumor gevormd was. De wetenschappers maten vervolgens tumorgrootte, standaard bloedmarkers voor levergezondheid en een reeks chemische en microscopische aanwijzingen voor schade en herstel in de lever.
De lever beschermen tegen stress en schade
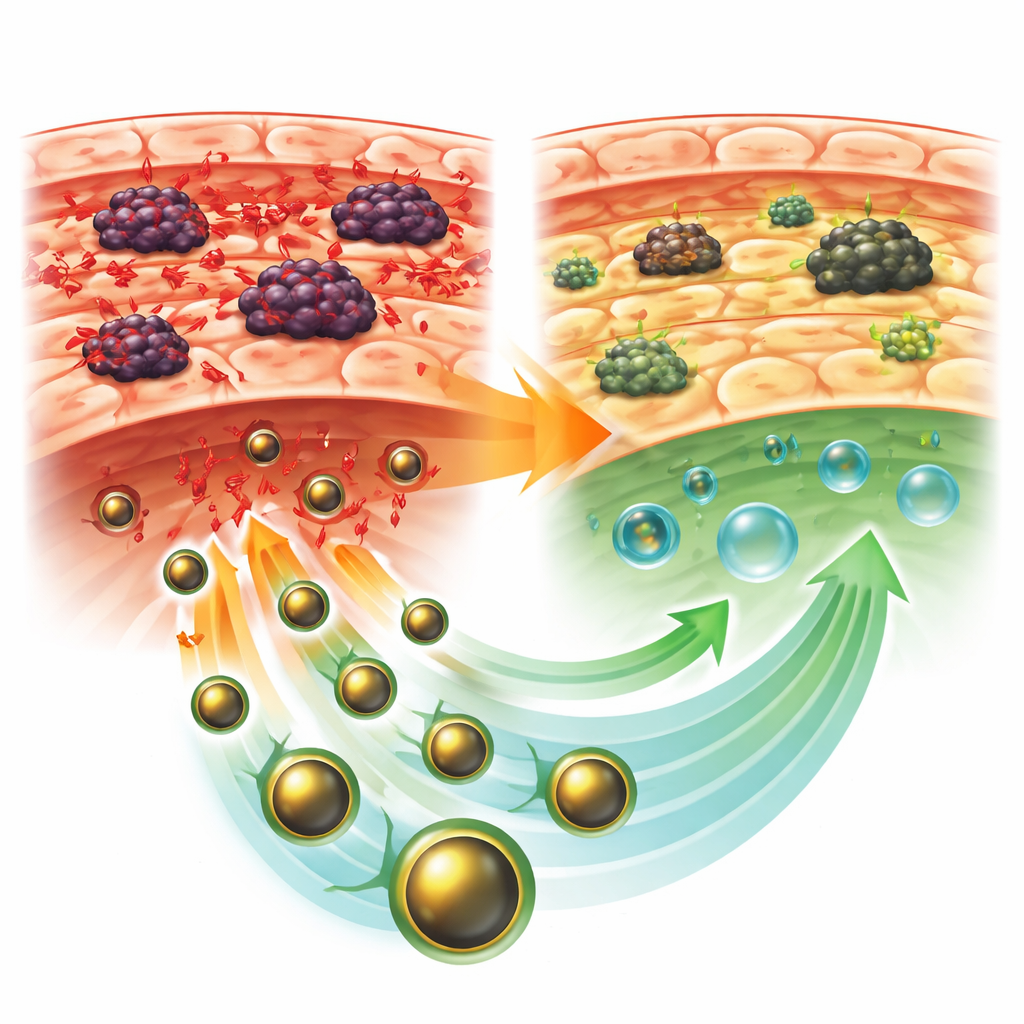
Muizen met onbehandelde tumoren toonden het klassieke beeld van leverbeschadiging. Enzymen die in het bloed lekken wanneer levercellen beschadigd zijn, stegen sterk, terwijl nuttige bloedproteïnen daalden. In de lever namen de niveaus van schadelijke oxidatiebijproducten toe en daalden natuurlijke verdedigingsmechanismen zoals beschermende enzymen en glutathion. Weefseldoorsneden onder de microscoop onthulden een verstoorde leverarchitectuur, met gezwollen en stervende cellen, littekenachtige veranderingen en sterke invasie van ontstekingscellen. Ter vergelijking hadden muizen die met GLONF werden behandeld kleinere tumoren en beduidend gezondere leverwaarden. Hun bloedtesten keerden richting normaal, oxidatieve schade nam af en de antioxidatieve verdediging herstelde zich, vooral wanneer GLONF werd toegediend nadat de tumor zich had gevormd.
Het kalmeren van ontspoorde celsignalen
Het team onderzocht ook twee sleutelproteïnen in levercellen. PCNA hangt samen met celproliferatie en P53 reageert op DNA-schade en kan celdood induceren. Bij muizen met tumoren zonder behandeling waren beide markers sterk verhoogd, wat wijst op intense stress en ongecontroleerde reparatiepogingen. GLONF-behandeling verlaagde merkbaar de aanwezigheid van deze markers in leverweefsel, wat suggereert dat het nanosysteem de noodzaak voor noodreparatie verminderde en het cellulaire milieu stabiliseerde. Dit sluit aan bij de biochemische en structurele bevindingen en duidt op een gecoördineerde vermindering van oxidatieve stress en letsel.
Wat dit kan betekenen voor toekomstige kankerzorg
Samengevat laat dit werk zien dat GLONF, een magnetisch reagerende, suikergebaseerde nanodrager, tumoren bij muizen kan verkleinen terwijl het de lever tegen ernstige schade beschermt. Door gerichte afgifte te combineren met antioxidatieve en metabole effecten, biedt het systeem een mogelijke manier om kankerbehandeling vriendelijker te maken voor vitale organen. Hoewel deze resultaten nog in diermodellen zijn en ver verwijderd van routinematig klinisch gebruik, demonstreren ze hoe zorgvuldig ontworpen nanostructuren toekomstige therapieën kunnen helpen tumoren aan te vallen en tegelijk de natuurlijke filters van het lichaam te sparen.
Bronvermelding: Tousson, E., Atrash, A.E., Abdelrasol, M.Y. et al. Modulation of oxidative stress and P53/PCNA signaling by glucosodiene-loaded nanoferrites (GLONF) in ehrlich solid tumor–induced hepatotoxicity. Sci Rep 16, 12351 (2026). https://doi.org/10.1038/s41598-026-45548-4
Trefwoorden: nanogeneeskunde, leverbescherming, borstkankermodel, oxidatieve stress, drugdelivery