Clear Sky Science · es
Modulación del estrés oxidativo y de la señalización P53/PCNA por nanoferritas cargadas con glucosodieno (GLONF) en la hepatotoxicidad inducida por tumor sólido de Ehrlich
Por qué importa esta investigación
Los tratamientos contra el cáncer frecuentemente dañan órganos sanos, en especial el hígado, que debe metabolizar muchos fármacos y los productos de desecho procedentes de los tumores. Este estudio explora un nuevo transportador diminuto, guiable por imanes, que entrega un compuesto anticancerígeno derivado de un azúcar directamente hacia los tumores, al tiempo que protege al hígado del daño. Para los lectores, ofrece una visión de cómo la nanotecnología y la química inteligente podrían algún día hacer los tratamientos contra el cáncer más efectivos y menos tóxicos.
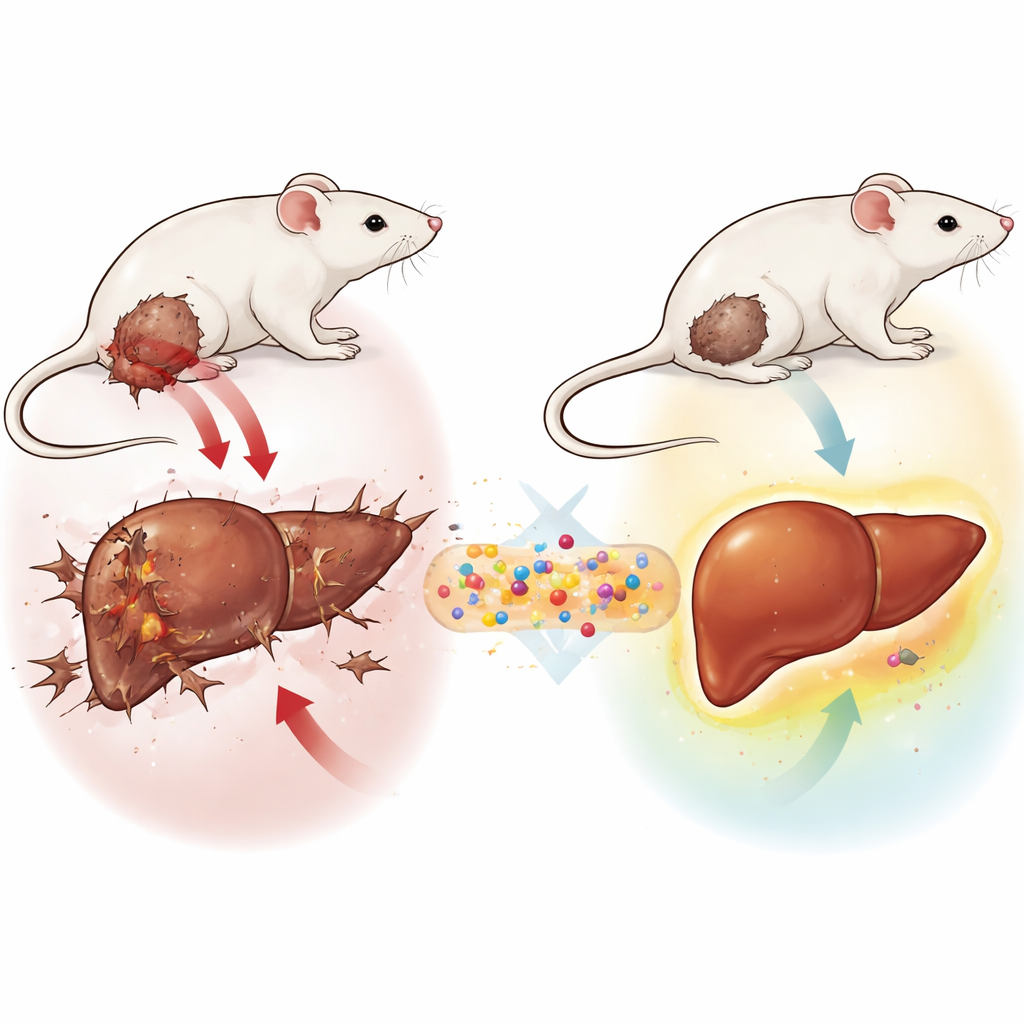
Un sistema de entrega minúsculo con una gran misión
Los investigadores construyeron un sistema nanoestructurado de tres partes denominado GLONF. En su núcleo hay un mineral magnético formado por un material especial a base de hierro. Alrededor de ese núcleo añadieron una cubierta natural derivada de azúcares llamada quitosano, utilizada a menudo en materiales médicos por su seguridad y estabilidad. Finalmente, incorporaron una nueva molécula derivada de azúcar llamada glucosodieno, diseñada para interferir con la necesidad de glucosa de las células cancerosas y atenuar el ambiente ácido y agresivo alrededor de los tumores. Juntos, estos componentes crean un vehículo en miniatura que, en principio, puede ser guiado por imanes, viajar con seguridad por el organismo y liberar un agente anticancerígeno donde más se necesita.
Pruebas en un modelo murino de cáncer similar al de mama
Para evaluar si GLONF podía proteger el hígado durante el cáncer, el equipo utilizó un modelo murino bien establecido llamado tumor sólido de Ehrlich. Este tumor, originalmente derivado del tejido mamario, crece rápidamente bajo la piel y replica muchas características de los cánceres humanos agresivos. Las hembras fueron divididas en grupos: algunas permanecieron sanas, otras recibieron solo la nanoformulación, algunas desarrollaron tumores sin tratamiento y otras recibieron GLONF bien al mismo tiempo que se implantó el tumor o bien después de que el tumor se hubiera formado. Los científicos midieron entonces el tamaño tumoral, marcadores sanguíneos estándar de la salud hepática y una batería de señales químicas y microscópicas de daño y reparación dentro del hígado.
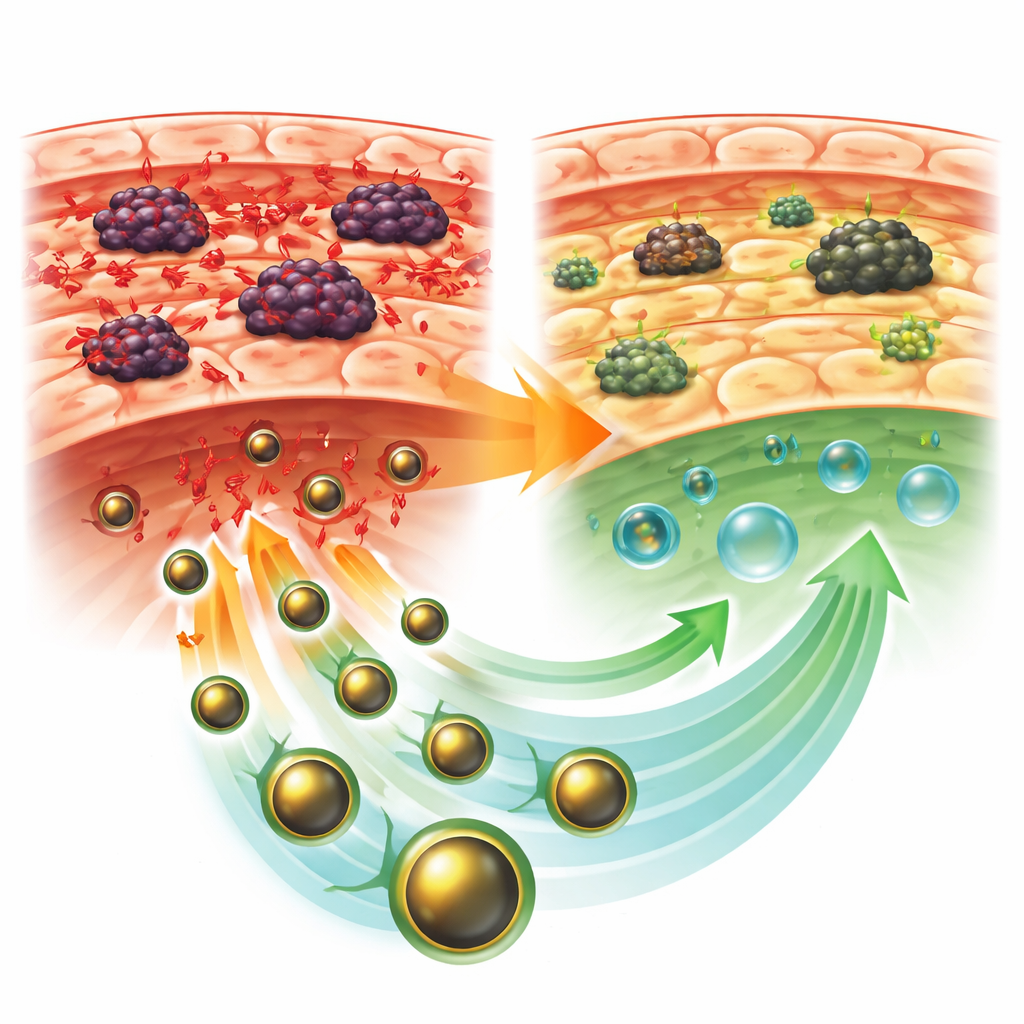
Protección del hígado frente al estrés y al daño
Los ratones portadores de tumores sin tratamiento mostraron el cuadro clásico de lesión hepática. Las enzimas que se filtran a la sangre cuando las células hepáticas están dañadas aumentaron de forma notable, mientras que las proteínas sanguíneas beneficiosas disminuyeron. En el interior del hígado, aumentaron los niveles de subproductos dañinos de la oxidación y cayeron las defensas naturales como enzimas protectoras y glutatión. Las secciones tisulares al microscopio revelaron una arquitectura hepática distorsionada, con células hinchadas y moribundas, cambios similares a cicatrices e intensa invasión de células inflamatorias. En contraste, los ratones tratados con GLONF tuvieron tumores más pequeños y hígados sustancialmente más sanos. Sus análisis de sangre tendieron a la normalidad, el daño oxidativo se redujo y las defensas antioxidantes se recuperaron, sobre todo cuando GLONF se administró después de que el tumor se hubiera formado.
Calmando señales celulares desbocadas
El equipo también examinó dos proteínas clave dentro de las células hepáticas. Una, PCNA, está asociada con la proliferación celular, y la otra, P53, responde al daño del ADN y puede desencadenar la muerte celular. En los ratones con tumor sin tratar, ambos marcadores estaban fuertemente elevados, señalando un estrés intenso y intentos de reparación descontrolados. El tratamiento con GLONF redujo de forma notable la abundancia de estos marcadores en el tejido hepático, lo que sugiere que el nano-sistema disminuyó la necesidad de reparación de emergencia y ayudó a estabilizar el entorno celular. Esto concuerda con los hallazgos bioquímicos y estructurales, y apunta a un alivio coordinado del estrés oxidativo y la lesión.
Qué podría significar esto para la atención del cáncer en el futuro
En resumen, este trabajo muestra que GLONF, un nanoportador magnéticamente sensible y derivado de azúcares, puede reducir tumores en ratones a la vez que protege al hígado de daños graves. Al combinar la entrega dirigida con efectos antioxidantes y metabólicos, el sistema ofrece una vía potencial para que los tratamientos contra el cáncer sean más benignos con los órganos vitales. Aunque estos resultados siguen siendo en animales y están lejos de un uso clínico rutinario, demuestran cómo las nanoestructuras cuidadosamente diseñadas podrían ayudar a que futuras terapias ataquen tumores mientras preservan los filtros naturales del organismo.
Cita: Tousson, E., Atrash, A.E., Abdelrasol, M.Y. et al. Modulation of oxidative stress and P53/PCNA signaling by glucosodiene-loaded nanoferrites (GLONF) in ehrlich solid tumor–induced hepatotoxicity. Sci Rep 16, 12351 (2026). https://doi.org/10.1038/s41598-026-45548-4
Palabras clave: nanomedicina, protección hepática, modelo de cáncer de mama, estrés oxidativo, administración de fármacos