Clear Sky Science · ar
تعديل الإجهاد التأكسدي وإشارات P53/PCNA بواسطة نانوفيريتات محمّلة بالغلوكوزوديين (GLONF) في سمية الكبد الناتجة عن ورم إرليش الصلب
لماذا يهم هذا البحث
غالبًا ما تتسبب علاجات السرطان في تلف أعضاء سليمة، لا سيما الكبد الذي يجب أن يكسر العديد من الأدوية والنفايات الناتجة عن الأورام. تستكشف هذه الدراسة ناقلًا صغيرًا جديدًا موجهًا مغناطيسيًا ينقل مركبًا مضادًا للسرطان مشتقًا من السكر مباشرة نحو الأورام، مع إسناد دورٍ في حماية الكبد من الضرر. للقراء، يقدم البحث لمحة عن كيف يمكن لتقنية النانو والكيمياء الذكية أن تجعلا علاج السرطان يومًا ما أكثر فعالية وأقل سمية.
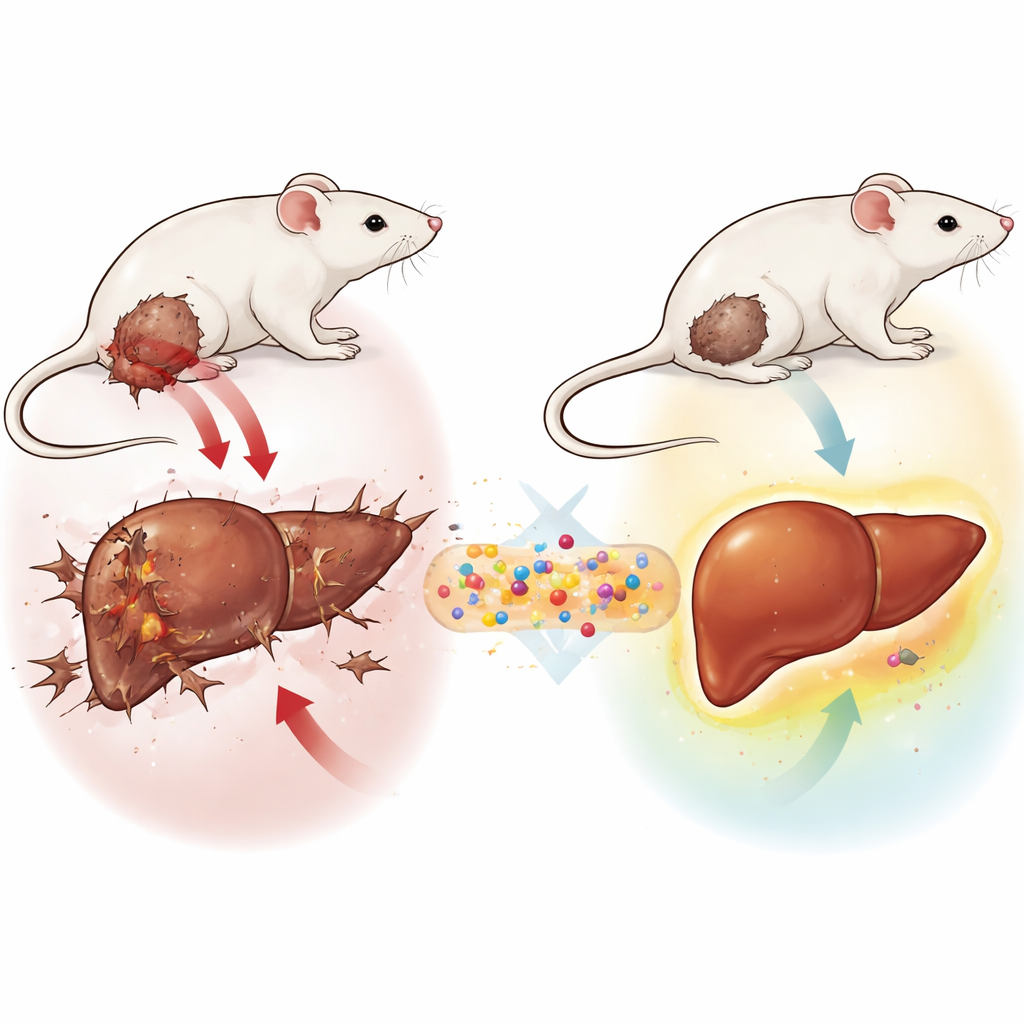
نظام توصيل صغير بمهمة كبيرة
بنى الباحثون نظامًا نانويًا ثلاثي المكونات أطلقوا عليه اسم GLONF. في مركزه نواة معدنية مغناطيسية مصنوعة من مادة حديدية خاصة. حول تلك النواة أضافوا غلافًا طبيعيًّا مشتقًا من السكر يسمى الكيتوزان، وغالبًا ما يُستخدم في المواد الطبية لأمانه واستقراره. وأخيرًا ربطوا جزيئًا جديدًا مشتقًا من السكر يدعى غلوكوزوديين، صُمم للتداخل مع حاجة خلايا السرطان للغلوكوز ولتخفيف البيئة الحمضية القاسية حول الأورام. معًا تخلق هذه المكونات ناقلة مصغرة يمكن، من الناحية النظرية، توجيهها بالمغانط، وأن تنتقل بأمان داخل الجسم، وتطلق العامل المضاد للسرطان حيث يلزم الأمر.
الاختبار في نموذج فأري يشبه سرطان الثدي
لاختبار ما إذا كان GLONF يمكنه حماية الكبد أثناء السرطان، استخدم الفريق نموذجًا فأريًا معتمدًا جيدًا يُدعى ورم إرليش الصلب. هذا الورم، المأخوذ أصلاً من نسيج الثدي، ينمو بسرعة تحت الجلد ويقلد العديد من خصائص السرطانات البشرية العدوانية. وُزعت الإناث الفأرية إلى مجموعات: بقيت بعضهن سليمة، وبعضهن تلقت فقط التشكيل النانوي، وبعضهن نمت لديهن أورام دون علاج، وأخريات تلقت GLONF إما في وقت زراعة الورم أو بعد تشكل الورم. ثم قاس العلماء حجم الورم، ومعايير دم معيارية لصحة الكبد، ومجموعة من العلامات الكيميائية والمجهرية للضرر والإصلاح داخل الكبد.
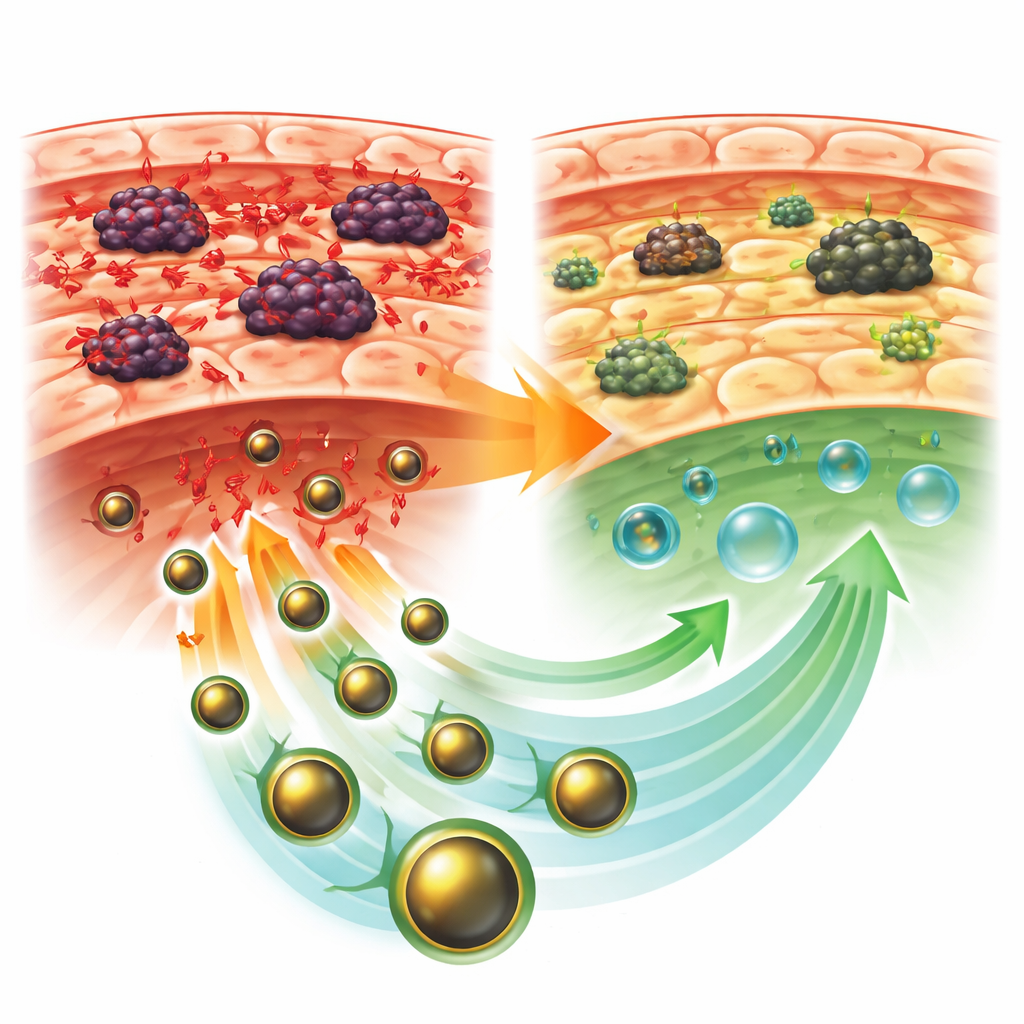
حماية الكبد من الإجهاد والضرر
أظهرت الفئران الحاملة للأورام دون علاج صورة كلاسيكية لإصابة الكبد. ارتفعت الإنزيمات التي تتسرب إلى الدم عند تلف خلايا الكبد بشكل حاد، بينما انخفضت البروتينات المفيدة في الدم. داخل الكبد، زادت مستويات نواتج الأكسدة الضارة، وتراجعت الدفاعات الطبيعية مثل الإنزيمات الواقية والجلوتاثيون. كشفت مقاطع الأنسجة تحت المجهر عن تشوه في بنية الكبد، مع خلايا متورمة وتموتية، وتغيرات تشبه الندبة، وغزو كبير للخلايا الالتهابية. بالمقابل، كانت الفئران المعالجة بـGLONF تمتلك أورامًا أصغر وكبدًا بصحة أفضل إلى حد كبير. عادت نتائج اختبارات الدم نحو الطبيعي، وانخفضت الآثار الأكسدية، وانتعشت الدفاعات المضادة للأكسدة، لا سيما عندما أعطي GLONF بعد تكوُّن الورم.
تهدئة إشارات الخلايا المتسارعة
فحص الفريق أيضًا بروتينين رئيسيين داخل خلايا الكبد. أحدهما، PCNA، مرتبط بتكاثر الخلايا، والآخر، P53، يستجيب لتلف الحمض النووي ويمكن أن يحفز موت الخلايا. في الفئران الحاملة للأورام دون علاج، ارتفعت كلتا العلامتين بقوة، مشيرةً إلى ضغط شديد ومحاولات إصلاح خارجة عن السيطرة. خفضت معالجة GLONF بشكل ملحوظ وفرة هذه العلامات في نسيج الكبد، مما يوحي بأن النظام النانوي قلل الحاجة إلى إصلاح الطوارئ وساعد في استقرار البيئة الخلوية. يتوافق هذا مع النتائج البيوكيميائية والتركيبية، مشيرًا إلى تخفيف منسق للإجهاد التأكسدي والضرر.
ما الذي قد يعنيه هذا لرعاية السرطان المستقبلية
باختصار، تظهر هذه الدراسة أن GLONF، ناقل نانوي مستجيب مغناطيسيًا ومشتق من السكر، قادر على تقليص الأورام في الفئران مع حماية الكبد من أضرار خطيرة. من خلال الجمع بين التوصيل المستهدف والتأثيرات المضادة للأكسدة والتمثيلية، يقدم النظام وسيلة محتملة لجعل علاج السرطان ألطف على الأعضاء الحيوية. وعلى الرغم من أن هذه النتائج ما تزال في حيوانات وبعيدة عن الاستخدام السريري الروتيني، فإنها توضح كيف قد تساعد البنى النانوية المصممة بعناية العلاجات المستقبلية على مهاجمة الأورام مع حفظ وظائف المرشحات الطبيعية في الجسم.
الاستشهاد: Tousson, E., Atrash, A.E., Abdelrasol, M.Y. et al. Modulation of oxidative stress and P53/PCNA signaling by glucosodiene-loaded nanoferrites (GLONF) in ehrlich solid tumor–induced hepatotoxicity. Sci Rep 16, 12351 (2026). https://doi.org/10.1038/s41598-026-45548-4
الكلمات المفتاحية: الطب النانوي, حماية الكبد, نموذج سرطان الثدي, الإجهاد التأكسدي, توصيل الأدوية