Clear Sky Science · he
וויסות מתח חמצוני וסיגנלינג P53/PCNA על ידי ננופראיטים טעוני גלוקוזודין (GLONF) ברעילות כבד המוּגרמת על ידי גידול מוצק של אירליך
מדוע מחקר זה חשוב
טיפולים בסרטן לעתים קרובות פוגעים באיברים בריאים, ובפרט בכבד, שאחראי לפירוק תרופות רבות ולסילוק תוצרי פסולת של הגידולים. מחקר זה חוקר נשא חדש, זעיר ובהנחיה מגנטית, שמוביל תרכובת אנטי‑סרטנית מבוססת סוכר ישירות אל הגידולים ובמקביל מגן על הכבד מפגיעה. לקוראים הוא מציע מבט על האופן שבו ננוטכנולוגיה וכימיה חכמה עשויות יום אחד להפוך את טיפול הסרטן ליעיל פחות ורעיל פחות.
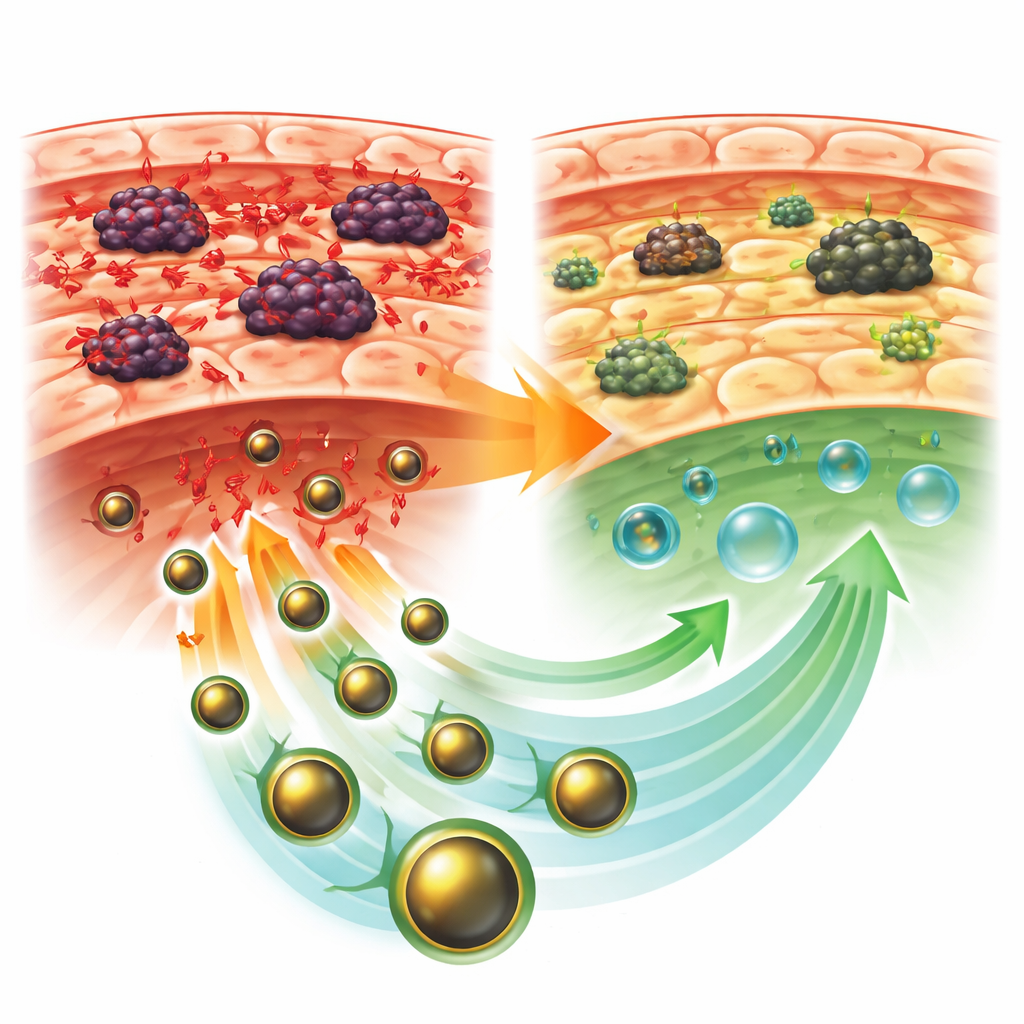
מערכת משלוח זעירה עם משימה גדולה
החוקרים בנו מערכת ננומטרית תלת‑חלקית שנקראת GLONF. במרכז שלה נמצא ליבת מינרל מגנטית העשויה מחומר ייחודי מבוסס ברזל. סביב הליבה הוסיפו מעטפת טבעית מבוססת סוכר בשם כיטוזן, המשמשת לעתים קרובות בחומרים רפואיים בשל בטיחותה ויציבותה. לסיום, צירפו מולקולה חדשה נגזרת סוכר בשם גלוקוזודין, שתוכננה להפריע לתאבון הגלוקוז של תאי סרטן ולרכך את הסביבה החומצית והאלימה סביב הגידולים. ביחד, רכיבים אלה יוצרים רכב זעיר שניתן, עקרונית, לכוונו באמצעות מגנט, שייסע בבטחה בגוף וישחרר את הסוכן האנטי‑סרטני במקום שבו הוא נדרש ביותר.
בדיקות במודל עכבר המדמה סרטן דמוי שד
כדי לבדוק האם GLONF יכול להגן על הכבד במהלך מחלת הסרטן, הצוות השתמש במודל עכבר מבוסס היטב הנקרא גידול מוצק של אירליך. גידול זה, שמקורו ברקמת שד, גדל במהירות מתחת לעור ומחקה תכונות רבות של סרטן אנושי אגרסיבי. עכברות חולקו לקבוצות: חלק נשארו בריאות, חלק קיבלו רק את הננו‑פורמולציה, חלק פיתחו גידולים ללא טיפול ואחרות קיבלו GLONF או בו זמנית עם השתלת הגידול או לאחר שהגידול כבר נוצר. המדענים מדדו אורך גידול, סמני דם סטנדרטיים של בריאות הכבד, וסדרה של סימנים כימיים ומיקרוסקופיים לנזק ולתיקון בתוך הכבד.
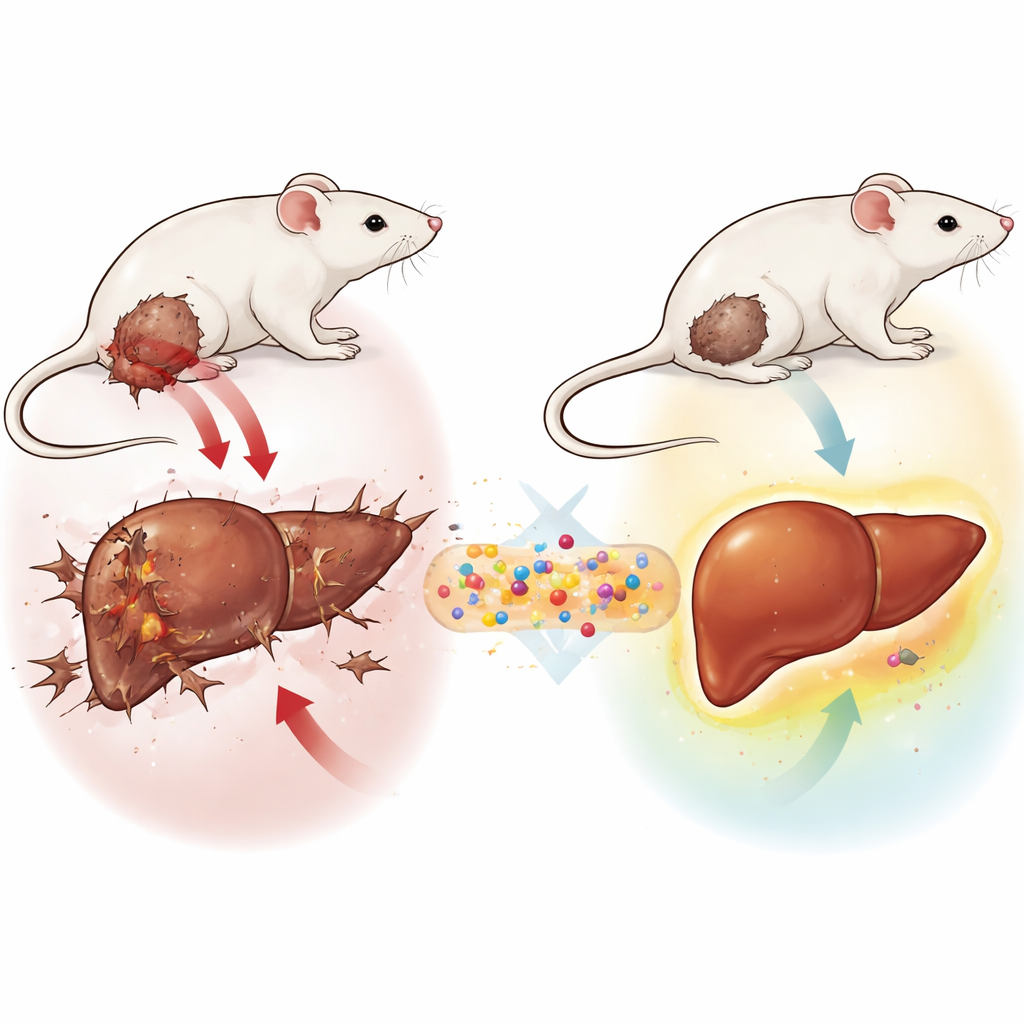
הגנה על הכבד מפני מתח ונזק
עכברים נשאי גידול שלא קיבלו טיפול הציגו תמונה קלאסית של פגיעה בכבד. אנזימים שנשטפים אל הדם כאשר תאי הכבד ניזוקים עלו במידה ניכרת, בזמן שחלבוני דם תומכים ירדו. בתוך הכבד עלו רמות תוצרי חמצון מזיקים, וההגנות הטבעיות כגון אנזימים מגן וגלוטתיון ירדו. פרוסות רקמה במיקרוסקופ חשפו ארכיטקטורה כבדית מעוותת, עם תאים נפוחים ומתים, שינויים דמויי צלקת וחדירה דלקתית כבדה של תאים. לעומת זאת, עכברים שקיבלו טיפול ב‑GLONF היו בעלי גידולים קטנים יותר וכבדות בריאות בהרבה. בדיקות הדם שלהם חזרו לכיוון הנורמלי, הנזק החמצוני פחת וההגנות האנטי‑חמצוניות השתקמו, במיוחד כאשר ה‑GLONF ניתן לאחר שהגידול כבר הוקם.
הרגעת אותות תאי שנמלטו משליטה
הצוות בחן גם שתי חלבונים מרכזיים בתוך תאי הכבד. אחד, PCNA, מקושר להתרבות תאים, והשני, P53, מגיב לנזק ל‑DNA ויכול להפעיל מוות תאי. בעכברים נשאי גידול ללא טיפול שניהם היו מורמים במידה ניכרת, מה שמעיד על מתח עז וניסיונות תיקון בלתי מבוקרים. טיפול ב‑GLONF הוריד במידה ניכרת את רמות הסמנים הללו ברקמת הכבד, מרמז שהננו‑מערכת הקטינה את הצורך בתיקון חירום וסייעה לייצב את הסביבה התאית. זה מתאים לממצאים הביוכימיים והמבניים, ומצביע על הקלה מתואמת במתח החמצוני ובנזק.
מה זה עשוי להשפיע על טיפול בסרטן בעתיד
לסיכום, עבודה זו מראה כי GLONF, נשא ננו־מגנטי מבוסס סוכר, יכול לצמצם גידולים בעכברים ובאותו זמן להגן על הכבד מפגיעה חמורה. על ידי שילוב של משלוח ממוקד עם השפעות אנטי‑חמצוניות ומטבוליות, המערכת מציעה דרך פוטנציאלית להפוך את טיפולי הסרטן לרחמנים יותר כלפי איברים חיוניים. אף שעדיין מדובר בתוצאות בחיות והן רחוקות משימוש שגרתי קליני, הן ממחישות כיצד מבנים ננו־מהונדסים בקפידה עשויים לעזור לטיפולים עתידיים לתקוף גידולים תוך שמירה על מסנני הגוף הטבעיים.
ציטוט: Tousson, E., Atrash, A.E., Abdelrasol, M.Y. et al. Modulation of oxidative stress and P53/PCNA signaling by glucosodiene-loaded nanoferrites (GLONF) in ehrlich solid tumor–induced hepatotoxicity. Sci Rep 16, 12351 (2026). https://doi.org/10.1038/s41598-026-45548-4
מילות מפתח: ננודרוגו, הגנה על הכבד, מודל סרטן השד, מתח חמצוני, התמסר תרופתי