Clear Sky Science · de
Modulation von oxidativem Stress und P53/PCNA-Signalgebung durch glucosodien-beladene Nanoferrite (GLONF) bei durch Ehrlich-Festtumor induzierter Hepatotoxizität
Warum diese Forschung wichtig ist
Krebsbehandlungen schädigen oft gesunde Organe, insbesondere die Leber, die viele Arzneimittel und Abbauprodukte von Tumoren verarbeiten muss. Diese Studie untersucht einen neuen, winzigen, magnetisch steuerbaren Träger, der eine zuckerbasierte anticancerale Verbindung gezielt zu Tumoren transportiert und gleichzeitig die Leber vor Schäden schützt. Für Leserinnen und Leser bietet sie einen Einblick, wie Nanotechnologie und clevere Chemie eines Tages die Krebstherapie wirkungsvoller und weniger toxisch machen könnten.
Ein winziges Transportsystem mit großer Aufgabe
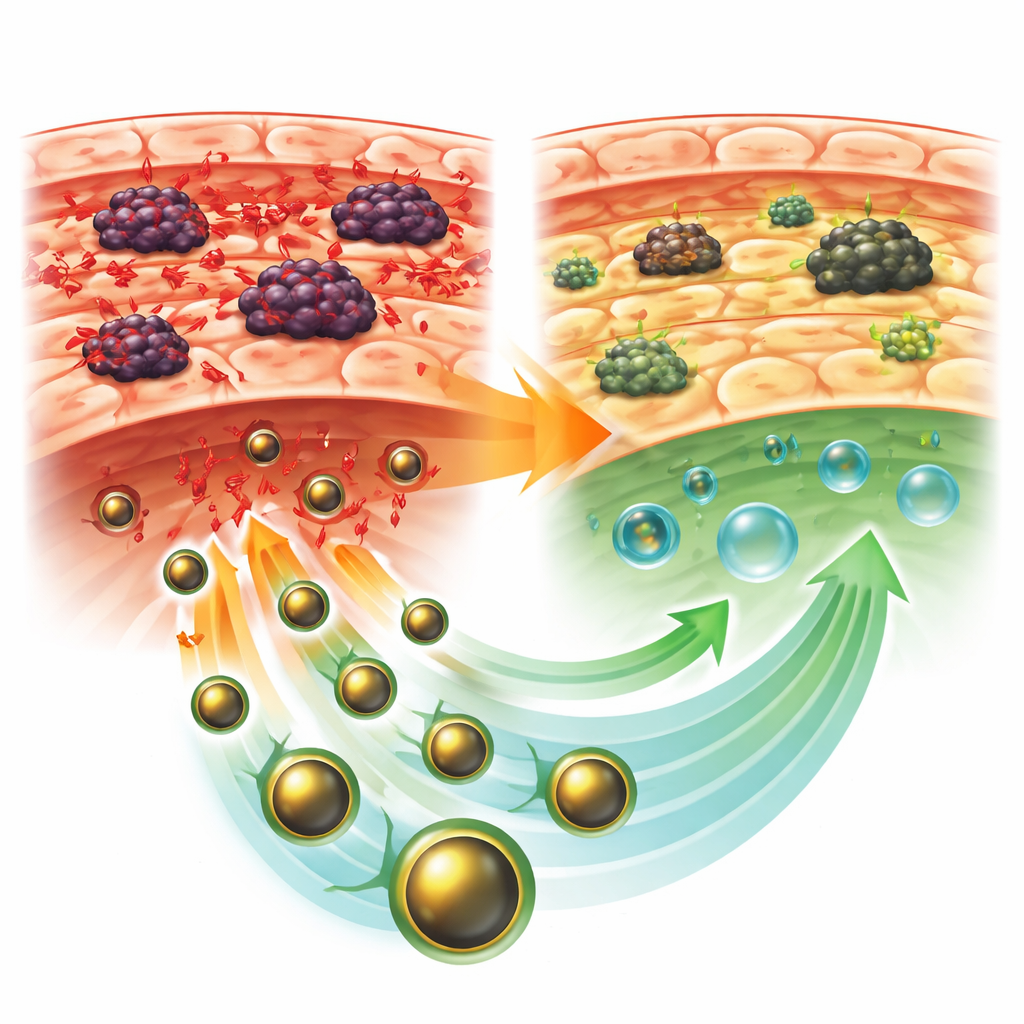
Die Forschenden bauten ein dreiteiliges nanoskaliges System namens GLONF. Im Zentrum steht ein magnetischer Mineral-Kern aus einem speziellen eisenbasierten Material. Um diesen Kern legten sie eine natürliche, zuckerartige Hülle aus Chitosan, das wegen seiner Sicherheit und Stabilität häufig in medizinischen Materialien verwendet wird. Schließlich befestigten sie ein neues, zuckerabgeleitetes Molekül namens Glucosodien, das darauf ausgelegt ist, den Glukosebedarf von Krebszellen zu stören und das raue, saure Milieu um Tumoren zu mildern. Zusammen bilden diese Komponenten ein winziges Vehikel, das prinzipiell magnetisch gesteuert werden kann, sicher im Körper zirkuliert und den Wirkstoff dort freisetzt, wo er am dringendsten benötigt wird.
Tests in einem mausähnlichen Brustkrebsmodell
Um zu prüfen, ob GLONF die Leber während einer Krebserkrankung schützen kann, verwendete das Team ein etabliertes Mausmodell, den Ehrlich-Festtumor. Dieser Tumor, ursprünglich aus Brustgewebe gewonnen, wächst schnell unter der Haut und ahmt viele Merkmale aggressiver menschlicher Krebserkrankungen nach. Weibliche Mäuse wurden in Gruppen aufgeteilt: einige blieben gesund, einige erhielten nur die Nanoformulierung, einige entwickelten Tumoren ohne Behandlung, und andere bekamen GLONF entweder gleichzeitig mit der Tumorimplantation oder nachdem sich der Tumor gebildet hatte. Die Wissenschaftler maßen dann Tumorgröße, gängige Blutmarker der Lebergesundheit sowie ein Bündel chemischer und mikroskopischer Zeichen von Schädigung und Reparatur in der Leber.
Die Leber vor Stress und Schäden schützen
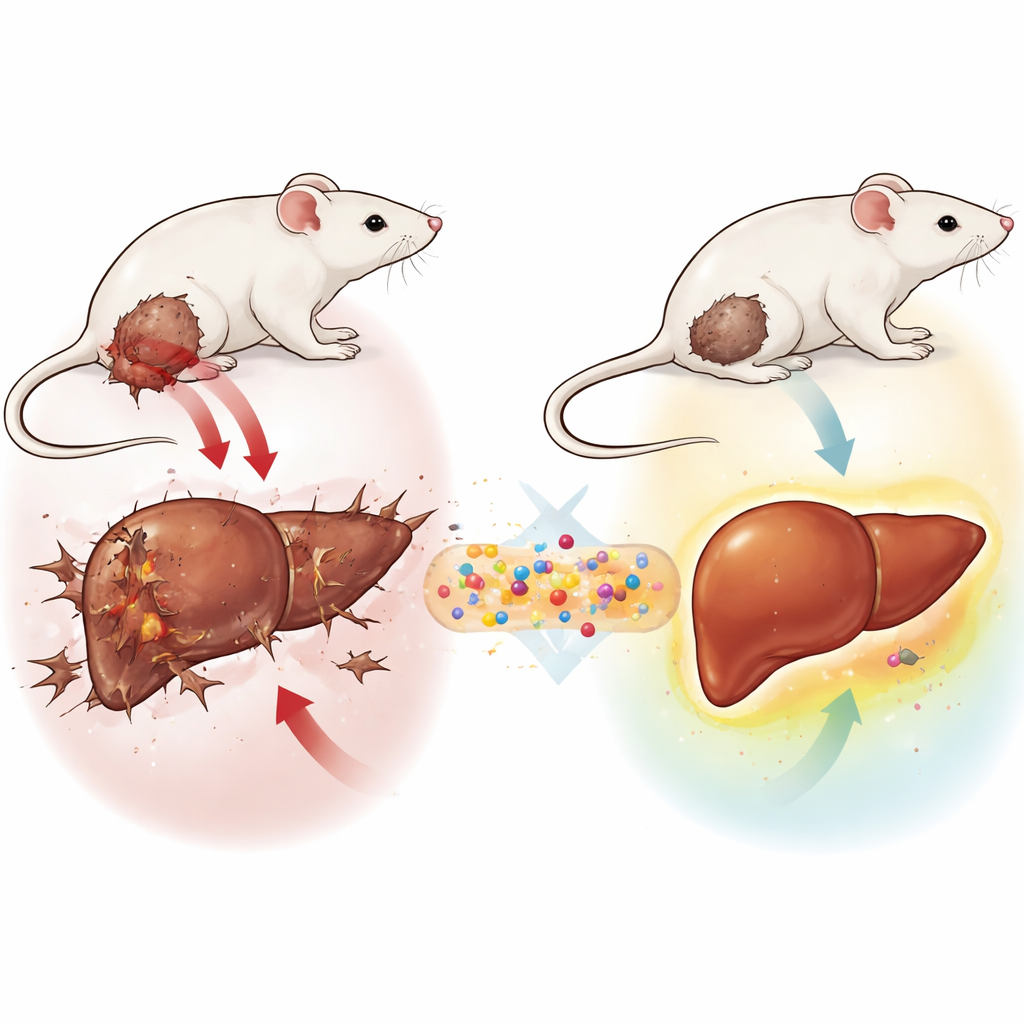
Mäuse mit unbehandelten Tumoren zeigten ein klassisches Bild von Leberschädigung. Enzyme, die ins Blut gelangen, wenn Leberzellen beschädigt sind, stiegen stark an, während nützliche Bluteiweiße zurückgingen. In der Leber nahmen die Konzentrationen schädlicher Oxidationsnebenprodukte zu, und natürliche Abwehrmechanismen wie schützende Enzyme und Glutathion fielen ab. Gewebeschnitte unter dem Mikroskop zeigten eine verzerrte Leberarchitektur mit angeschwollenen und sterbenden Zellen, narbenähnlichen Veränderungen und starker Invasion entzündlicher Zellen. Im Gegensatz dazu hatten Mäuse, die mit GLONF behandelt wurden, kleinere Tumoren und deutlich gesündere Lebern. Ihre Blutwerte bewegten sich wieder in Richtung Normalbereich, oxidative Schäden wurden reduziert und die antioxidativen Abwehrkräfte erholten sich, insbesondere wenn GLONF verabreicht wurde, nachdem der Tumor bereits gebildet war.
Beruhigung entgleister Zellsignale
Das Team untersuchte auch zwei Schlüsselproteine in Leberzellen. Eines, PCNA, ist mit Zellproliferation verbunden, das andere, P53, reagiert auf DNA-Schäden und kann den Zelltod auslösen. Bei tumortragenden Mäusen ohne Behandlung waren beide Marker stark erhöht, was auf intensiven Stress und unkontrollierte Reparaturversuche hinweist. Die GLONF-Behandlung senkte die Häufigkeit dieser Marker im Lebergewebe deutlich, was darauf hindeutet, dass das Nanosystem den Bedarf an Notfallreparaturen reduzierte und zur Stabilisierung der zellulären Umgebung beitrug. Dies stimmt mit den biochemischen und strukturellen Befunden überein und deutet auf eine koordinierte Abschwächung von oxidativem Stress und Schädigung hin.
Was das für die zukünftige Krebsversorgung bedeuten könnte
Zusammenfassend zeigt diese Arbeit, dass GLONF, ein magnetisch reagierbarer, zuckerbasierter Nano-Träger, Tumoren bei Mäusen verkleinern und gleichzeitig die Leber vor schweren Schäden schützen kann. Durch die Kombination zielgerichteter Abgabe mit antioxidativen und metabolischen Effekten bietet das System einen möglichen Weg, Krebstherapien schonender für lebenswichtige Organe zu gestalten. Obwohl diese Ergebnisse noch an Tieren gewonnen wurden und weit von einer routinemäßigen klinischen Anwendung entfernt sind, demonstrieren sie, wie sorgfältig konstruierte Nanostrukturen künftigen Therapien helfen könnten, Tumore anzugreifen und gleichzeitig die natürlichen Filter des Körpers zu schonen.
Zitation: Tousson, E., Atrash, A.E., Abdelrasol, M.Y. et al. Modulation of oxidative stress and P53/PCNA signaling by glucosodiene-loaded nanoferrites (GLONF) in ehrlich solid tumor–induced hepatotoxicity. Sci Rep 16, 12351 (2026). https://doi.org/10.1038/s41598-026-45548-4
Schlüsselwörter: Nanomedizin, Leberprotektion, Brustkrebsmodell, oxidativer Stress, Arzneimittelabgabe